OPO结构脂的酶法制备毕业论文
2020-06-14 16:30:26
摘 要
本文中,是对酶法制备OPO结构脂的最佳实验路线的研究,分别控制该反应的含水量、反应底物摩尔比、反应温度、反应时间、加酶量这五种不同的实验条件因素来进行OPO结构脂的酶法制备,并对最终产物的C52含量进行比较,并且还以化学法路线合成OPO结构脂,控制反应底物摩尔比、反应温度、反应底物含水量、反应时间、催化剂含量等一些实验合成因素来得出OPO结构脂的化学法制备的最佳路线,然后将两种实验结果进行比对,并分析得出各自的优缺点,以及关于酸解法的不足所在。实验结果表明:酶法制备OPO的最佳实验路线为:⑴3%的反应底物含水量 ⑵70℃的反应温度 ⑶9%的加酶量 ⑷PPP:OA=1:6(摩尔比) ⑸反应最佳时长为10h;而化学法的最佳反应路线为:⑴PPP:OA=1:4的反应底物摩尔比 ⑵3%的反应底物含水量 ⑶5%的催化剂含量 ⑷6h的反应时间。通过化学法合成该物质,对反应条件的要求很高,且在整个过程中的能量消耗大,目的产物的分离比较困难,而且还会伴随着生而成很多有毒副产物,不符合大规模工业化的要求。与化学法催化相对比而言,酶法催化合成不易产生副产物,不会污染环境,还能够减轻产品生产过程中下游的分离任务与工作。因此,酶法催化技术是未来社会绿色化学工业的发展方向。但是总而言之,酸解法如今还没能够被广泛使用,并实现大规模工业化的重要因素就是反应之后脂肪酸回收难度高,原子利用率不高,影响经济效益,即成本核算以及实际利益方面达不到社会发展的要求与期望。
关键词:OPO结构脂 脂肪酶 化学催化剂 控制变量 绿色发展 规模化。
Enzymatic preparation of OPO structural lipids
Abstract
In this paper, we study the best experimental route of enzymatic preparation of OPO structural lipids, and control the moisture content of the reaction, the molar ratio of the reaction substrate.The five different experimental conditions The enzymatic preparation of OPO structural lipids was carried out and the C52 content of the final product was compared. The OPO structure was also synthesized by chemical route, the molar ratio of reaction substrate, reaction temperature, reaction substrate water content, reaction time, Catalyst content and other experimental factors to obtain the OPO structure of the chemical preparation of the best route, and the results of the two methods for comparison, and analysis of the advantages and disadvantages of these two methods, as well as the acid solution of the defects. The experimental results show that the best experimental route of enzymatic preparation of OPO is 3% of the reaction substrate water content, 70 ℃ reaction temperature, 9% enzyme dosage, 1: 6 reaction substrate molar ratio, 10h reaction time And the best reaction route of the chemical method is 1: 4 molar ratio of the reaction substrate, 3% of the reaction substrate water content, 5% of the catalyst content, 6h reaction time. Chemical synthesis of synthetic routes will produce toxic by-products, demanding reaction conditions, high energy consumption, follow-up product separation steps cumbersome, not suitable for large-scale industrial development, and easy to cause environmental pollution and other issues, do not meet the contemporary society to the environment- Social change. In contrast to chemical catalysis, enzymatic synthesis is not easy to produce by-products, does not pollute the environment, but also can reduce the downstream production process of separation tasks and work. Therefore, the enzymatic catalytic technology is the future development direction of the social green chemical industry. But in short, the acidolysis method has not yet been widely used, and the realization of large-scale industrialization is an important factor in the reaction after the recovery of fatty acids is difficult, the utilization of atoms is not high, affecting economic efficiency, that is, the cost of accounting and the actual benefits of social Development requirements and expectations.
Key words: OPO structure fat,;lipase; chemical catalyst; control variable,;green development;scal
目录
摘要 I
Abstract II
第一章 文 献 综 述 1
1.1 OPO的构效关系 1
1.2 OPO的酶法合成 2
1.2.1生物催化剂——脂肪酶 2
1.2.2固定化脂肪酶的应用以及限制因素 3
1.3 OPO的合成路线 4
1.3.1OPO的酯酯交换合成路线 4
1.3.2 OPO的醇解法合成路线 5
1.3.3 OPO的酸解法合成路线 6
1.4 OPO的酸解法合成路线及其相关优缺点 6
1.5 实验思路 7
第二章 OPO结构脂的合成 8
2.1实验试剂与仪器 8
2.2实验方法 9
2.2.1酶法制备OPO结构脂 9
2.2.2化学法制备OPO结构脂 9
2.3 液相检测 10
2.3.1 液相检测的基本定义 10
2.2.2 液相检测的优缺点 10
2.4 气相检测 12
2.4.1 气相检测的基本定义 12
2.4.2气相检测的工作原理 12
2.4.3 气相检测的优缺点 13
2.5 薄层色谱法 14
2.5.1薄层色谱法的基本应用原理 14
2.5.2 薄层色谱法的注意事项 14
2.6 具体检测操作流程 14
2.6.1 TLC法检测油脂 14
2.6.2 油脂的萃取与甲酯化处理 15
2.6.3 Sn-2位脂肪酸的检测 15
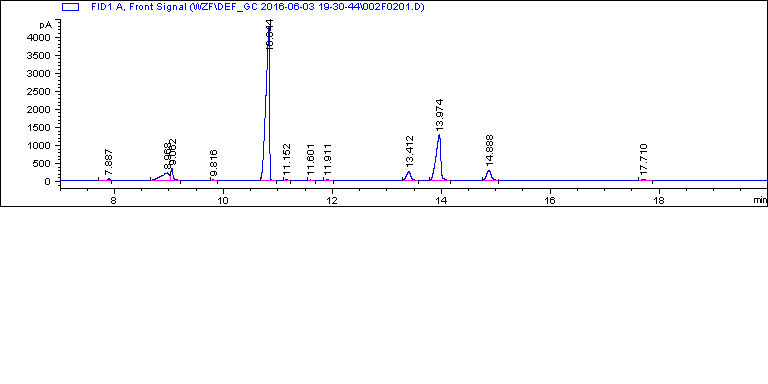
2.6.4实验产物气相结果图以及液相结果图与分析 16
第三章 化学法和酶法催化的结果比较、讨论与展望 21
3.1 酶法与化学法合成OPO结构脂的最适条件与结果比较 21
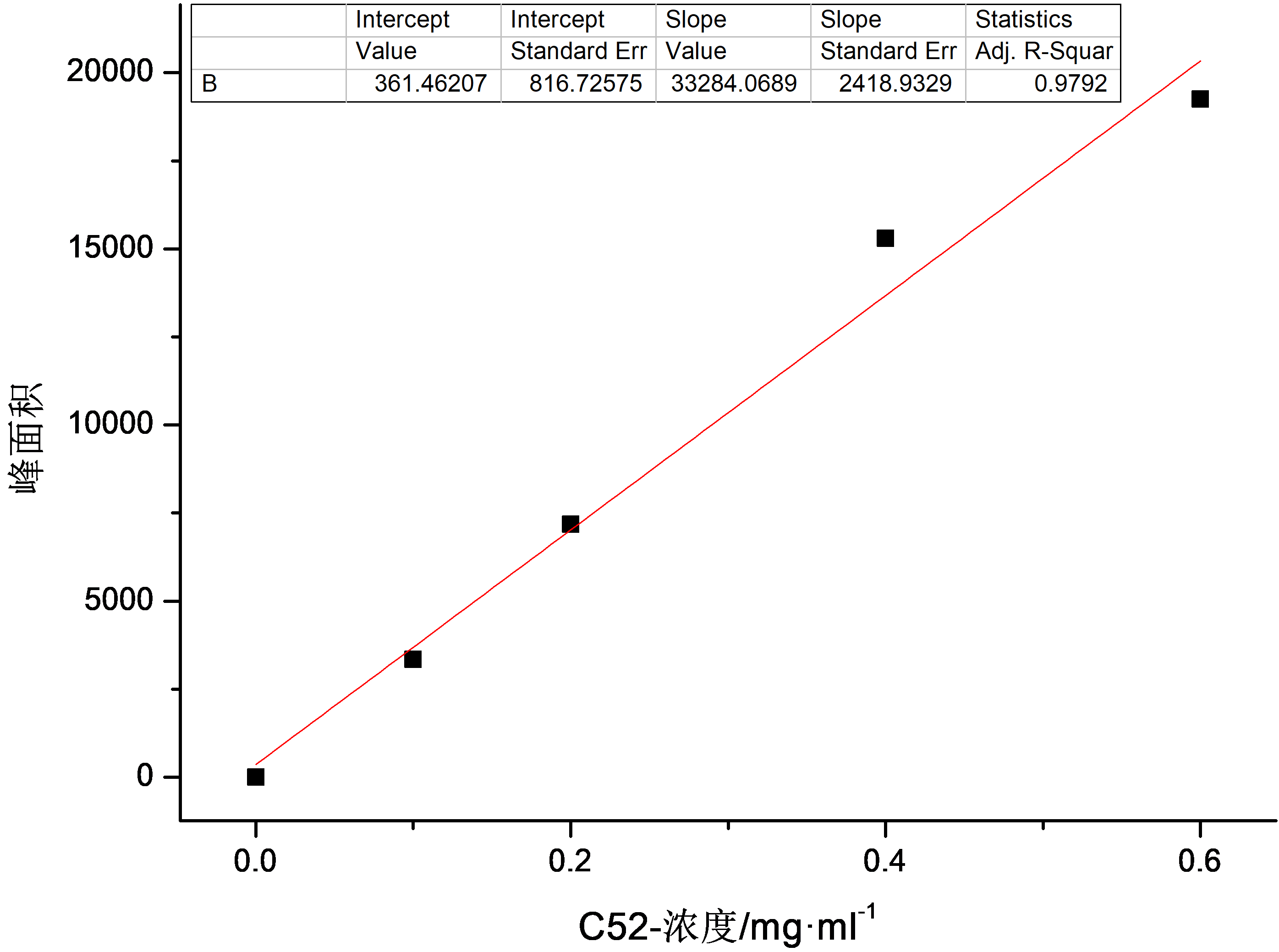
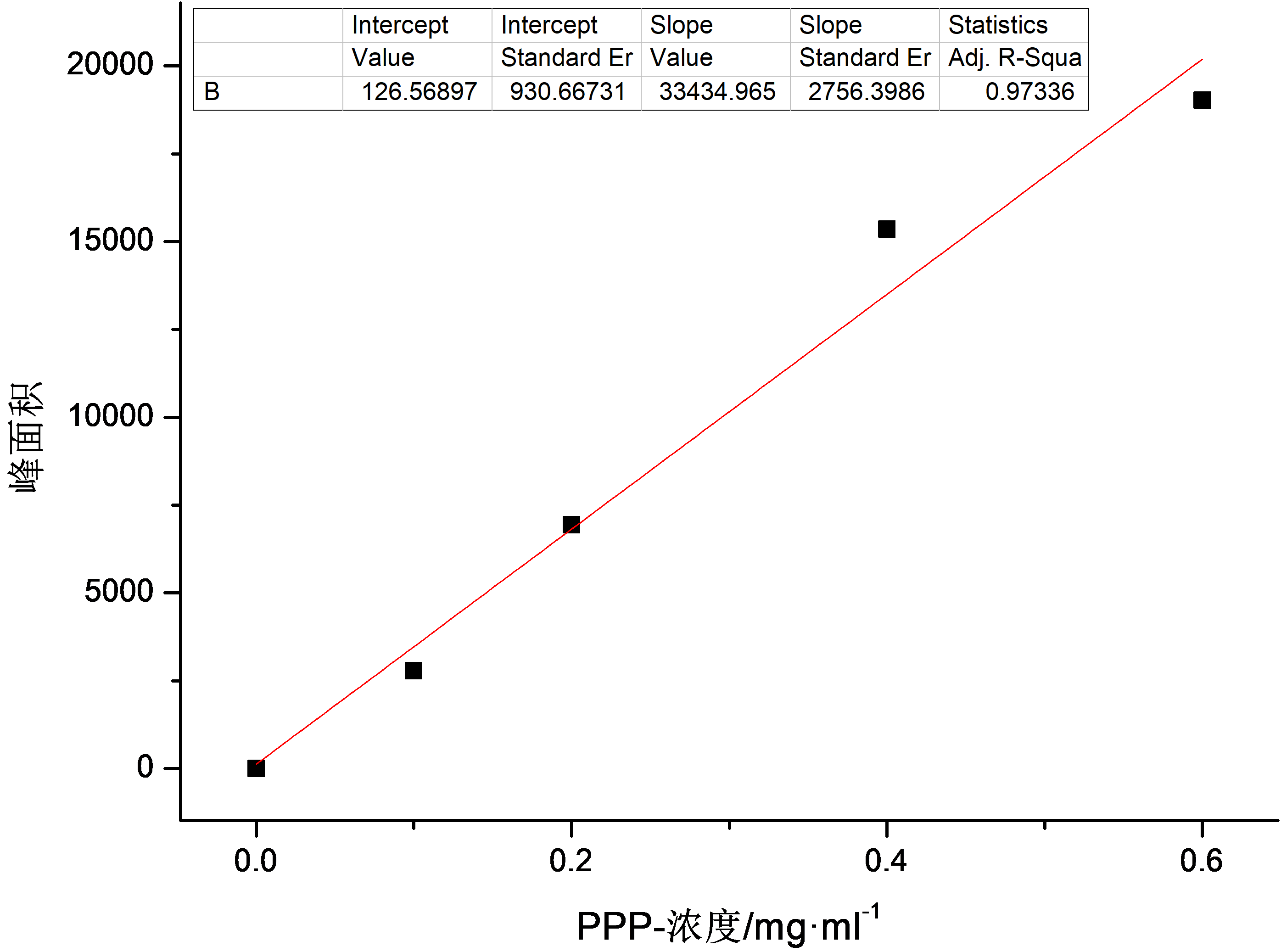
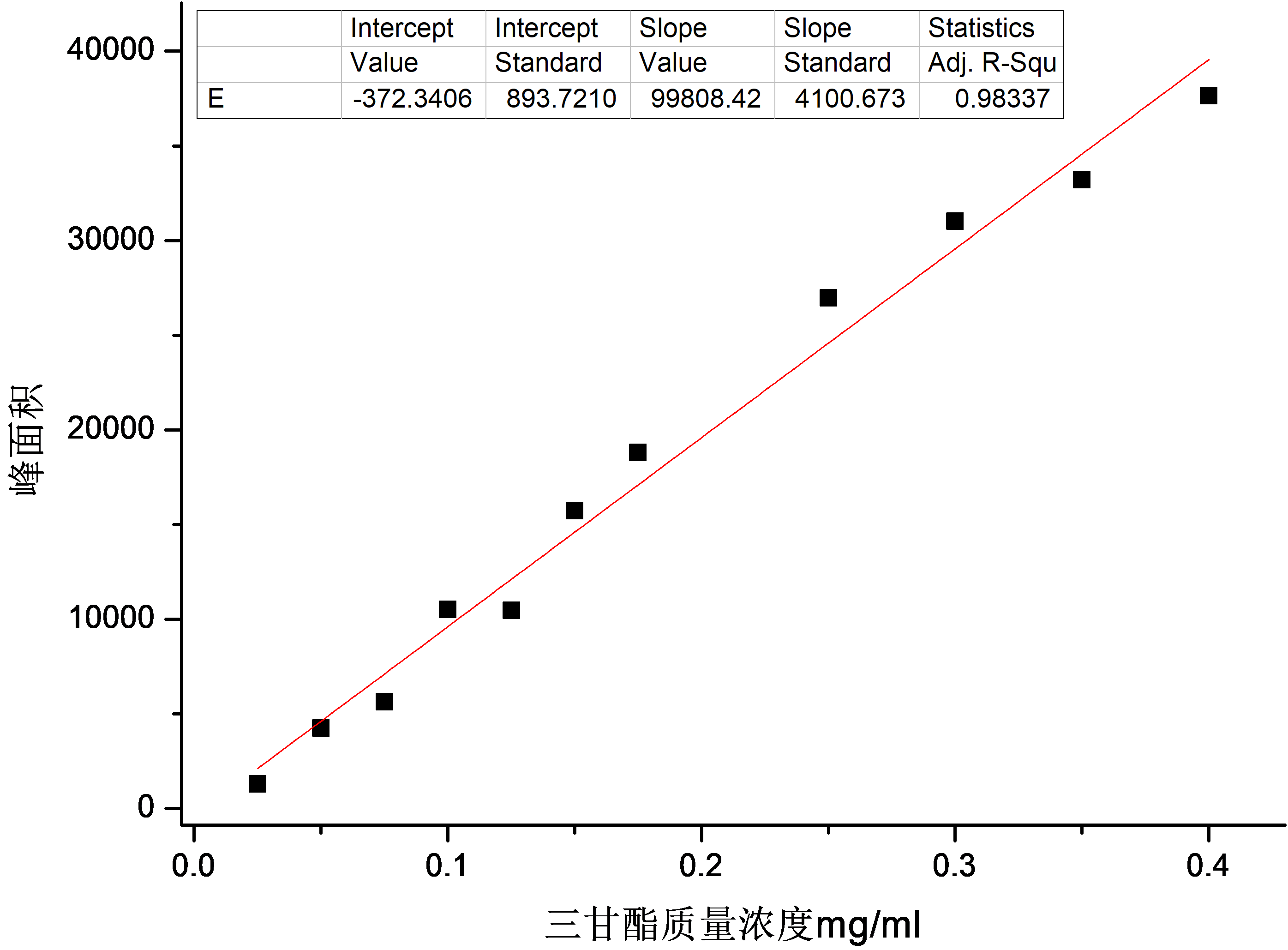
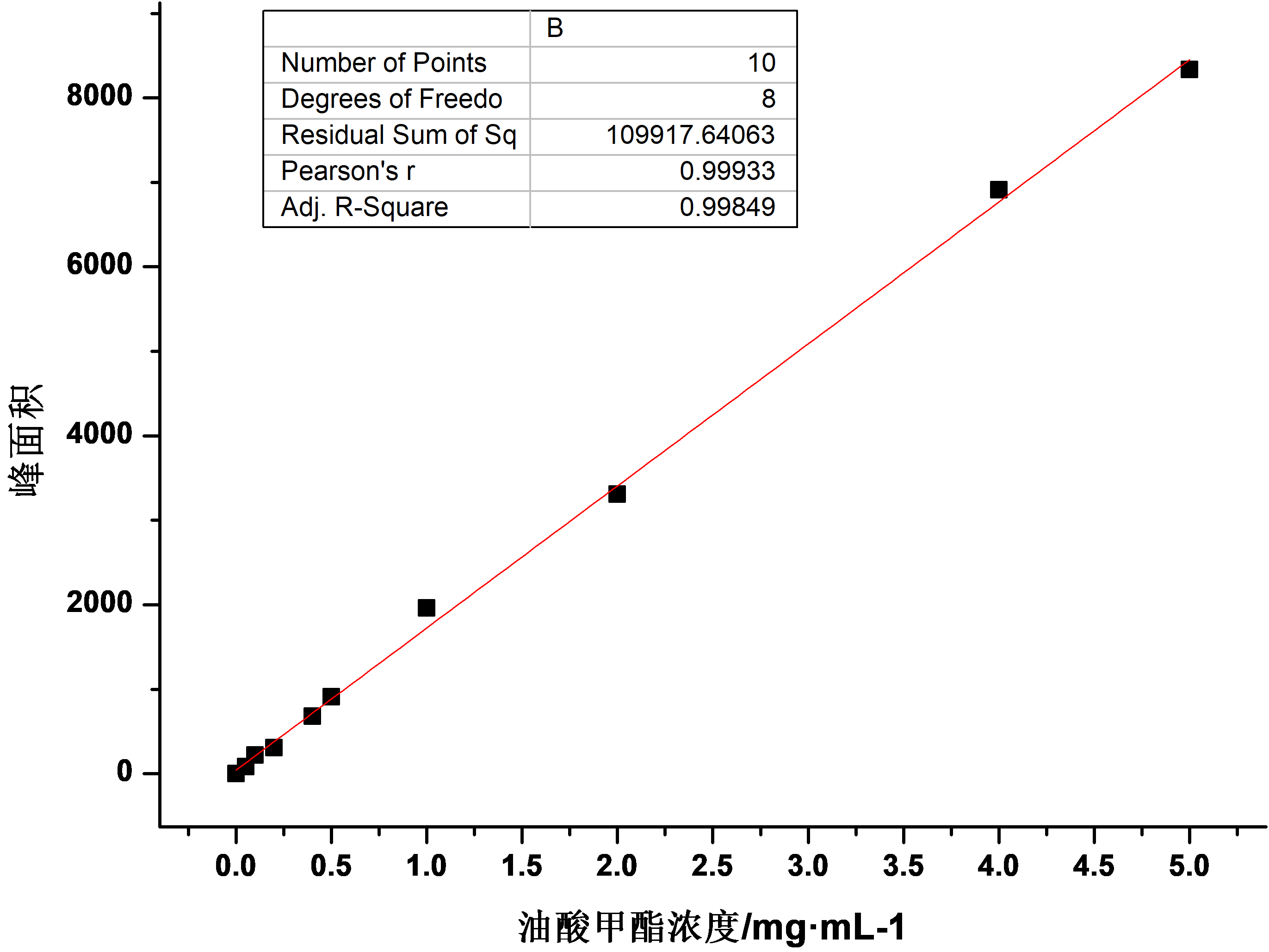
3.1.1酶法制备OPO结构脂的图像结果与分析 21
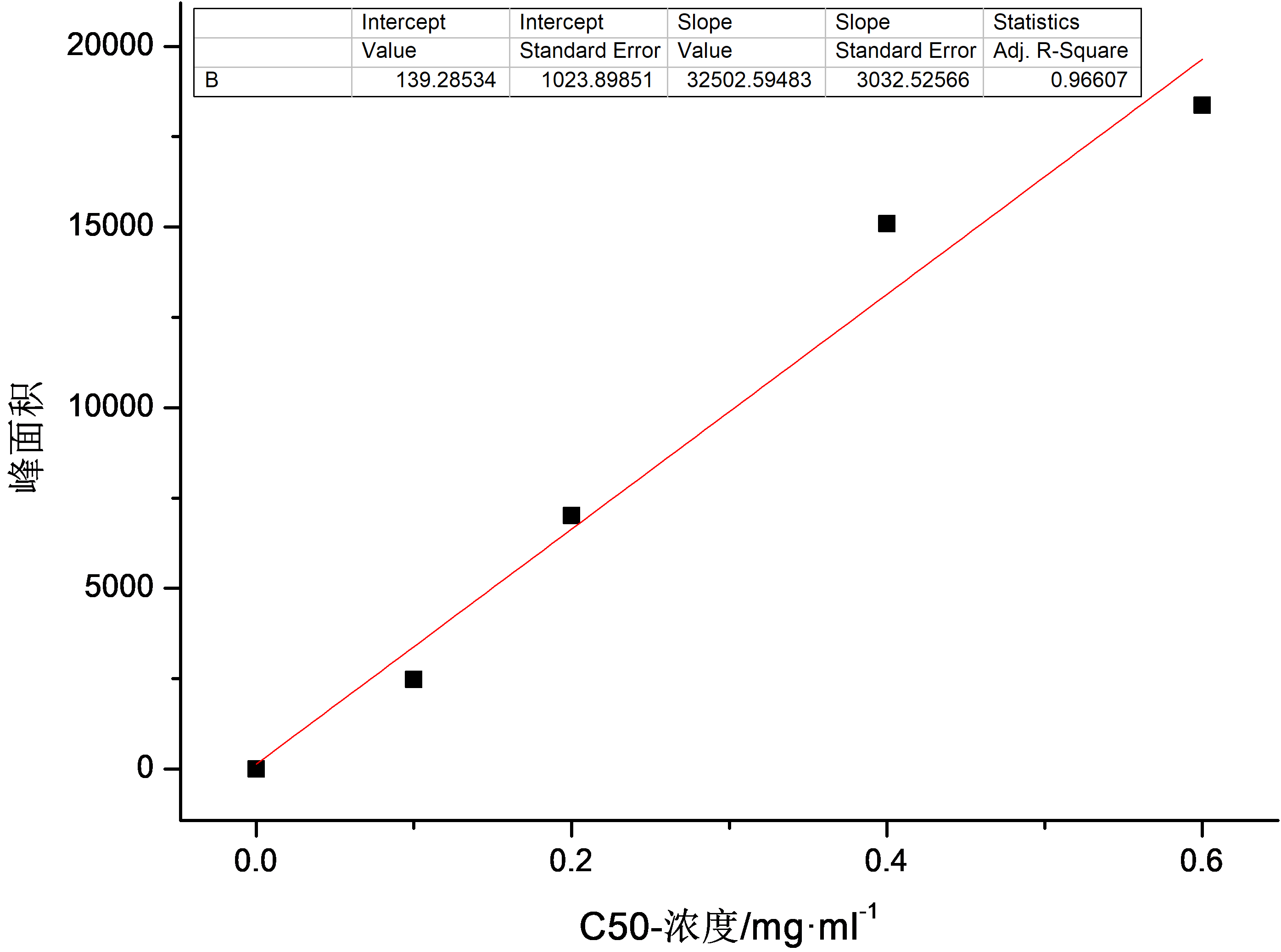
3.1.2化学法合成OPO结构脂结果图与分析 22
3.2酶法合成OPO结构脂的优缺点 24
3.3 OPO结构脂合成的前景与展望 25
参考文献 26
致谢 28
第一章 文 献 综 述
1.1 OPO的构效关系
OPO全称为1,3-二油酸-2-棕榈酸甘油酯,人体从日常饮食中摄取的脂肪酸甘油酯用脂肪酶对其进行处理[1],将OPO上Sn-1以及Sn-3上的脂肪酸通过脂肪酶的水解作用,使其成为游离脂肪酸状态[2][3],最后剩下的单甘脂不宜溶于水,很难能够被人体内部进行吸收和利用[4][5]。淋巴系统将Sn-2位上的单甘脂吸收之后进入体内的血液循环[6]。假若酶水解得到的是游离状态的脂肪酸是棕榈酸(饱和脂肪酸),游离状态下的棕榈酸的熔点实在63摄氏度左右(高于人类正常体内温度37.5摄氏度),进入肠道消化系统之后,棕榈酸会跟人体内部的金属矿物质元素发生皂化反应,进而生成无法被人体吸收和利用的皂化盐,然后随着人体的新陈代谢作用,被排出体外,造成了能量以及物质的浪费。假若能让棕榈酸从游离状态下转变成单甘脂的形式的话,就会容易被人体所吸收利用,并为人体的生命活动提供所需的物质以及能量,所以说棕榈酸分布在三甘酯的位置的不同也会极大程度上的改变它在人体内被吸收利用程度上的大不同[7]。棕榈酸于牛乳脂肪中的含量为26%,其中Sn-1位置上的有占34%,Sn-2位上的占比为32%:而相比于母乳来说,其中棕榈酸的总含量在20%到25%之间,而在Sn-2上的占比达到总棕榈酸的70%。选择母乳为基料的话,将会更加容易被婴幼儿吸收,即吸收的效果更加显著[8]。
很多相关实验结果表明,人体内部在吸收和利用了棕榈酸之后,会对脂肪的吸收和利用产生较大的促进作用,特别是婴儿。在一组对照实验中,添加长链脂肪酸的一组婴儿对于脂肪的吸收利用率明显高于另一组食用短链脂肪酸的婴儿对于脂肪的吸收利用率[7]。而且相关实验表明,不只是棕榈酸,其它人体可吸收的有益于人体健康的脂肪酸分布在二号位上时,都会大大提高其吸收率,但是研究对象多为棕榈酸,而且Sn-2的棕榈酸还可以促进婴儿集体对钙、镁的骨骼物质的吸收率,并能够进一步地促进婴儿集体的新陈代谢,是婴儿保持正常的生长发育以及智力发育,避免佝偻病的一系列因新陈代谢迟缓而引起的病情发生[9]。
1.2 OPO的酶法合成
1.2.1生物催化剂——脂肪酶
在实验中,因为由氨基酸为基本构成单位的脂肪酶的水解特性,所以脂肪酶常在有甘油酯作为反应物参与实验时,被用作为生物催化剂来加入实验中使用,脂肪酶英文名称为LIPASE,学名:甘油水解酶,实验室中常有的脂肪酶有RMIM和TLIM这两种脂肪酶,在适宜的活性条件范围内,脂肪酶会与反应中的甘油脂类的酯键发生水解反应[10],另与该键相连的结合脂肪酸变成游离状态的脂肪酸,并且根据特性和选择性的不同,使用不同类型的脂肪酶,可以针对水解某一特定位置的脂肪酸,而保持其他位置的脂肪酸不被水解,仍以结合状态留在原有甘油酯上。而且脂肪酶还具有高效率性以及较少的副产物和较小污染甚至零污染特性,便于后期产物的提取,以及后续仪器的清洗工作,所以在实验中的使用频率极高[11]。
相关图片展示: