新型CaV2O6超长纳米线的制备,表征及电化学性能毕业论文
2020-04-05 10:44:33
摘 要
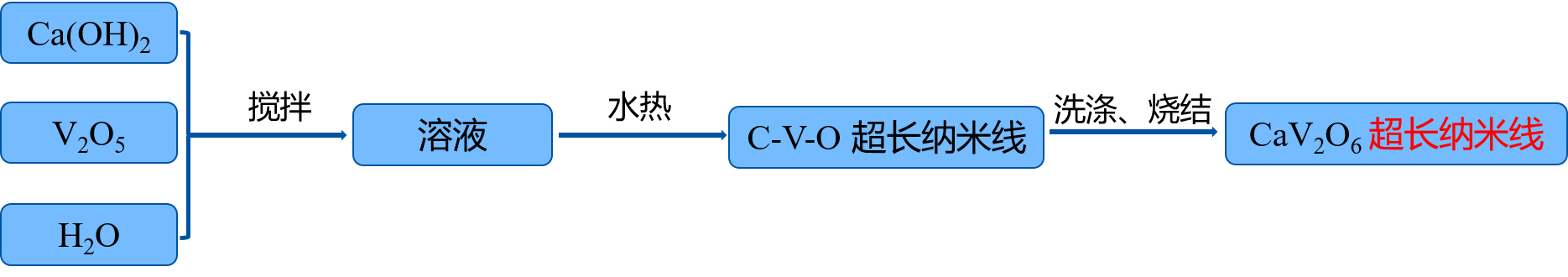
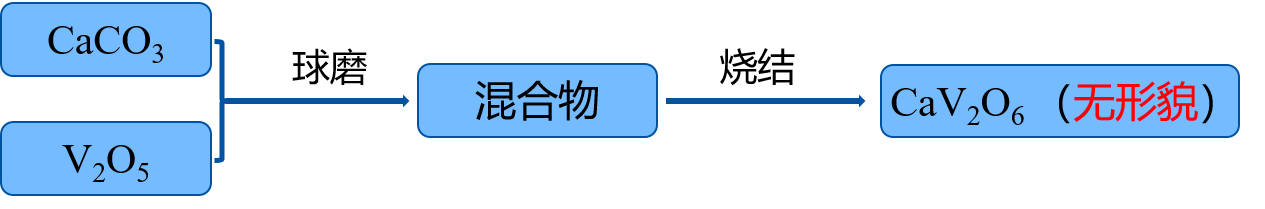
随着能源需求的日益增长,高性能储能器件在各个方面都扮演着越来越重要的角色。研发新型高能量锂离子电池已是当前科研工作者的首要任务之一。钒酸钙材料基于钒的高氧化价态,具有高容量电极材料的研发前景,同时充放电过程中非活性CaO纳米晶粒能缓冲体积变化,提高循环稳定性;而一维纳米材料由于其独特的性质,已被广泛应用于储能领域。结合以上特点,本文采用水热法结合后期烧结制备了一种新型CaV2O6超长纳米线材料,并结合奥斯特瓦尔德熟化和定向连接机制对其形成机理提出了合理假设。同时,本文通过球磨法结合后期烧结制备了无特定形貌的CaV2O6材料,将其作为对比样。本文将两种形貌的CaV2O6材料作为锂离子电池负极,进行电化学性能测试,发现CaV2O6材料作为锂离子电池负极具有良好的充放电循环稳定性,纳米线形貌的CaV2O6材料具有更高的充放电可逆容量。
关键词:钒酸钙;超长纳米线;锂离子电池
Abstract
With the increasing demand for energy, high-performance energy storage devices play more and more important roles in many fields. It is one of the most important tasks for scientific researchers to develop the next-generation lithium ion batteries with a higher energy density. Calcium vanadates have the potential to become the electrode materials with a high capacity, due to the high valence of vanadium. Besides, the generated inactive CaO nanograins during cycling can improve the cycling performance through buffering the volume change of the electrodes. One-dimensional nanomaterials have been extensively studied in energy storage due to the unique properties. Based on the above considerations, we have synthesized novel ultralong CaV2O6 nanowires by hydrothermal method followed by sintering treatment, and proposed the formation mechanism of ultralong CaV2O6 nanowires based on the orientated attachment and Ostwald ripening. We have also synthesized CaV2O6 by a ball milling method as the control sample. The results show that the CaV2O6 materials exhibit an outstanding cycling performance when used as the anode for lithium ion batteries, with the ultralong CaV2O6 nanowires displaying higher capacity.
Key Words: calcium vanadate, nanowires, lithium ion battery
目 录
摘 要 I
Abstract II
第1章 绪论 1
1.1 引言 1
1.2 锂离子电池 1
1.2.1 锂离子电池的结构与工作原理 1
1.2.2 钒基锂离子电池电极材料 5
1.2.3 含钙化合物锂离子电池电极材料 5
1.3 一维纳米电化学储能材料 6
1.3.1 一维纳米电化学储能材料概述 6
1.3.2 一维纳米电化学储能材料的特点 7
1.3.3 一维纳米材料的合成方法 8
1.4 本论文的选题意义及主要研究内容 8
第2章 实验原料,仪器及表征测试方法 10
2.1 实验原料 10
2.2 实验仪器 10
2.3 表征测试方法 11
2.3.1 材料表征方法 11
2.3.2 材料电化学性能测试方法 11
第3章 CaV2O6超长纳米线及其对比样的制备 13
3.1 引言 13
3.2 水热法制备CaV2O6超长纳米线 13
3.2.1 合成方案 13
3.2.2 合成方案的调控 14
3.2.3 水热法制备的优势与不足 14
3.3 球磨烧结法制备CaV2O6对比样 15
3.3.1 合成方案 15
3.3.2 球磨烧结法的优势与不足 15
第4章 CaV2O6超长纳米线及其对比样的结构与形貌分析 16
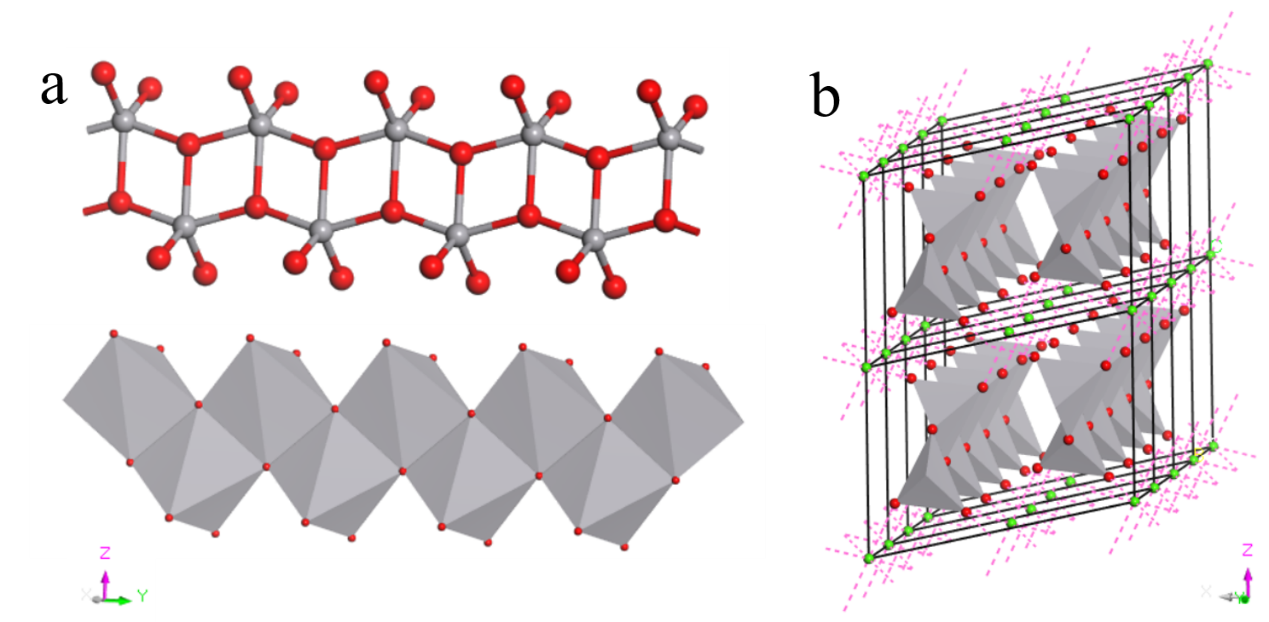
4.1 CaV2O6晶体结构 16
4.2 CaV2O6超长纳米线的结构与形貌 16
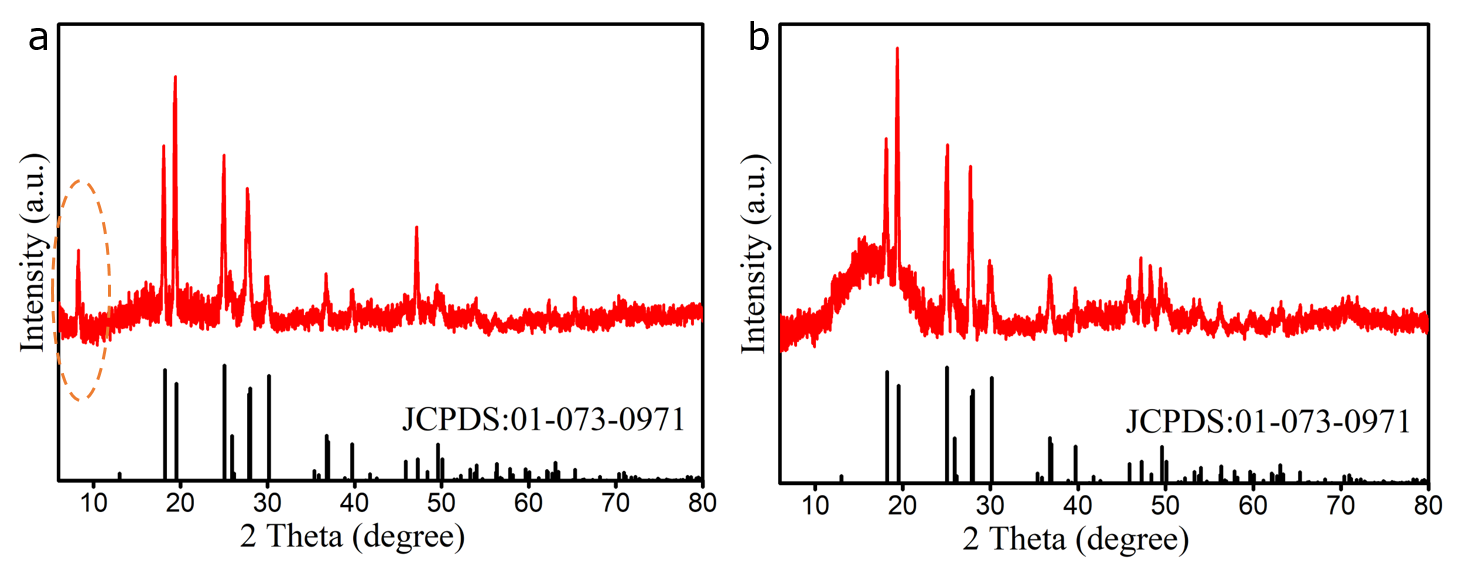
4.2.1 XRD分析 16
4.2.2 SEM分析 17
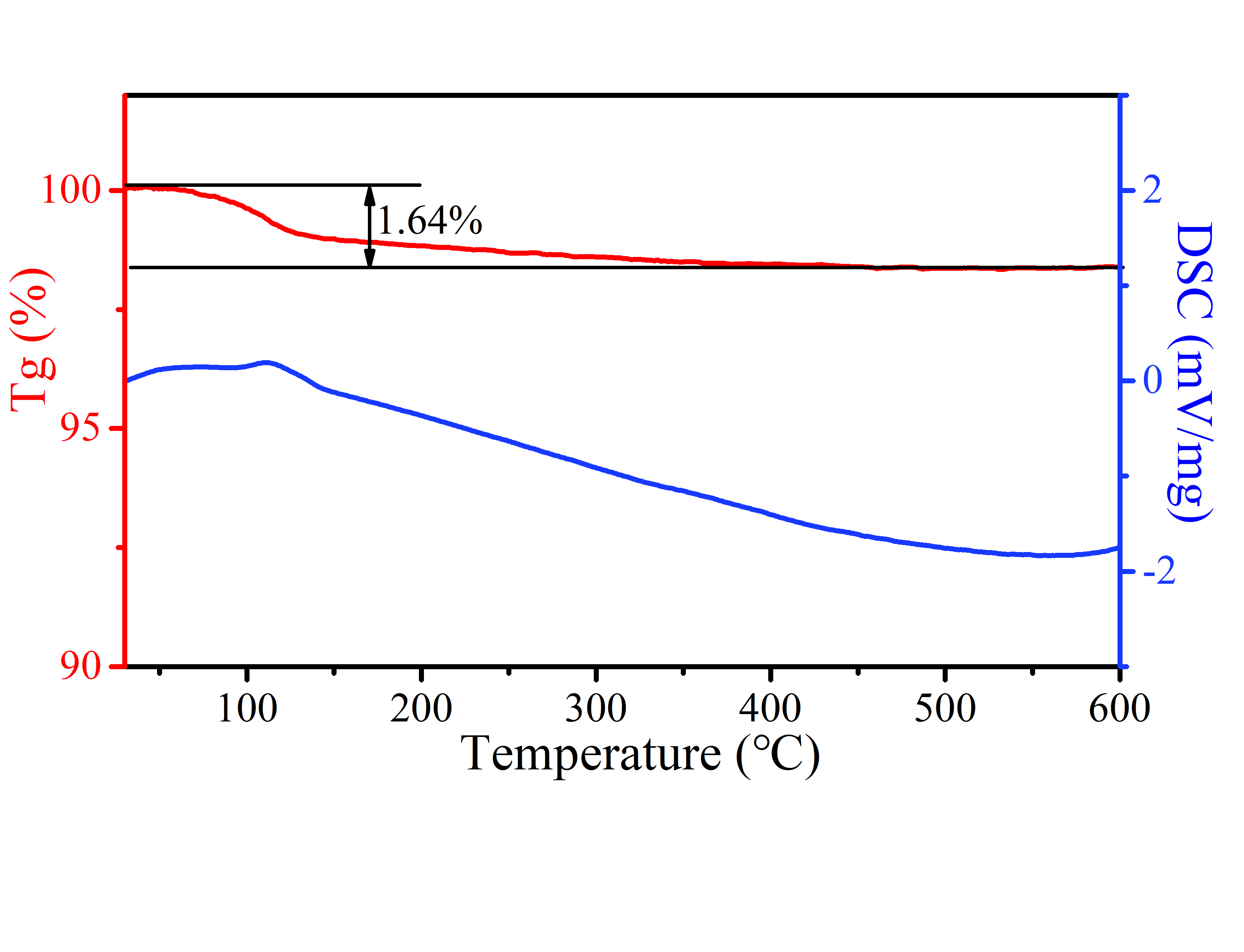
4.2.3 热重分析 18
4.2.4 微观形貌形成机理分析 19
4.3 CaV2O6对比样的结构与形貌 20
第五章 电化学性能测试与研究 21
5.1 锂离子电池循环性能 21
5.2 锂离子电池倍率性能 21
5.3 其它电化学测试 22
第6章 结论与展望 23
6.1 结论 23
6.2 展望 23
致 谢 28
第1章 绪论
1.1 引言
19世纪后期第二次工业革命的爆发带领人们步入了“电气时代”,以煤气和汽油为燃料的内燃机的发明解决了交通运输工具中发动机的问题,人类社会对能源的需求也日益增加。然而,有限的化石能源日益枯竭,同时化石燃料燃烧会产生大量温室气体,造成全球变暖,严重威胁自然生态环境间的平衡。因此,寻找一种可替代传统化石能源的绿色能源,是当前科研工作者面临的巨大挑战。太阳能,地热能,潮汐能,风能都是存在于自然界中的可再生能源,但其能量的提供具有间歇性,只有将其有效地存储收集才能更好地为人类所利用[1,2]。大自然提供的绿色能源有望缓解人类能源紧缺的问题,但能否将其有效利用很大程度上取决于能源存储与转换的技术。
将从自然中获得的可再生能源转化为化学能进行高效存储,是一种可靠的能源存储方式。比如燃料电池系统,燃料电池又称电化学发电机,通过电化学反应将燃料的化学能中的吉布斯自由能部分转化为电能,因为不受卡诺循环效应的限制,所以比传统的热机做工更为高效。燃料电池的气体排放取决于所使用的燃料的种类,比如氢燃料电池反应产物是H2O,气态的水虽然是温室气体,但当大气中的水蒸气达到饱和,水蒸气会液化为雨。因此,产生H2O的燃料电池并不会恶化全球气候变暖的问题。然而,现在还没有一种可靠且廉价的方法去获取氢燃料电池的原料H2,在找到一种合适的H2制备方法前燃料电池难以得到大规模应用[3]。
相比之下,锂离子电池作为一种能源存储器件在大多数情况下更为实用。相比与传统的铅酸电池,镍镉电池,锂离子电池具有更高的能量密度[4],广泛应用于手机,手提电脑,数码相机,平板电脑等便携设备中,大大促进了互联网时代的“无线革命”[5~7]。但是目前,随着电动汽车和混合动力汽车的发展,锂离子电池的能量密度需要进一步地提升[8,9],而高性能电极材料的开发是提高锂离子电池能量密度的关键突破口之一。
1.2 锂离子电池
锂离子电池通常由正极材料,负极材料,隔膜和电解液组成,本节主要介绍锂离子电池的结构与工作原理,以及钒基材料和含钙化合物作为锂离子电极材料的应用。
1.2.1 锂离子电池的结构与工作原理
锂离子电池的正极材料和负极材料在锂离子电池充电和放电的过程中分别可逆地嵌入和脱出锂离子,正极材料和负极材料通过隔膜隔开,浸润在液态电解液中。另外还有全固态电解质,凝胶态电解质,本文中的讨论都是基于液态电解质。充电时,锂离子从正极材料中脱出,在电解液中迁移,穿过隔膜嵌入负极材料;放电时,锂离子从负极材料中脱出,以同样的方式嵌入正极材料。1980年,Armand等提出了摇椅式电池的概念[10]。在充放电过程中,锂离子电池就像一把摇椅,摇椅的两端是正极材料和负极材料,而锂离子就像运动员一样在之间来回奔跑,所以锂离子电池又称为摇椅式电池。
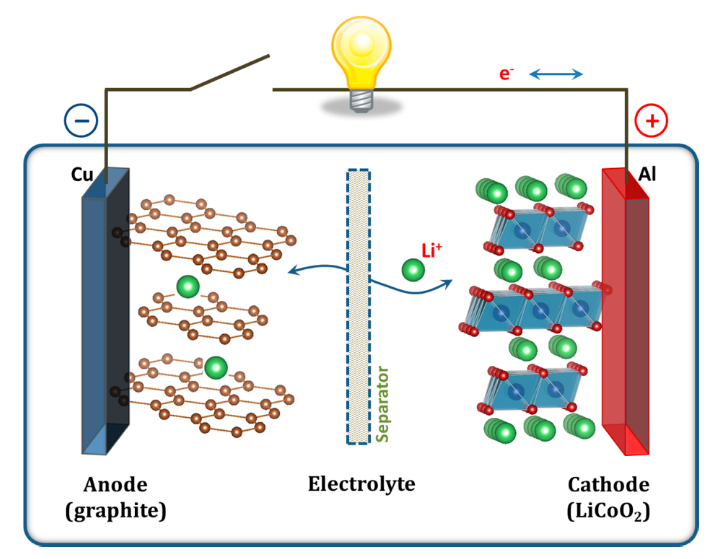
图1.1 锂离子电池原理示意图[11]
Goodenough等分别于1981年和1997年提出的层状LiCoO2材料[12],和 LiFePO4 材料[13],以及Thackeray发现的LiMn2O4尖晶石正极材料[14]是较为典型的锂离子电池正极材料,并且均已得到商业化应用。正极材料在锂离子全电池中首先要起到锂源的作用,提供充放电过程中往返于正极和负极材料之间的锂离子,以及首次充放电过程中形成SEI膜消耗的锂离子。其次,正极材料需要具有较高的电极电位,以保证全电池高的输出电压。优秀的电极材料除了安全性好,环境友好外,还应具有(1)高的能量密度:电极材料能量密度越高,同等情况下锂离子电池输出的能量越高;(2)高的锂离子化学扩散系数:使电池适用于更高的充放电倍率;(3)稳定的结构:充放电过程中保持结构的稳定,使锂离子电池具有更好的循环性能。
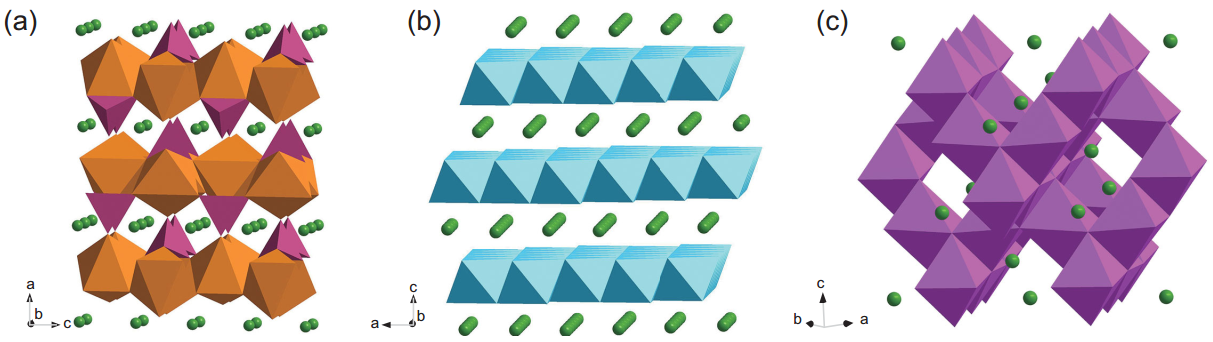
图1.2 典型锂离子电池正极材料结构示意图,从左到右依次是(a)橄榄石结构的LiFePO4,锂为绿色,FeO6多面体为棕色,PO4多面体为紫色(b)层状结构的LiCoO2,CoO6多面体为蓝色(c)尖晶石结构的LiMn2O4,MnO6多面体为洋红色[15]
与正极材料一样,负极材料的优劣对锂离子电池也有至关重要的影响。1983年,法国INPG 实验室[16]在电化学电池中实现了锂离子在石墨负极中的可逆脱嵌。石墨具有层状结构,作为锂离子电池负极材料具有优秀的电化学性能,而且成本也不高,是应用最广泛的商业化锂离子电池负极材料之一[17,18]。同正极材料一样,优秀的负极材料应具备安全性好,环境友好,能量密度高(可逆容量大),高的锂离子化学扩散系数,充放电过程中结构稳定等特点,另外为了和具有较高电极电位的正极材料配对,锂离子电池负极材料脱嵌锂反应应具有低的氧化还原电位,这样以此组装的全电池才能能量最大化。
锂离子电池电解液一般是由电解质锂盐和非水有机溶剂两部分组成。电解质锂盐在有机溶剂中应具有较高的溶解度和电导率,并且与有机溶剂,电极材料等之间不发生不利于电池工作的副反应。六氟磷酸锂(LiPF6 )是目前锂离子电池中应用最为广泛的锂盐,而溶剂通常使用多种有机溶剂按一定比例配比而成的混合溶剂,因为单一的溶剂很难满足电解液的各项性能要求。醚类,脂类,碳酸烷基酯,腈类都可作为溶剂[19]。
锂离子电池中隔膜的关键作用是将正极材料和负极材料分隔开,同时又能让锂离子自由通过,所以隔膜应同时具备电子绝缘性,高的离子电导率,保证正负极的机械隔阂与锂离子的通透性同时具备。其次,隔膜材料应有足够的电化学稳定性,能耐电解液腐蚀。在机械性能上,隔膜应具有足够的穿刺强度和拉伸强度,并且尽可能薄。实验室中,使用最为广泛的是使用具有高强度的聚烯烃多孔膜。

图1.3 聚烯烃多孔锂离子电池隔膜实物图
除了正极材料,负极材料,隔膜,电解液这四大组成部分外,正负极材料所依附的集流体也是锂离子电池重要组成部分之一。铜箔具有导电性好,价格便宜,质地软等特点,是作为集流体的首选材料,但铜箔在高电位下容易被氧化,因此通常只将铜箔作为负极集流体,而具有高氧化电位的铝箔则是正极集流体的最佳选择。

图1.4 正极(铝箔),负极(铜箔)集流体材料实物图
1991年,日本SONY公司的研究人员以LiCoO2作为正极材料,石油焦作负极材料,LiPF6溶于丙烯碳酸酯和乙烯碳酸酯作电解液,开始商业化生产二次锂离子电池,这种锂离子电池具有超过3.6 V 的电压,能量密度120—150 Wh kg-1 。近几十年来,锂离子电池产业迅速发展,主要应用于各种便携设备的电源提供,同时还涉及二次能源发电储能[20]。但是随着社会发展,人类对能源的需求越来越大,研发具有更好性能,更强适用性,更经济的新型电池是当前科研人员面临的首要挑战之一[21]。
1.2.2 钒基锂离子电池电极材料
钒基材料作为电极材料已有30多年的研究历史,并得到广泛应用[22~26]。锂离子电池通过充放电过程中的物质传输和电子转移实现化学能和电能之间的转换,在能量转换的过程中,伴随着电极材料化合价和结构的变化。电池的能量存储由电池电压和正负极材料的容量决定,而高价态的电极材料在充放电过程中可以实现多电子转移,通常是制备高容量电极材料的突破口。比如钒,铬,铌,钼,等元素,在氧化还原反应中,高的氧化态可以实现多个锂的嵌入脱出。但是钨,铌等元素虽然具有高价的氧化态,其元素本身的相对分子质量较大,所以用做制备高质量比容量的材料并不具备优势。电极材料的结构稳定性对电池的长循环性能有直接影响,许多基于传统转换反应的电极材料(比如SnO2 和 Fe2O3),虽然具有高的比容量,但是能量转换过程中电极材料的体积变化较大,导致其结构易崩溃瓦解,作为电极材料长循环稳定性差。而钒与氧之间能形成相互作用力强的V—O键,所以钒基材料在还原反应过程中通常不会形成0价的金属钒,保证其不会有过大的体积变化[27]。
电极材料资源的丰富度也是考量其应用潜质的关键因素之一。根据美国地质调查局的统计,截止2015年年底,全球钒储量超过1500万吨,未开采的钒资源量超过6300万吨。中国、俄罗斯、芬兰、南非等国是钒资源的主要分布国,其中钒资源最丰富的3个国家俄罗斯,南非,中国的钒资源储量就占全球钒资源储量的三分之一以上[28]。由此可见,钒基材料不仅在科研方面具备极大的发展潜质,钒基材料的研发也与我国的自然资源优势相符合。
1.2.3 含钙化合物锂离子电池电极材料
Reddy等[29]总结锂离子电池的反应机制主要有三种:(1)嵌入—脱出反应。过渡金属氧化物等具有二维层状结构或者三维网状结构的化合物可以可逆地嵌入和脱出锂离子,并且锂离子的脱嵌过程不会破坏晶体结构。(2)合金化-脱合金化反应。能够和锂金属形成合金的非金属元素单质或者金属会发生这种反应。比如单质硅,金属锌,金属铟,金属铋。合金化-脱合金化反应通常在低电位下发生。(3)转换反应(氧化还原反应)。电极材料在合适的电位下和锂发生氧化还原反应,氧化物,氟化物,氟氧化物,硫化物,氮化物,磷化物等电极材料通常基于转换反应机制。
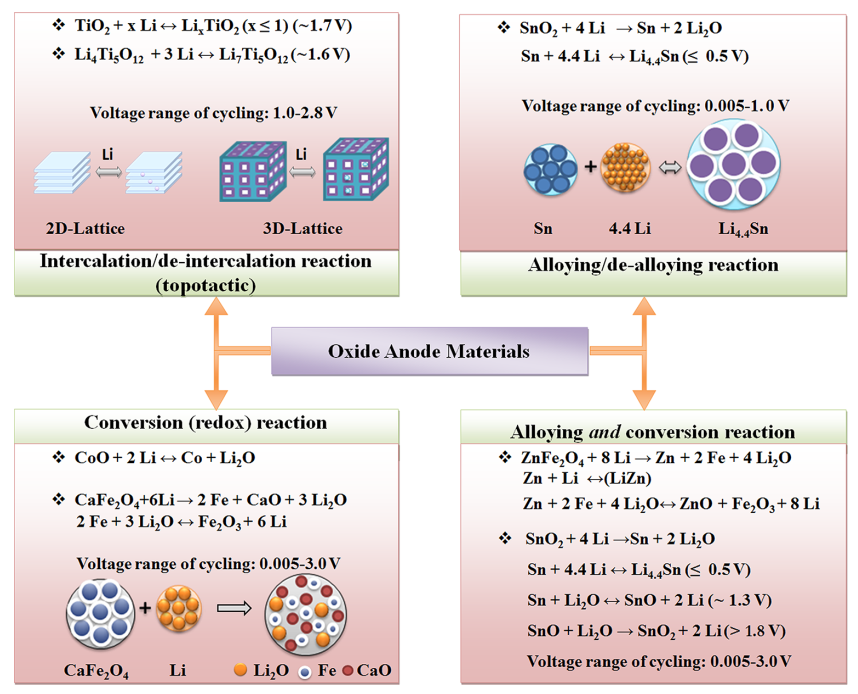
图1.5 锂离子电池反应机制示意图[28]
基于转换反应机制的电极材料,在充放电过程中发生氧化还原反应,更多的电子转移能够使电极材料具有更高的比容量。但通常基于这类机制的材料反应过程中体积变化较大,电极材料的结构稳定性较差,导致电池的长循环性能较差。倘若在电极材料中引入不具电化学活性的佐料,可起到稳定电极材料结构的作用。比如图1.5中的CaFe2O4,由于金属钙和氧之间作用力强大的化学键,首次充放电过程中所形成的CaO纳米晶粒在充放电反应中表现出非活性,可以对电极材料的体积变化起到有效的缓冲作用,同时还能抑制Fe2O3的团聚,相比于单一的Fe2O3电极材料,其循环性能得到极大的提升。类似的还有Kim等工作中的Ca—Co—O化合物[30],Li等工作中的Ca—Sn—O化合物[31], Ca在首次充放电过程中形成不具电化学活性的CaO纳米晶粒,在“旁观者效应”的作用下对电极材料的结构变化起到缓冲作用,从而提高电池的长循环稳定性。
1.3 一维纳米电化学储能材料
1.3.1 一维纳米电化学储能材料概述
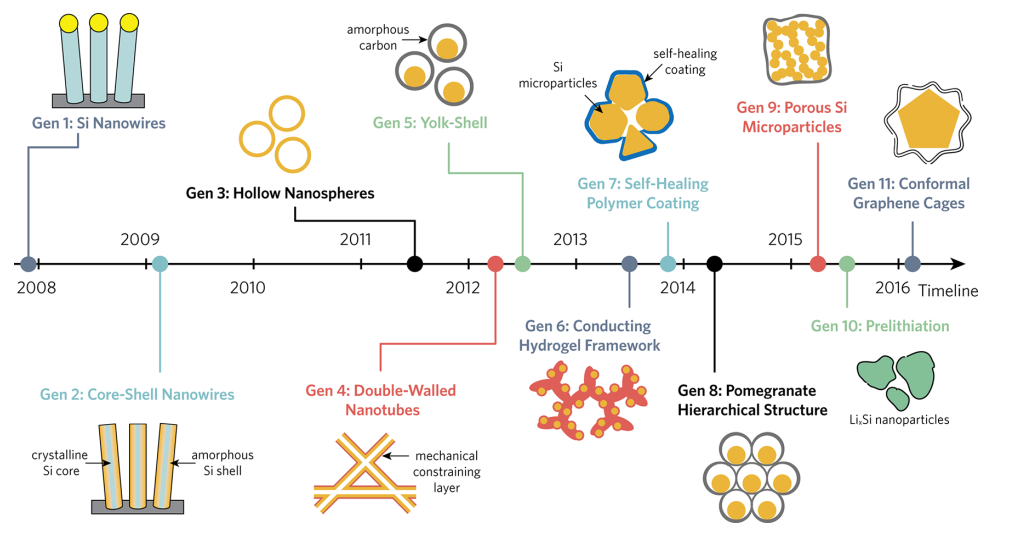
纳米技术在电极材料的研究有诸多优势:首先,纳米技术通过降低电极材料的体积,使材料有更大的比表面积,从而在材料表面获得更多的电化学活性位点,同时更大的比表面积也能降低反应过程中电子/离子的传输路径;其次,纳米技术还提供了一种构造包覆结构以及功能化层状结构的方法,有效的降低副反应对电极材料中活性组分的影响;最后,纳米技术使电极材料的设计更具灵活性,可针对每一个单一组分进行设计,使电极材料具备传统制备方法难以实现的功能特点。Yi Cui等在硅电极的研发过程中,充分应用了纳米技术的各项优势,设计多种性能优异的硅电极材料[32]。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: