环糊精主客体作用调控壳聚糖胶囊释药行为毕业论文
2020-04-06 13:11:04
摘 要
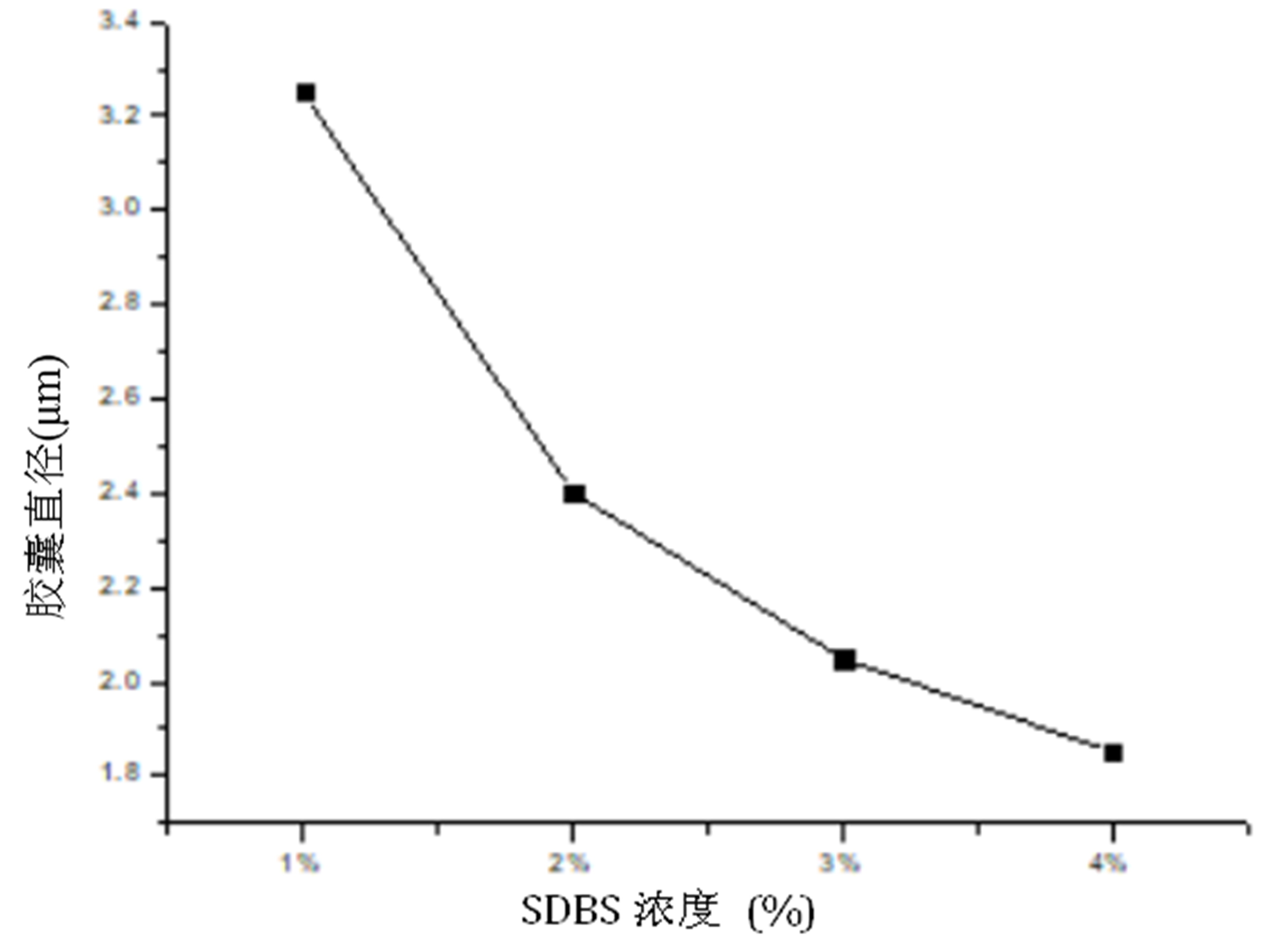
本文通过阳离子聚电解质壳聚糖与阴离子表面活性剂的静电作用制备包覆环糊精的壳聚糖胶囊。采用三维显微镜探索不同浓度的十二烷基苯磺酸钠(SDBS)作为接收液,对于壳聚糖胶囊形态的影响。随着SDBS的浓度增加,生成的胶囊尺寸呈现减小趋势。采用SEM研究环糊精对壳聚糖胶囊表面形貌的影响,并分析了环糊精对微胶囊囊壁的作用机理。结果表明,由于环糊精与十二烷基硫酸钠之间存在主客体包络作用,环糊精对壳聚糖胶囊具有破坏作用,使胶囊表面结构和形态发生变化,从而实现对壳聚糖胶囊释药行为的可控性。
以水杨酸钠为模型药物,研究了环糊精对胶囊释药性为的影响。研究结果表明,环糊精浓度越高,酸度越高,越能够促进胶囊的药物释放。相比于β-环糊精,α-环糊精可以提高胶囊的药物释放速率。这说明环糊精能够通过主客体相互作用来调控壳聚糖胶囊的药物释放行为,所得结果对于壳聚糖微胶囊的药物控释具有重要的理论意义。
关键词 :壳聚糖 胶囊 环糊精 主客体作用 药物释放
Abstract
In this paper, chitosan capsules encapsulated with cyclodextrin were prepared by electrostatic action of cationic polyelectrolyte chitosan and anionic surfactant. A three-dimensional microscope was used to explore the effect of 12 alkyl benzene sulfonate (SDBS) with different concentrations on the morphology of chitosan capsules as receiving solution. With the increase of the concentration of SDBS, the size of chitosan capsules showed a decreasing trend. The effects of different conditions on the surface morphology of capsules were studied by SEM and three-dimensional microscope, and the effect of cyclodextrin on the release of capsule was investigated, and the mechanism of cyclodextrin on microcapsule wall was analyzed. In order to realize the controllability of the drug release of chitosan capsules, drug-loaded chitosan capsule containing sodium salicylate was prepared by the electrostatic interaction of 12 alkyl sodium sulfate with sodium salicylate as a model. The effect of cyclodextrin on the release performance of microcapsules was studied in detail by using cyclodextrin to control the release of capsules. The effect of cyclodextrin on the release of chitosan microcapsules was analyzed by UV-vis spectrophotometer test, the drug concentrations of different chitosan capsules prepared under different conditions were tested and the drug release curves were made.
The results showed that the higher the concentration of cyclodextrin, the higher the acidity, the better the drug release of microcapsules could be promoted. Compared with beta-cyclodextrin, α-cyclodextrin can improve the drug release rate of microcapsules. This shows that cyclodextrin can regulate the drug release behavior of chitosan microcapsules through the interaction of host and object, and the results are of great theoretical significance for drug release of chitosan microcapsules.
Key Words:chitosan capsule, cyclodextrin, main object, drug release
目录
摘 要 I
Abstract II
第1章 绪论 1
1.1甲壳素简介 1
1.2壳聚糖简介 1
1.3胶囊以及壳聚糖胶囊 3
1.4环糊精研究简介 4
1.4.1环糊精研究进展 4
1.4.2 α-/β-环糊精的结构和性质 4
1.4.3 环糊精应用 5
1.5本实验研究目的、意义和内容 5
第二章 实验部分 7
2.1 实验试剂及设备 7
2.2 实验内容 7
2.2.1原料的准备 7
2.2.2壳聚糖胶囊的制备 9
2.2.3 胶囊的尺寸与形态表征 9
2.2.4研究环糊精对胶囊表面形貌的影响 10
2.2.5 研究环糊精对胶囊药物释放的影响 10
2.3产物的表征 11
2.3.1 三维显微镜 11
2.3.2 SEM测试 11
2.3.3 紫外-可见吸收光谱 11
第三章 结果与讨论 12
3.1胶囊的制备与形态 12
3.1.1胶囊的制备 12
3.1.2胶囊的形态 13
3.2各组分对胶囊形态的影响 14
3.2.1环糊精种类的影响 14
3.2.2环糊精含量的影响 14
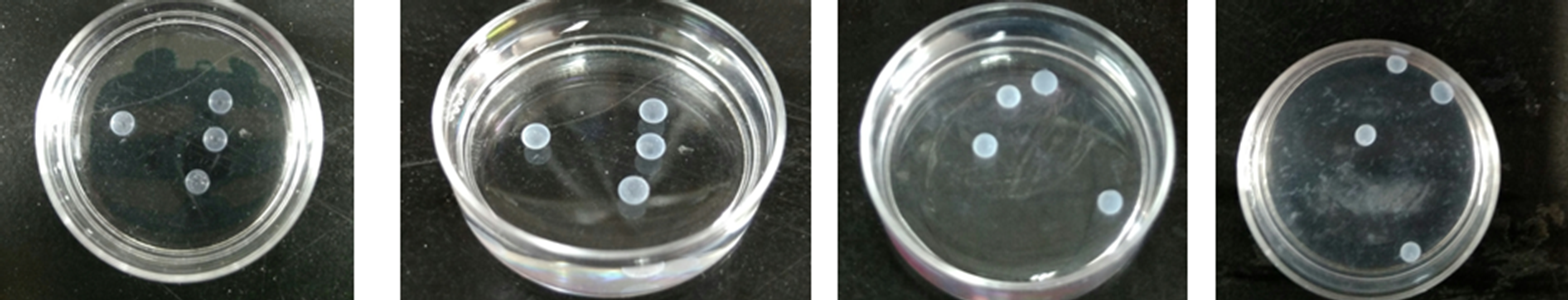
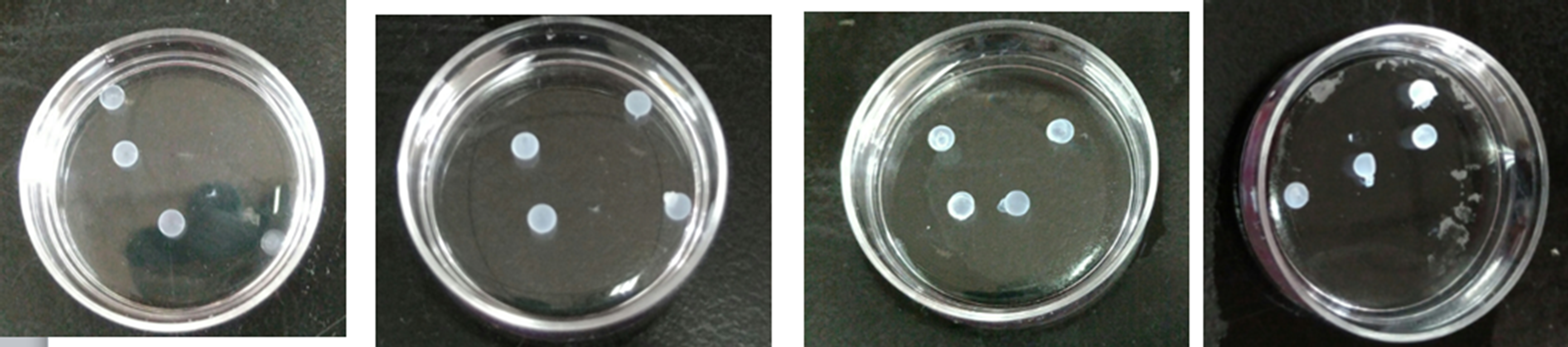
3.2.3接受液种类的影响 15
3.3 胶囊的破坏机理 16
3.4胶囊的染料释放性能 17
3.4.1环糊精的影响 17
3.4.2接收液的影响 17
3.5 胶囊的药物释放性能 17
3.5.1水杨酸钠标准曲线的绘制 17
3.5.2 环糊精种类的影响 18
3.5.3 环糊精用量的影响 19
3.5.4 醋酸浓度的影响 20
第四章 结论 21
参考文献 22
致 谢 24
第1章 绪论
1.1甲壳素简介
甲壳素(Chitin),又被称为甲壳质、壳多糖、几丁、几丁质、蟹壳素或明角壳蛋白。甲壳素是自然世界中唯一带正电荷的多糖,是一种可食用动物纤维,其与植物纤维的多碳聚合物相似;作为一种高含氮量的天然高聚物,壳聚糖含氮量仅次于蛋白质;作为一种生物资源,其产量排在纤维素之后,是自然界中的第二大可再生天然生物高分子材料,科学界将其誉为在糖、蛋白质、脂肪、维生素、矿物质(无机盐)之后人体必须的第六生命要素。甲壳素存在于甲壳动物外壳、腔肠动物、软体动物、节枝动物、环节动物、原生动物、海藻、 真菌以及动物骨肉与骨结合处,动物关节、足以及蹄等坚硬部分 [1]。
图1.1给出了甲壳素的分子结构式图,聚N-乙酰脱氧葡萄糖胺-β(1,4)是甲壳素的化学式,甲壳素是一种线性双螺旋结构聚合物,类似于纤维素结构的一种六碳糖的聚合物,乙酰葡萄糖胺是其分子基本组成单元,从图1.1可以看出,m链节占整了个分子链的绝大部分 [1]。。
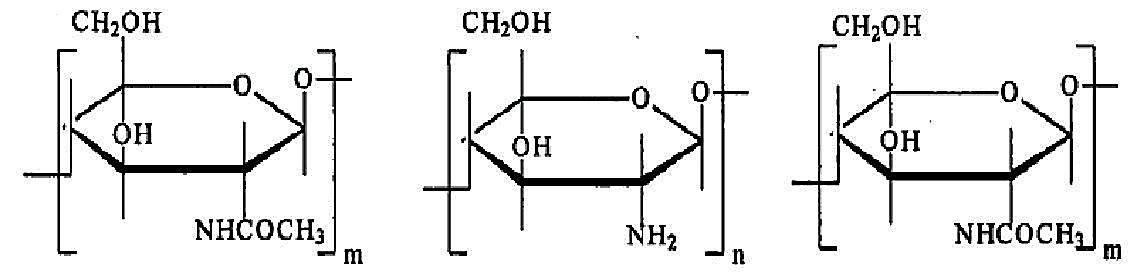
图1.1 甲壳素的化学结构图
甲壳素包括它的衍生物生物相容性良好、抑菌性强、能促进伤口愈合,广泛用于伤口包覆、药物缓释、重金属吸附生物医用组织植入以及生物分离等高附加值领域[3]。但甲壳素富含氢键且具有较高的结晶度,导致其难溶不熔、加工有一定困难等难题,必须进行改性,目前常常借助削弱氢键的方法来改性,如接枝、酰化、烷基化、醚化以及无机酸酯化等[4-6]。
我们国家多面临海,拥有丰富的海洋资源,这就意味着可以从大量的鱼虾蟹等动物上提取出甲壳素,如果能够充分利用这些能源,有利于能源可持续发展。
1.2壳聚糖简介
壳聚糖(Chitosan简写为CS)为从虾蟹等外壳中提取的甲壳素,将虾或蟹壳在常温下用稀盐酸脱钙,再用碱溶液除去蛋白质,高温碱水解脱乙酰而得到(壳聚糖的来源如图1.2所示),由于聚糖可以由甲壳素脱乙酰基得到,是甲壳素脱乙酰度达到70%以上的产物,故又被称为脱乙酰甲壳素,脱乙酰后得到的壳聚糖,在生物活性,物理化学性能等方面表现优于甲壳素。
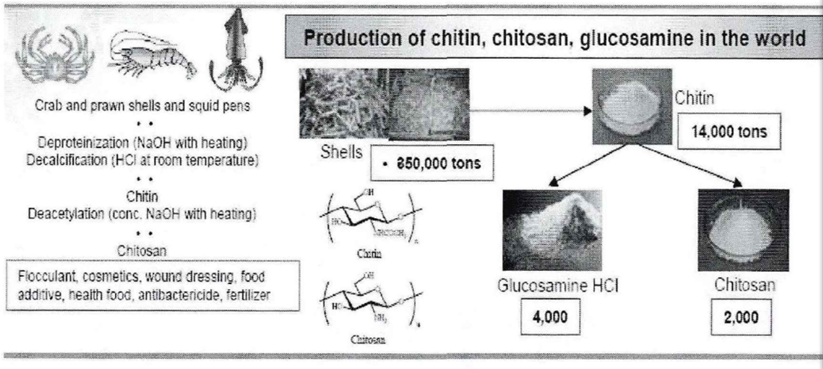
图1.2壳聚糖的来源
壳聚糖的化学名称为聚葡萄糖胺-β(1,4)-2-氨基-D-脱氧葡萄糖,分子结构式如图1.3所示。由于壳聚糖是由甲壳素脱乙酰化得来,它和甲壳素结构相似[7] ,n链节占了整个分子式的绝大部分。
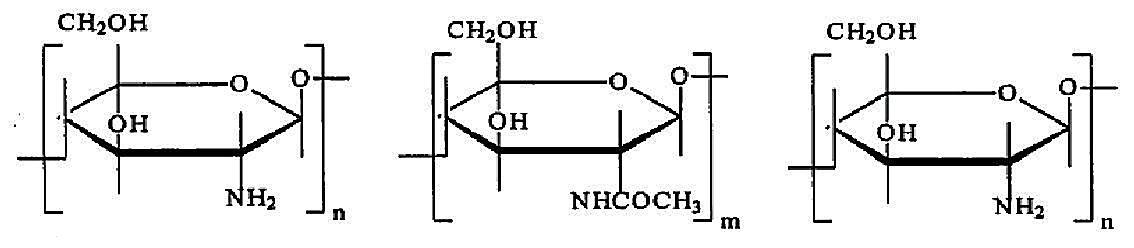
图1.3 壳聚糖的化学结构图
壳聚糖的性状为白色无定形透明,实验室所用的壳聚糖为粉末状,类似于淀粉。甲壳素溶解性能不太好,不同于具有有序结构的甲壳素导致甲壳素难溶解于一般溶剂,壳聚糖具有游离氨基,溶解性有所提升,虽然它不溶于强酸、碱液以及水溶液,在中性水溶液中只能形成膨润状态,但可溶于多数有机酸和大多数稀酸中,例如稀盐酸稀醋酸等。其吸附、吸湿,通透、成膜性能良好,具有较好的生物相容性能,环境友好型材料,具有广泛的应用面,从上世纪70年代以来,人们一直在深入对壳聚糖的研究,并获得“人体第六生命要素”称号,其重要性不言而喻。
壳聚糖的应用面非常广,包括在纺织上的应用:织物上浆剂、印染助剂、织物功能整理、处理印染废水;在医药卫生中的应用:可吸收手术缝合线、医用敷料、医用胶囊、人工皮肤;在食品中的应用:抗菌剂、果蔬保鲜剂、果汁澄清剂、保健食品添加剂;在化妆品中的应用:护发用品、护肤用品、其他洗涤用品。本文主要研究对象就是壳聚糖应用的一种:壳聚糖胶囊[8]。
1.3胶囊以及壳聚糖胶囊
胶囊是一种以天然或者合成的高分子为原料制备的具有聚合物壁壳的球形小囊,其中被包裹的物质称为芯材,包裹芯材的物质称为壁材。
胶囊制备的过程中,壁材的选择对微胶囊的性质至关重要,同时这也是获得高微胶囊化效率、性能优越的微胶囊产品的重要前提条件之一。对于壁材的选择,要遵循以下基本条件:首先要能与芯材不发生化学反应;然后作为微胶囊的壁材要有一定的强度和稳定性;此外,壁材还应价格合理,且来源广泛,容易制备[9]。从本实验采用的壁材是壳聚糖。正如前文介绍的,壳聚糖取材于天然物质,节能环保,是一种优秀的环保可持续发展型胶囊壁材。常用的壁材按照水溶性和水不溶性可分为两大类两大类; 从来源上来分类,可以分为无机材料壁材,天然高分子壁材[10],天然高分子改性材料和合成高分子壁材[11]。
制备胶囊的方法一般有三种:化学法,物理法和机械法。物理化学法包括相分离法和干燥浴法;机械法包括法空气悬浮法、喷雾干燥[12]。等三大类,化学法可分为凝聚法,收缩法和界面聚合法。在此实验中,复合凝聚法用于指在不同pH值下两种聚合物的电荷变化。也就是说,由于不均匀的电荷,带正电的胶体溶液与另一带负电的胶体溶液混合。混合液之间通过相互作用生成沉淀,助力制备胶囊。制备胶囊应用最广的方法为凝聚法、界面聚合法、原位聚合法。
1.4环糊精研究简介
1.4.1环糊精研究进展
1891年Villier首先发现了环糊精[13],其发展经历了三个阶段。在第一阶段,威利尔从淀粉消化淀粉直链淀粉溶液中提取重结晶材料并命名为“木粉”(cellulosine)[14],但其结构直到12年后才由Schardinger确定,他通过分离获得两种结晶化合物,并与碘-碘化钾反应,得到一种蓝色晶体的环糊精命名为α-环糊精,得到红棕色晶体的环糊精命名为β-环糊精[15]。像这样判断α-/β-环糊精的方法今天仍在使用。
第二阶段是从20世纪30年代中期到20世纪60年代末。在这个阶段,科德宝首先分离纯环糊精,并提出环糊精是一种仅与葡萄糖分子结合的环状分子,仅含有α-1,4配糖键。,他还与Cramer发现了γ-环糊精并明确了它的结构[16,17]。在此期间,法国和克莱默分离并表征了环糊精的物理化学性质,并指出环糊精和其他有机分子可能具有较大的包裹体[18,19]。此期间的研究使人们认识到环糊精可用于工业,但由于环糊精毒性的争议,阻碍了其在食品和医药领域的发展。
在法定资格单位给出环糊精毒理学研究成果后,人们不再怀疑它的毒性。环糊精化学的研究进入了20世纪70年代初的高峰,环糊精研究的相关论文数量逐年增加。Szejtli于1971年创立化学研究实验室,并在医药,食品,化妆品和分析化学领域进行环糊精研究。Szejtli也被国际同事称赞为“环糊精之父”[20]。
1.4.2 α-/β-环糊精的结构和性质
环糊精(Cyclodextfin,CD),是衍生自淀粉的环状低聚糖,其通过α-1,4-环糊精通过α-D-吡喃葡萄糖基单元,形成糖苷键,其中α-,β-,γ-,δ-和ε-环糊精分别由6,7,8,9个α-葡萄糖结构单元组成。本实验采用的是常见的环糊精α-环糊精,β-环糊精。环糊精可溶于水,但不溶于大多数有机溶剂,只能溶于某些极性惰性溶剂,如二甲基亚砜,二甲基甲酰胺等[21]。在室温下,β-环糊精在水中的溶解度仅为0.0163 mol/L,而α-环糊精的溶解度高达0.1211 mol/L[22]。环糊精的溶解度随温度升高增加。在α-环糊精中,由于其中一个吡喃葡萄糖单元处于扭曲状态,分子内氢键是不完全的,6个可能形成的氢键只有4个形成,因此大环结构处于扭曲状态[23]。由于β-环糊精中的一个吡喃葡萄糖单元的C2-羟基可以与相邻的吡喃葡萄糖单元的C3羟基形成氢键,环糊精分子中的这些氢键形成完整的环,完整的氢键带使其成为刚性结构,因此β-环糊精水溶性非常低[24]。环糊精是稳定的,可以储存多年而不会变质,在碱性条件下相对稳定,在强碱下水解。它们对酸不稳定并且经常在酸性条件下发生水解反应以形成线性单糖。开环水解的速率与环糊精的空腔大小有关,随着空腔尺寸的增加而增加,即β-环糊精gt;α-环糊精,但弱有机酸不易水解环糊精[25]。
因为吡喃葡萄糖结构单元的椅子构型相对稳定,所以环糊精分子具有截头圆锥形状而不是完整的圆柱形[26]。天然的α-,β-环糊精,特别是β-环糊精具有有限的水溶性,因此它们与亲脂性物质的包合配合物也难溶于水,通常作为固体环糊精形式从水溶液中沉淀出来[27]。
图1.4显示了β-环糊精的结构图和立体结构图。在腔内部,排列了糖和氧的桥原子以及醚结构,并且氧原子的非键合电子指向环糊精腔内部,使得空穴具有非常高的电子密度,显示出一些路易斯碱性质[15]。
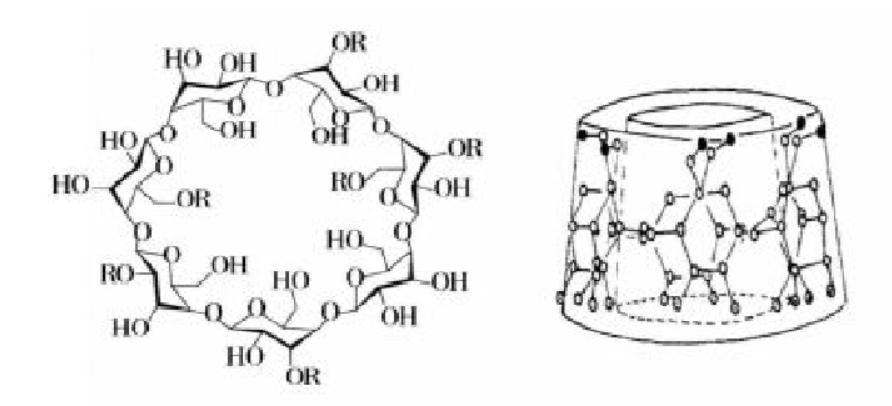
图1.4 β-环糊精环状构型图与立体结构图
1.4.3 环糊精应用
环糊精具有生物无毒性,生物可降解性的特点,这使其在食品,化妆品,医药等领域得到广泛应用。
1.5本实验研究目的、意义和内容
将环糊精溶解在壳聚糖溶液中,用滴管吸取一定量的壳聚糖盐酸溶液滴加到阴离子电解质溶液中,由于正负电荷的静电作用,在壳聚糖液滴的外表面会形成由壳聚糖和阴离子电解质(如十二烷基苯磺酸钠)组成的较为坚硬的外壳。环糊精能够与十二烷基苯磺酸钠等发生作用,从而破坏原有的壳聚糖与十二烷基苯磺酸钠的相互作用,导致胶囊遭到破坏。我们将探讨壳聚糖胶囊与不同电解质形成胶囊的最优实验室制备条件,通过对比胶囊对于制备胶囊时加入环糊精的响应,以及胶囊被破坏前后的SEM和显微镜照片,分析环糊精破坏胶囊的机理。同时,讨论在不同条件下,环糊精对胶囊的破坏情况,比如不同pH值,不同温度,不同种类的环糊精等,并尝试根据实验现象分析环糊精对胶囊释药行为的影响、包载物的释放情况,染料甲基蓝为模型被封装在胶囊内部,研究了胶囊在不同环境条件的刺激下的释放行为。
第二章 实验部分
2.1 实验试剂及设备
实验中所用到的主要试剂和材料见表2.1
表2.1 实验主要试剂、材料
名称 | 规格 | 厂家 |
中粘度壳聚糖 | 分析纯 | 阿拉丁试剂 |
十二烷基硫酸钠 (SDS) | 分析纯 | 上海英鹏 |
十二烷基苯磺酸钠 (SDBS) | 分析纯 | 上海英鹏 |
ɑ-环糊精 (ɑ-CD) | ≥98.0% | 阿拉丁试剂 |
β-环糊精 (β-CD) | 分析纯 | 国药集团化学试剂有限公司 |
盐酸 | 分析纯 | 国药集团化学试剂有限公司 |
罗丹明B | 分析纯 | Sigma |
水杨酸钠 | 分析纯 | 国药集团化学试剂有限公司 |
甲基蓝 | 分析纯 | 国药集团化学试剂有限公司 |
表2.2 实验主要仪器/设备
设备名称 | 型号 | 厂家 |
电子天平 | FA2014 | 上海恒平科学仪器 |
数显控温磁力搅拌器 | SZCL-2A | 巩义市予华仪器有限责任公司 |
超声清洗器 | KQ-50E | 昆山超声仪器有限公司 |
微量移液器 | 720005 | 大龙兴创实验仪器 |
紫外分析仪 | ZF-6 | 上海嘉鹏科技有限公司 |
热场发射扫描电子显微镜 | JSM-7001F | 日本电子株式会社 |
冷冻干燥机 | FD-1C-50 | 北京博医康仪器 |
电热恒温鼓风干燥箱 | YLD-2000 | 浙江联泰仪表有限公司 |
2.2 实验内容
2.2.1原料的准备
2.2.1.1壳聚糖溶液的配制
称取2g的壳聚糖(CS),采用移液枪加入0.8g的盐酸于定量去离子水稀释,保证壳聚糖的质量分数为2%,将称量好的壳聚糖加入定量去离子水,与稀释好的盐酸混合,加入磁子搅拌。将配制好的混合溶液常温下搅拌1.5小时左右,使其溶解混合均匀。搅拌后静置1小时,消除溶液中的气泡,配置得到质量分数为2%的壳聚糖溶液。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示:




您可能感兴趣的文章
- 可聚合高分子模板增强制备高耐久超疏水涂层文献综述
- PVC/ABS合金的制备及性能研究开题报告
- 设计具有增强的赝电容及电催化性能的Co3O4/NiCo2O4双壳纳米笼结构外文翻译资料
- 光子上转换手性液晶:显著放大的上转换圆偏振发光外文翻译资料
- 氧空位型LiV3O8纳米片的快速稳定储锂性能研究外文翻译资料
- 应用于高性能钙钛矿太阳能电池的电子传输层的前体工程外文翻译资料
- 复合材料科学与技术 ——含碳纳米管的多孔导电弹性体复合材料悬浮在共连续聚合物的狭窄孔隙中的混合纳米复合材料外文翻译资料
- 一种用于先进锂硫电池源自聚罗丹宁纤维素的氮硫双掺杂碳外文翻译资料
- 短玻璃纤维增强聚丙烯控制界面和力学性能参数外文翻译资料
- 含Ca0的LaCO.0H纳米齿轮及其发光和脱NOx性能外文翻译资料




