壳二糖与EtmimCl-Urea相互作用的分子模拟研究毕业论文
2020-05-21 22:20:03
摘 要
在自然界中壳聚糖( chitosan) 储量非常的丰富,它既属于天然高分子材料,也属可持续发展的绿色再生性资源。近年来壳聚糖越来越受人们关注,因为它在化学、食品防腐、医学、农业、污水处理等方面应用越来越多。然而在壳聚糖的结构中存在着较强的分子内和分子间氢键,这些因素导致有少量的溶剂才能溶解壳聚糖,使其发展缓慢制。壳二糖是壳聚糖的最小二聚体。最近几年离子液体是新出的一种绿色溶剂,它跟其他的溶剂相比有突出的优点。
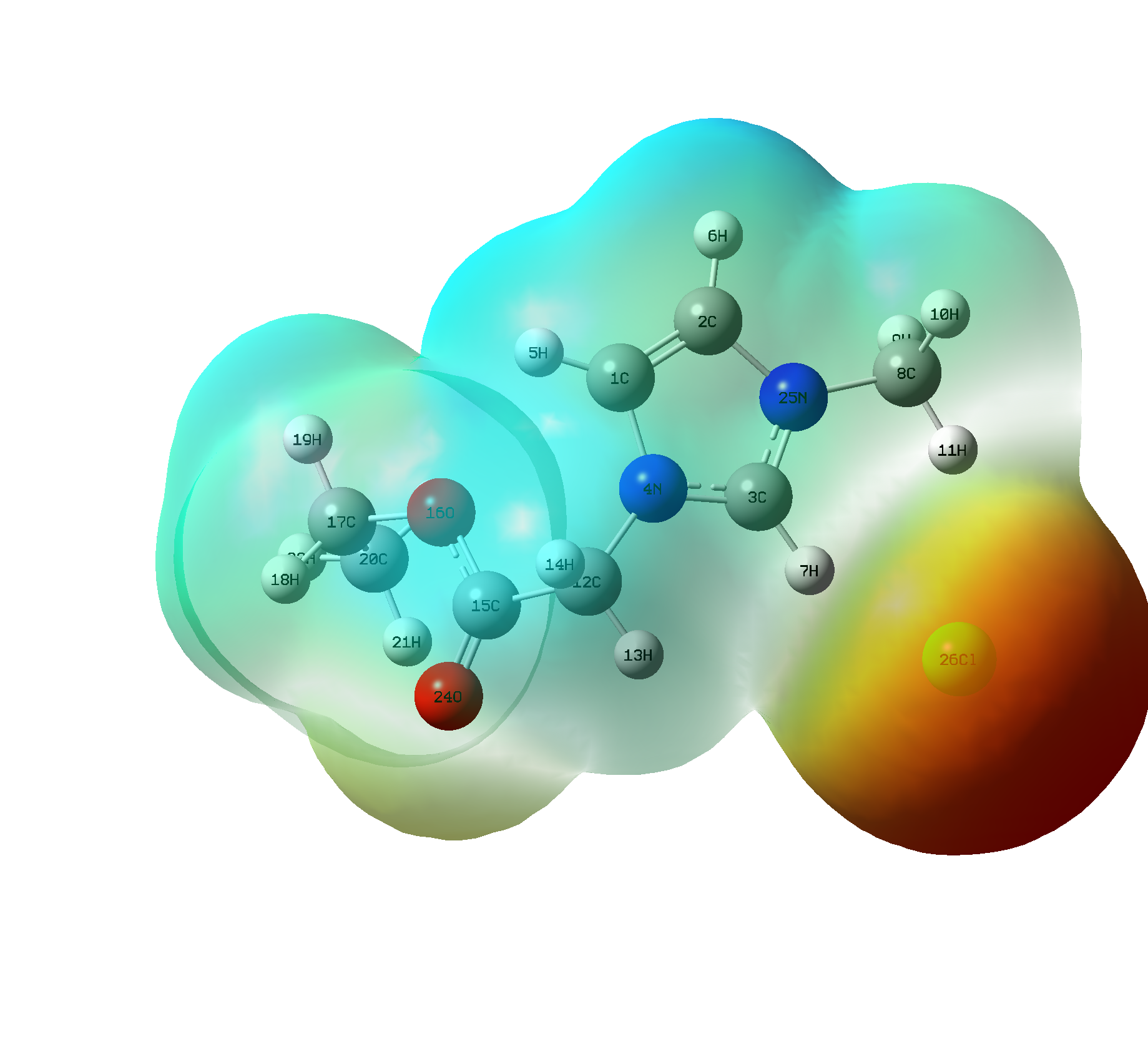
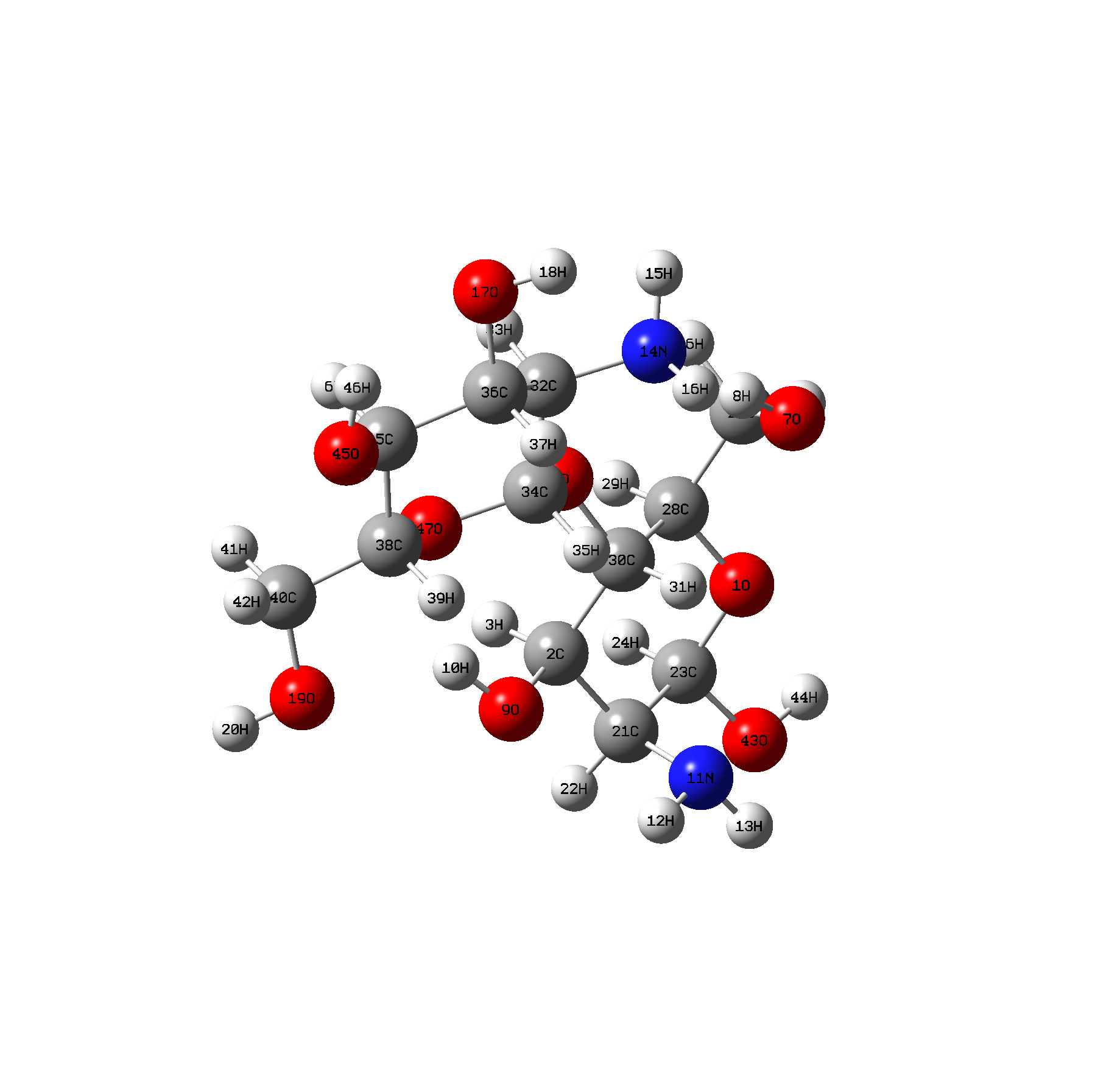
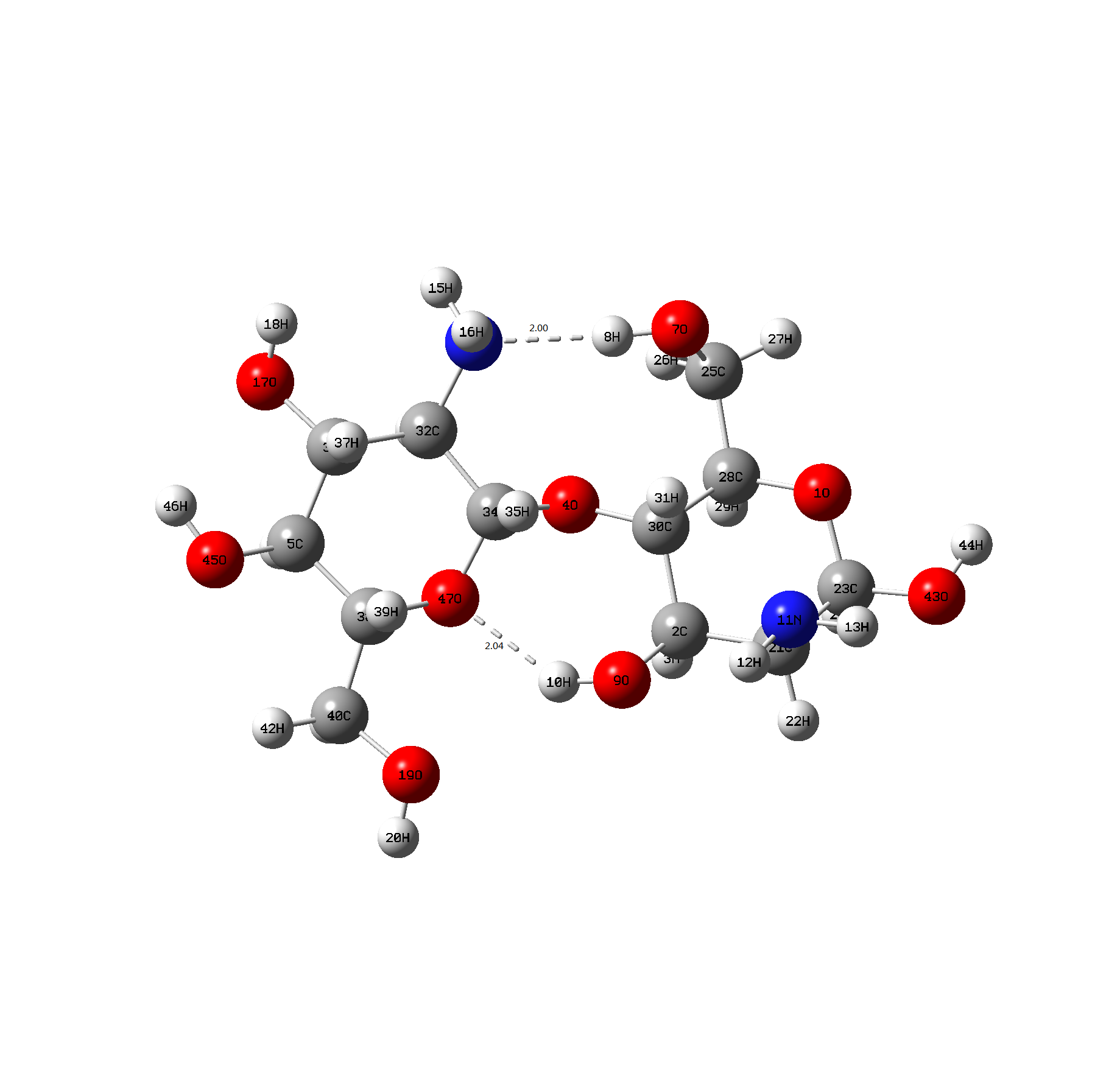
本次实验采用Gaussian 09W分子模拟软件对离子液体EtmimCl、壳二糖和尿素进行优化和频率计算,分别得到离子液体EtmimCl、壳二糖、EtmimCl-壳二糖-尿素优化后的构型及频率,对其进行分析其溶解机理。EtmimCl离子液体与壳二糖26 Cl与73 H形成氢键;26 Cl和42 H 形成氢键;58O与10H形成氢键;58O与71氢形成氢键;46O与16H形成氢键,使得壳二糖溶解于EtmimCl-Urea离子液体。
关键词:离子液体 壳二糖 尿素 分子模拟 溶解机理
Molecular Simulation of the Interaction Between Chitosan and Ionic Liquid EtmimCl-Urea
Abstract
Chitosan is a kind of natural polymer material with abundant natural resources, which is a kind of environment friendly and sustainable development.In recent years, chitosan and its derivatives have been widely used in chemical, food preservation, medicine, agriculture, sewage treatment and so on, which has attracted great attention of people.But too much strong intra-molecular hydrogen bonding exist,the solvent which can be used to dissolve the Chitosan is very poor,this is the most important reason that Chitosan can’t be effectively utilized.Chitobiose is the minimum dimer of chitosan.Ionic liquids are emerging in recent years a green solvent, as compared with the conventional solvent has unique advantages.
The experiment Gaussian09W molecular modeling software for ionic liquids EtmimCl Chitobiose optimization, frequency calculation and Urea,so we get the opt-structure of EtmimCl,chitobiose and EtmimCl-chitobiose and their frequency calculation.So we find that between the chitobiose and EtmimCl ionic liquid 26Cl and 73H form hydrogen bonds; 26Cl and 42H form hydrogen bonds; 58O form hydrogen bonds with 10H; 58O and 71H form hydrogen bonds; 48O and 16H form hydrogen bonds, leading to chitobiose is dissolved in the ionic liquid EtmimCl-Urea.
Keyword:ionic liquid EtmimCl ;chitosan;urea;molecular modeling;dissolution
目 录
摘要 II
Abstract III
第一章 前言 1
1.1 选题背景 1
1.2 壳聚糖 2
1.2.1 壳聚糖 2
1.2.2 壳聚糖的性质 2
1.2.3 壳聚糖的制备 3
1.2.4 壳聚糖的应用 3
1.2.5壳二糖简介 4
1.3 离子液体 5
1.3.1 离子液体概述 5
1.3.2离子液体的优点 5
1.3.3 离子液体的应用 6
(1)离子液体在有机合成中的应用 6
(2)离子液体在催化反应中的应用 6
(3)离子液体在电化学中的应用 6
(4) 离子液体在分离领域的应用 6
1.4 分子模拟 7
1.4.1 分子模拟的概念 7
1.4.2 室温离子液体的分子动力学模拟 7
1.4.3 分子模拟力场 7
1.4.4 量子化学计算的原理 8
1.8.2密度泛函理论(Density Functional Theory) 8
1.5 本文思路 9
第二章 EtmimCl离子液体和壳二糖的构型优化 10
2.1 引言 10
2.2 计算方法 10
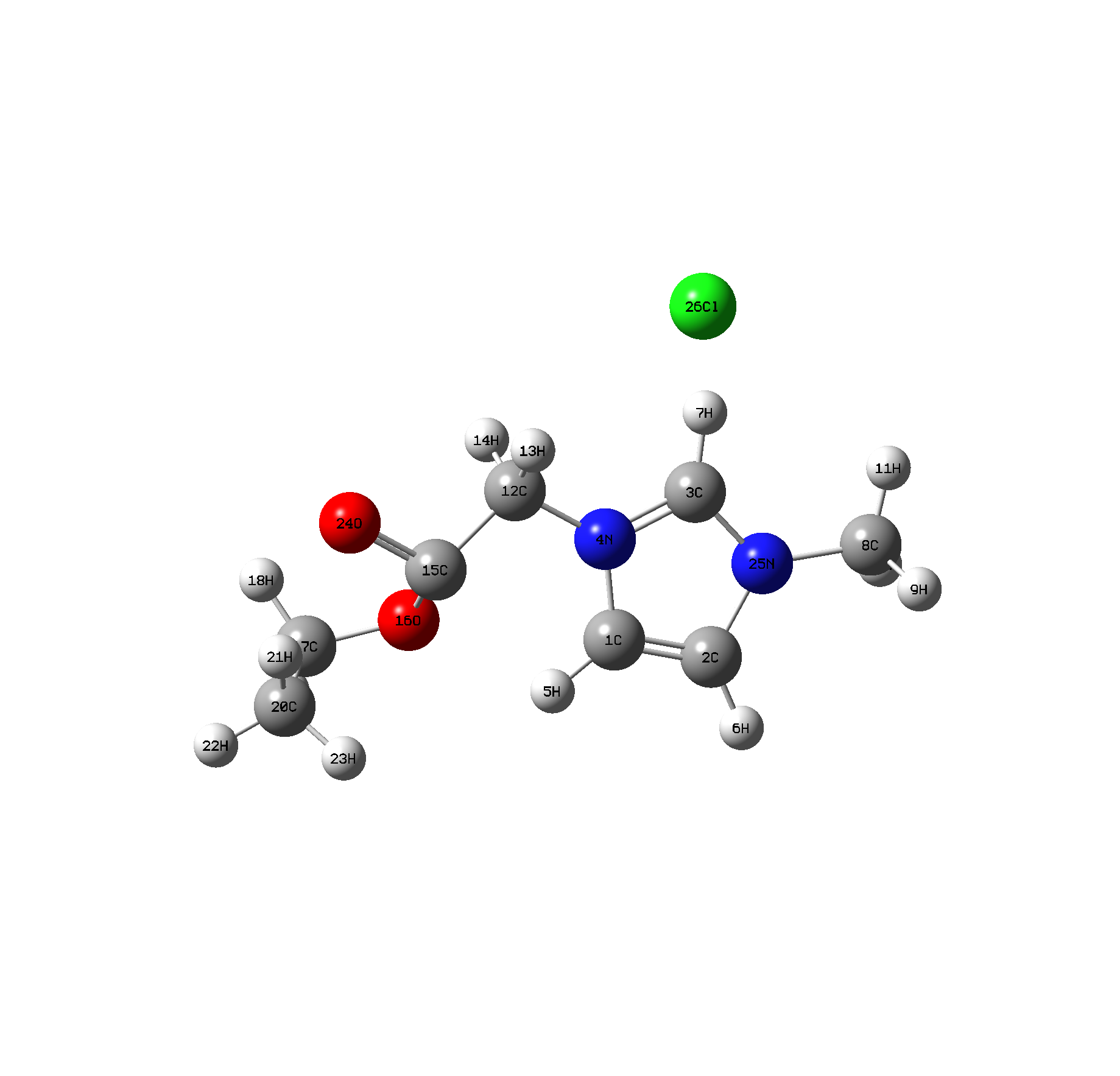
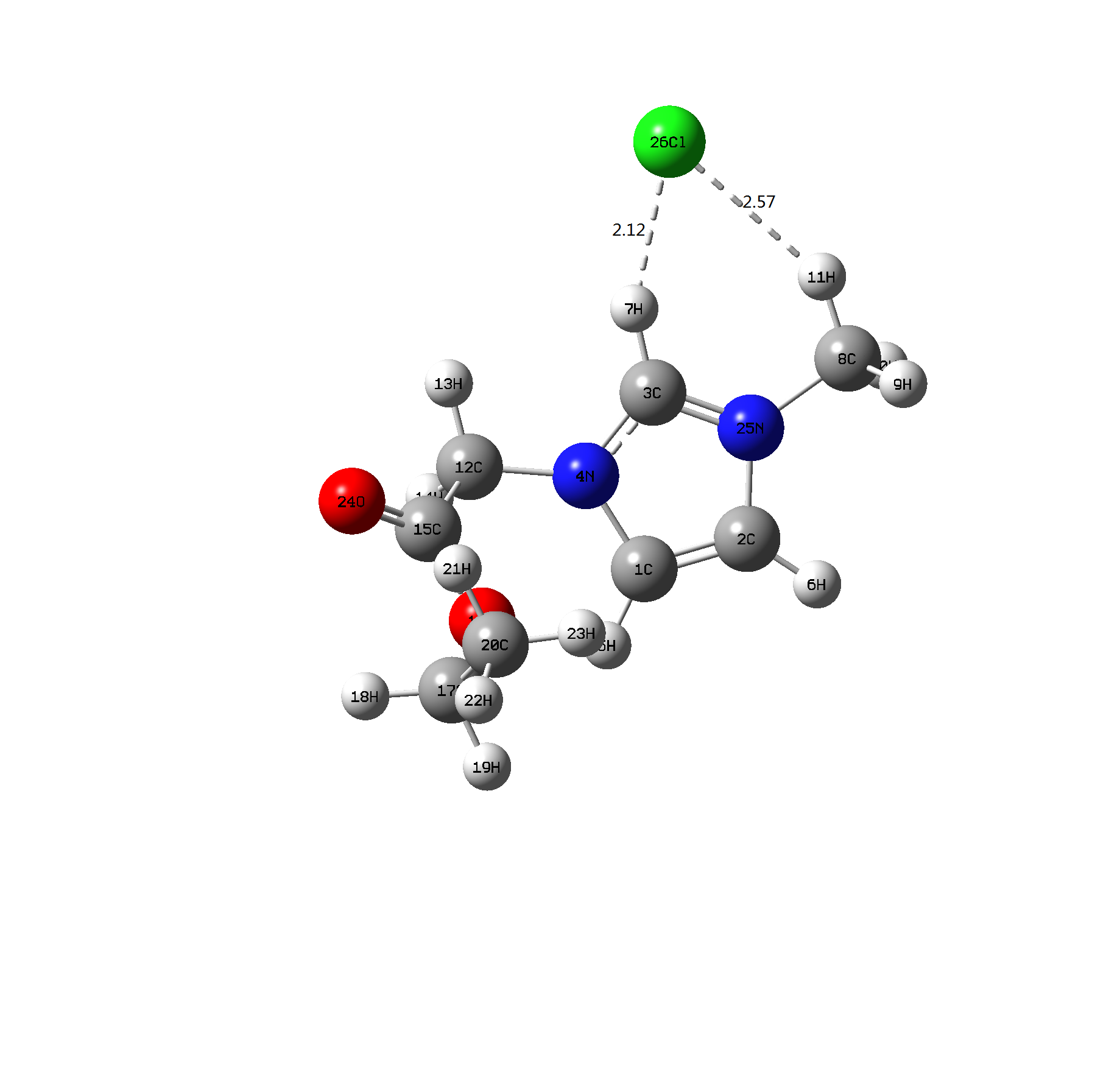
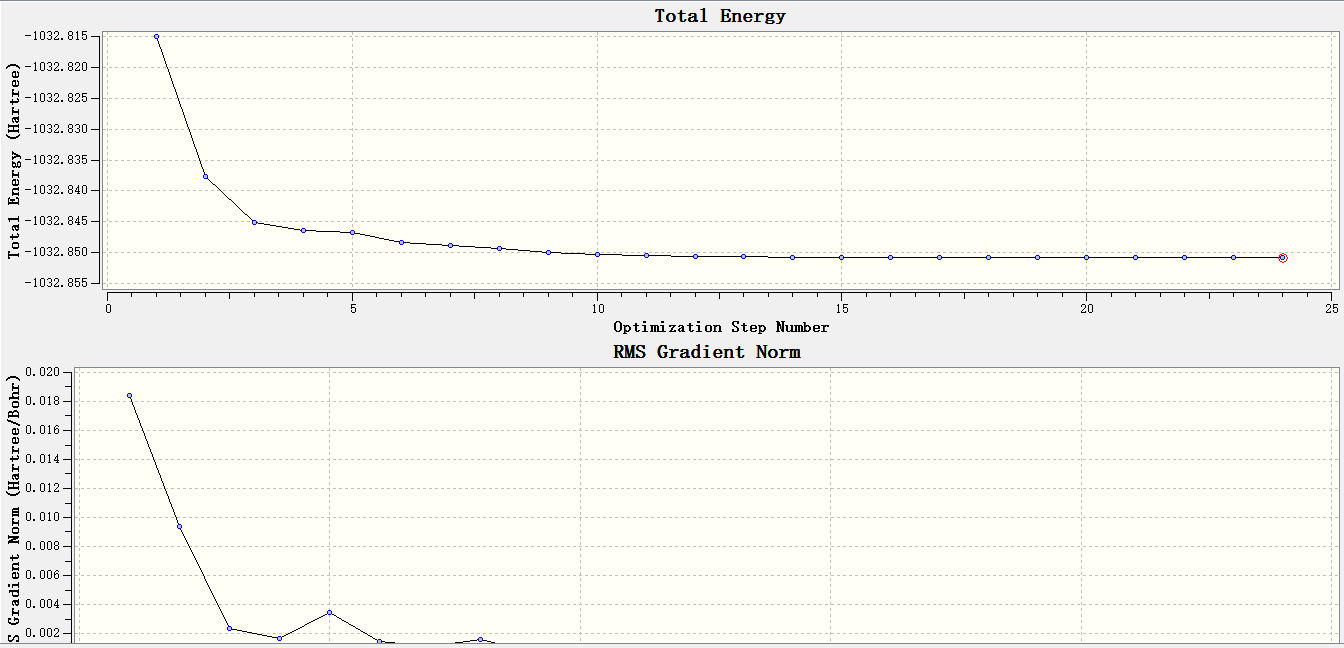
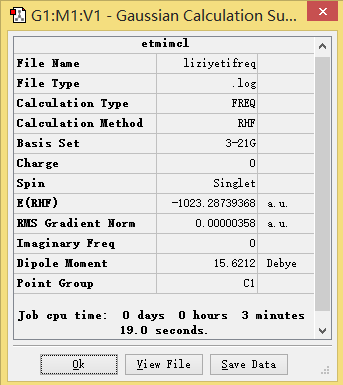
2.3 EtmimCl离子液体的构型及其优化 10
2.3.1 EtmimCl离子液体构型 10
2.3.2 结论 12
2.4 壳二糖的构型及其优化 14
2.4.1壳二糖构型对比 14
2.4.2 结论 15
第三章壳二糖与EtmimCl离子液体的相互作用 19
3.1引言 19
3.2 EtmimCl离子液体和壳二糖的构型及其优化 19
3.2.1 EtmimCl离子液体构型 20
3.2.2 结论 23
第四章结论与展望 27
4.1 结论 27
4.2 展望 27
参考文献 28
致 谢 ........................................................................................................................................ 29
第一章 前言
1.1 选题背景
壳聚糖是甲壳素经过脱乙酰得到的产物,为自然界中储存量最大的碱性生物多糖。壳聚糖及其衍生物具有可降解性、抗菌性、成纤成膜性、生物相容性等优异的特性,在广泛的领域如食品领域、医药领域、纺织领域、造纸领域、日化领域中具有广大的应用前景[1]。但由于分子内和分子间氢键较强烈,导致壳聚糖的溶解及改性很困难,极大限制了壳聚糖的应用。目前为止,壳聚糖的溶解方法主要为对其内部的氢键网络结构进行破坏,从而使之溶解,其溶剂一般为强碱溶液体系、锂盐-强极性非质子极性溶剂体系等,这些溶剂具有强腐蚀性、毒性、难后续处理等缺点,与当今的绿色环保工业生产的理念相悖。因此寻找一种利于壳聚糖溶解及改性的绿色溶剂成为拓展壳聚糖应用的重要方向和内容[2][3]。
离子液体,也称为室温离子液体,通常指在-30~50℃下呈液态的由阳离子与阴离子所构成的物质。早在1914年, Walden发现了一个在室温下呈液体的有机盐类硝酸乙基胺,它的性质不稳定,易爆炸,当时并未引起学者的关注[4]。直到20世纪50年代, F.H.Hurley 和 T.P.Wier 将N-甲基吡啶加入到AlCl3中,发现:两个固体混合物自发地形成了澄清透明的液体,这个无意的发现成就了当今所说的第一个离子液体。随后陆续合成出一系列高温的,低温的卤盐离子液体,这些有机离子盐有一个共同的缺点:遇水时反应生成具腐蚀性的盐酸。因此,学者们一向试图合成制备一种稳定的离子液体。直到1992年,Wilkes的研究小组合成了性质稳定的1-乙基-3-甲基咪唑四氟硼酸盐。此后,离子液体的研究才得以迅速发展[5][6]。
相关图片展示:
您可能感兴趣的文章
- 改性壳聚糖的合成、性质及其应用的研究进展综述外文翻译资料
- 染料与表面活性离子液体相互作用的光谱研究外文翻译资料
- 热力学,结构和动力学的原子论见解离子液体1-己基-3-甲基咪唑六氟磷酸盐分子动力学研究外文翻译资料
- 仙人掌果肉中的倍他青色素外文翻译资料
- 同轴静电纺丝法制备TiO2@CdS/PVA复合纳米纤维毡及其光降解催化性能的 研究.外文翻译资料
- 一种用于人体辐射散热的双向功能纺织品外文翻译资料
- 抗菌抗氧化剂电活性注射水凝胶作为皮肤创面愈合止 血粘连的自愈创面敷料外文翻译资料
- 二萜异斯特维醇三苯基溴化膦阳离子的合成及其 在海胆胚胎模型中的抗分裂活性外文翻译资料
- 异斯特维醇的制备及其与y-环糊精的包合物外文翻译资料
- 不同食品模型中非营养 甜味剂、甜菊糖和三氯蔗糖的提取效率分析外文翻译资料




