过渡金属掺杂 MoS2 电催化还原一氧化碳的第一性原理研究毕业论文
2021-12-04 19:24:55
论文总字数:25113字
摘 要
工业的高速发展以及对化石燃料的过度依赖已经引起了全球的能源危机。含碳化石燃料不完全燃烧产生的一氧化碳不仅对环境造成污染,而且严重影响人体的血红蛋白对氧气的利用,引起一氧化碳中毒。电化学催化还原一氧化碳产生醇类化合物具有可在常温常压条件下进行、消耗的能源清洁等优点。通过可再生的电能将一氧化碳转换成有经济附加值的工业原料,具有同时解决能源危机和环境污染的潜在价值。本课题拟采用第一性原理计算为研究手段,以过渡金属钴元素掺杂二硫化钼体系作为催化剂模型,探究其对一氧化碳电催化还原生成醇类的微观反应机制。研究发现钴元素掺杂前、后的单层二硫化钼体系均可将一氧化碳分子活化,进而电催化还原成甲醇,其中未掺杂的单层二硫化钼更有利于甲醇的生成。另外,钴元素掺杂的单层二硫化钼还可以通过相邻的两个活性位点将一氧化碳电催化还原成乙醇,而未掺杂的单层二硫化钼则不能催化生成乙醇。
关键词:过渡金属掺杂MoS2;电催化还原CO;第一性原理;密度泛函理论
Abstract
The rapid development of industry and over-reliance on fossil fuels have caused a global energy crisis. Carbon monoxide produced by incomplete combustion of carbon-containing fossil fuels not only pollutes the environment, but also seriously affects the utilization of oxygen by human hemoglobin, causing carbon monoxide poisoning. Catalytic reduction of carbon monoxide via electrochemical means has the advantages of being carried out at room-temperature and pressure. By using renewable electric energy, converting carbon monoxide into economical valuable industrial materials through has the potential to solve energy crisis and environmental pollution, simultaneously. In this project, by means of the first principle calculation, the electrochemical catalysis reaction mechanism of carbon monoxide on the cobalt (Co) doped and non-doped single layered molybdenum disulfide (MoS2) is studied. It is found that methanol is the product on both single-layer Co@MoS2 and MoS2, whereas the non-doped MoS2 shows more favoble to yield methanol. On the contrary, the single layered Co@MoS2 is able to prouduce ethanol on the adjancent active sites, while the non-doped system does not.
Key Words:Transition metal doped MoS2;CO Elelctrochemical Reduction Reaction;First-principles;Density Functional Theory
目 录
第1章 绪论 1
1.1引言 1
1.2 MoS2材料基本介绍 2
1.2.1 MoS2带隙和催化析氢活性 2
1.2.2 MoS2掺杂 2
1.2.3 MoS2应用 3
1.3 本论文研究内容及工作 5
第2章 理论计算原理 6
2.1 第一性原理 6
2.2 密度泛函理论 6
2.3 材料模拟软件介绍 7
第3章 理论计算方法 8
3.1 模型体系的搭建 8
3.2 计算参数设置 9
第4章 结果和讨论 11
4.1 电催化还原一氧化碳的反应机理 11
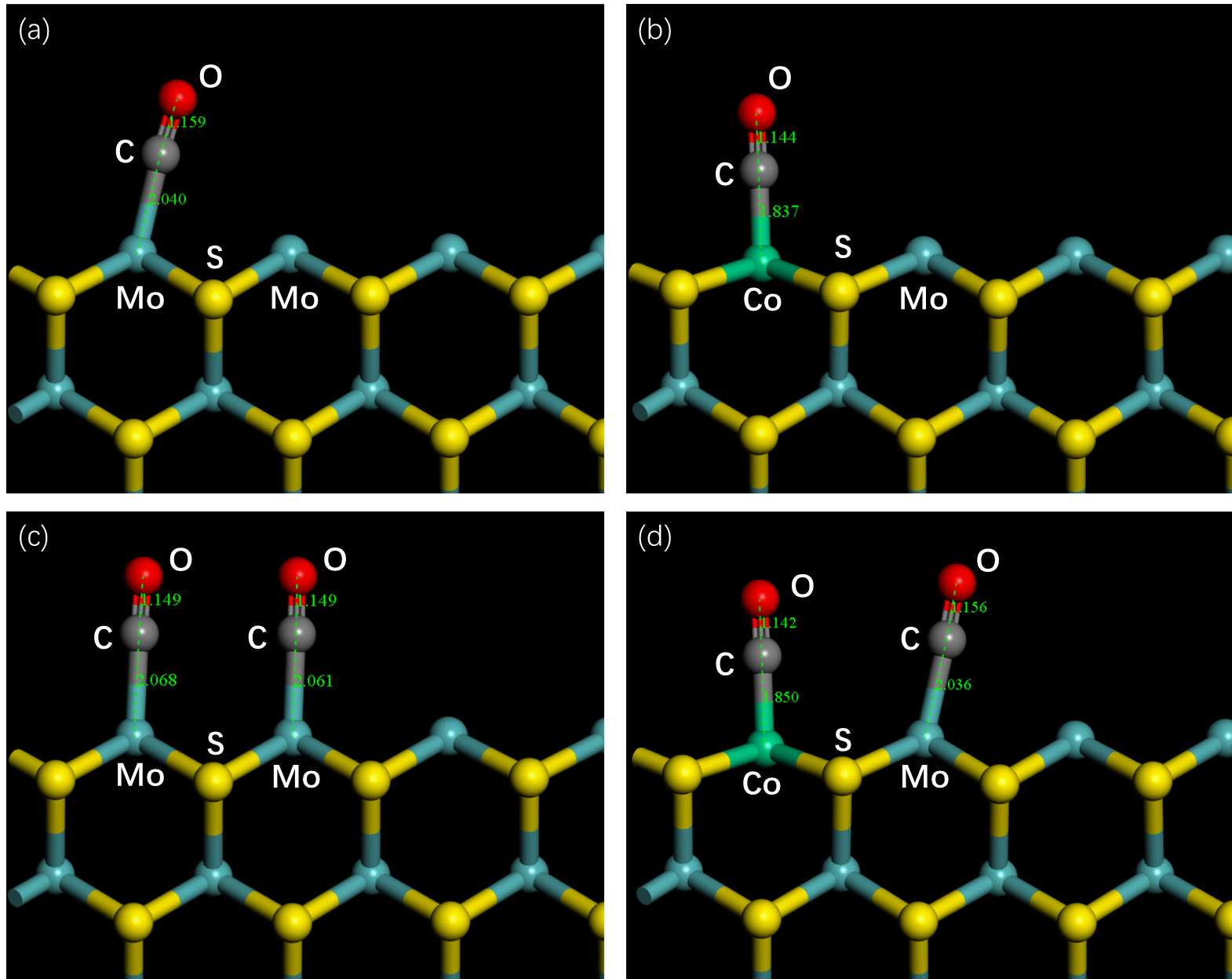
4.2 反应物的结构参数变化 12
4.3 反应物、中间体、产物的Gibbs自由能 13
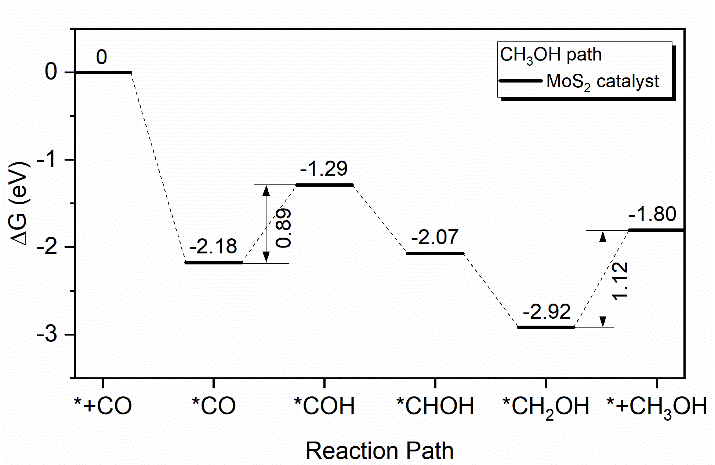
4.3.1单层二硫化钼电催化还原一氧化碳的路径 15
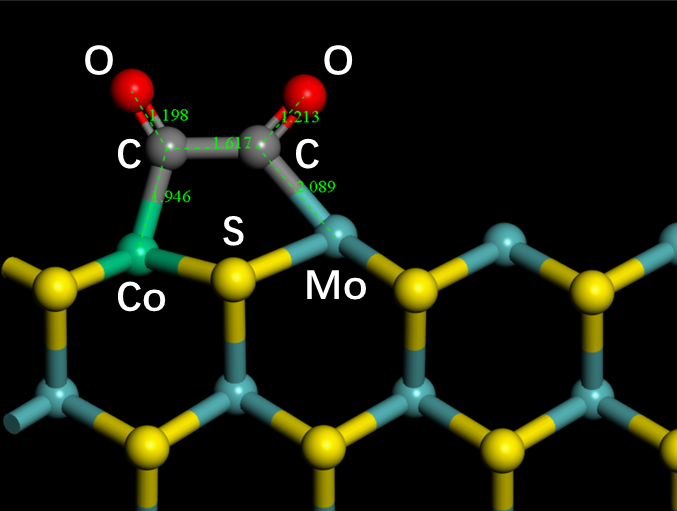
4.3.2 钴掺杂单层二硫化钼电催化还原一氧化碳的路径 16
4.3.3钴掺杂前、后对一氧化碳电催化还原路径的影响 18
第5章 结论与展望 20
参考文献 22
致 谢 25
第1章 绪论
1.1引言
一氧化碳(CO)是一种在自然界中广泛存在的略轻于空气的无色、无嗅、无味的有毒气体。由于人类使用的大量含碳自然资源的不完全燃烧,使得一氧化碳在大气污染中分布最广,最大。一氧化碳的主要生成机理为:RH→R→RO2→RCHO→RCO→CO(其中,R表示碳氢自由基团)。一氧化碳的主要来源包括工业生产过程、工业事故,日常生活以及自然界中。其中,工业生产包括冶金工业和化学工业生产过程中燃料的不完全燃烧;而工业事故包括矿井放炮和煤矿瓦斯爆炸事故。另外,现代交通产生的尾气排放;家庭中产生的煤气或液化气管道漏气;以及自然灾害包括森林火灾、地震、火山爆发等也是一氧化碳的天然来源[1]。此外,高层大气的化学反应、二氧化碳的轻微解离作用以及生物体的新陈代谢过程中也会产生少量的一氧化碳。一氧化碳对人体的主要危害是,它能与血液中的携氧血红蛋白中的铁原子络合,生成强配位络合物。这种络合物的生成会降低血红蛋白对氧气的结合,从而降低血液的载氧能力,进而使得人体各器官获得氧气的量降低,引起人体一氧化碳中毒[2]。
为了将一氧化碳变废为宝,各国研究者采用了多种手段。其中电化学催化还原CO产生具有高附加值的工业原料,具有可在常温常压条件下进行、消耗的能源清洁等优点[3]。通过可再生的电能将CO转换成有经济附加值的工业原料,具有同时解决能源危机和环境污染的潜在价值[3-6]。例如,在倪小明等的研究中[5],水煤气变换反应在Fe-Zn-Zr催化剂CO加氢可生成甲烷或者转换成C2 ,甚至在该催化剂上的加氢生成的主要产物中烃类所占的比例远远大于CO2所产生的。
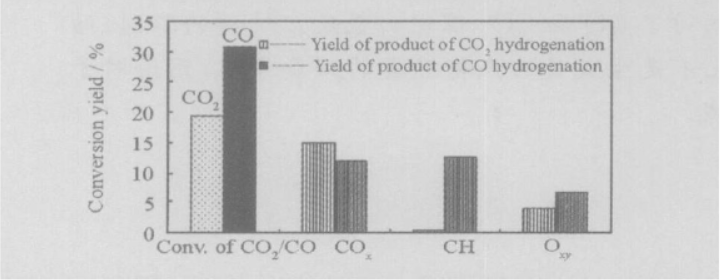
图1.1 CO2和CO在Fe-Zn-Zr催化剂上的催化加氢。引自文献[5]。
本研究采用典型的过渡金属硫属化合物单层MoS2作为电化学催化剂,由于其具有类石墨烯的二维平面结构和优良的物理化学性质,及其奇异的电子结构、可观的直接带隙[7],以及催化性质和储能性质等特性使得它成为晶体管、光发射器件、气体传感器[8, 9]等领域的研究热点,以及电化学催化析氢、锂离子电池的电极材料设计等领域的研究前沿和热点[6-9],同时也具有广泛的应用前景。
因此,对一氧化碳进行有效回收和利用具有解决能源及环保问题的双重意义。如何有效地将一氧化碳作为原料“变废为宝”成为科学研究的一个热点。本文将着重讨论一氧化碳还原成醇类的反应机理。
1.2 MoS2材料基本介绍
1.2.1 MoS2带隙和催化析氢活性
具有稳定的六方相的2H二硫化钼(MoS2)在过去的几十年中一直是研究最多的过渡金属二硫化物之一。在过去的五年中,MoS2的亚稳态阶段(1T, 1T', 1T'',和 1T''')越来越吸引人们的关注[7]。与2H相MoS2中的[MoS6]三棱柱不同,这些亚稳态相由[MoS6]八面体组成,相邻的钼之间的距离不同。由于晶体结构和电子构型的不相同,这些亚稳的多型体具有诱人的物理特性,并在各个领域都有潜在的应用。Zhao, W.等[7]通过光电发射光谱证实,单层的二硫化钼具有可观的直接带隙,达到了1.7电子伏。
由于MoS2表面缺乏活性位点,所以它的表面不具备催化能力,而MoS2的边缘具有催化析氢活性[10, 11]。Jaramillo等[10]在溶液中测量电化学活性之前,通过原子解析该催化剂的表面,确定了纳米级二硫化钼(MoS2)上由贵金属催化的氢析出的活性位点。通过制备不同尺寸的MoS2纳米颗粒,系统地改变了Au(111)上MoS2纳米颗粒表面位置的分布,并用扫描隧道显微镜对其进行了定量。发现氢逸出的电催化活性测量值与MoS2催化剂上边缘位点的数量线性相关。
二硫化钼可作为工业催化剂,并在电催化制氢方面显示出作为铂的低成本替代品的前景。Karunadasa等[11]通过利用五吡啶基配体的强配位环境,合成并在结构上表征了一种定义明确的二硫化钼-四硫化钼配合物,该配合物在电化学还原时可以从酸性有机介质和酸性水中催化生成氢气。
1.2.2 MoS2掺杂
增强MoS2催化活性最常用的方法是在其中引入杂质原子[12-14]。文献报道中,将过渡金属掺杂到MoS2中可以增加其表面的活性位点,提高其催化性能。研究表明,不同类型的过渡金属对MoS2掺杂均有效果。例如VB族的钒(V)、铌(Nb)、钽(Ta),VIB族的铬(Cr)、钨(W),VIIB族的锰(Mn)、铼(Re),VIII族的铁(Fe)、钴(Co)、镍(Ni)、钌(Ru)、铑(Rh)、钯(Pd)、锇(Os)、铱(Ir)、铂(Pt),IB族的铜(Cu)、银(Ag)、金(Au)掺杂单层二硫化钼后均能形成稳定的TM-Mo键[12, 13],使得体系有较低的形成能。而过渡金属的掺杂可以给MoS2提供新的催化活性位点,从而增强其催化活性。
研究结果表明,过渡金属铁(Fe)、钴(Co)、镍(Ni)、铜(Cu)、银(Ag)、金(Au)、铑(Rh)、钯(Pd)、铂(Pt)和铱(Ir)掺杂单层二硫化钼后,掺杂原子向平面外突出,形成较长的TM-Mo键[13]。掺杂原子与表面之间强的相互作用形成了稳定的掺杂表面。经过电子结构计算表明,掺杂单层MoS2后,某些过渡金属,如铁、钴、镍、铜、银等原子会失去部分电子(约0.04 − 0.36 e),而另一些过渡金属,如金、铑、钯、铂、铱原子会获得电子(约0.11 − 0.34 e)。通过对掺杂体系的态密度(density of states)分析发现,不同的过渡金属掺杂会不同程度地在MoS2的带隙中引入杂质态。这些杂质态对应于过渡金属nd轨道。此外,过渡金属掺杂还能对MoS2表面的磁矩进行调控。
赵普举[8]采用密度泛函理论研究了TM/MoS2掺杂体系对一氧化碳分子氧化的催化性能。这种TM/MoS2掺杂体系是由单层MoS2表面吸附单层3d过渡金属原子形成的。他的研究发现,对于体系的稳定性而言,相比于吸附单个过渡金属原子,在单层MoS2表面吸附单层3d过渡金属原子的稳定性更高。当一氧化碳分子吸附在Mn/MoS2表面时,其碳原子(C)与过渡金属锰原子(Mn)间的作用最强,一氧化碳分子的C−O键伸长最多。这一现象表明,一氧化碳分子中的C−O键更容易被破坏,从而有助于一氧化碳分子进行后续的氧化反应。过渡金属nd轨道的杂质态被不同程度地引入了掺杂后MoS2的带隙中也说明掺杂后表面的稳定性。此外, 过渡金属原子掺杂能够有效调控MoS2表面电子结构的事实,也可通过过渡金属掺杂有效改变了掺杂表面磁矩的现象证实。
Abbasi等[14]通过密度泛函理论计算发现,钼边缘原子附近的掺杂的低浓度铌可以通过改变中间体与二硫化钼边缘原子的结合能来增强二氧化碳形成的时间。通过原位差示电化学质谱等实验的电化学结果表明,在50 − 150 mV的过电位范围内,离子液体中5%铌(Nb)掺杂的垂直排列二硫化钼显示出比原始二硫化钼高一个数量级的一氧化碳形成翻转频率(turn-over frequency)。在整个研究过电位范围内(100 − 650 eV),该催化剂的反应时间也比银纳米粒子高两个数量级。这证明了掺杂的二硫化钼催化剂可将二氧化碳电催化转化为富含能量的燃料以实现有效的碳中和循环。
在掺杂二硫化钼催化剂体系中可以根据需要选择金属掺杂剂,以增强或减弱关键中间体的结合能。Tsai等[12]通过研究边缘位点上的氢释放反应(HER),确定了金属掺杂剂的作用是改变边缘上硫键的强度,使得氢与边缘上的硫原子键合。此外,MoS2型催化剂趋于具有接近最佳的氢键,由于氢键的独特的覆盖依赖性。同时,证实了掺杂后的二硫化钼的氢吸附自由能比原始MoS2有较为显著地提高。
1.2.3 MoS2应用
二硫化钼的催化性质和储能性质等特性使得它在晶体管、光发射器件、气体传感器[8, 9],以及催化析氢、锂离子电池等领域的研究前沿和热点[6-9],具有广泛的应用前景。
请支付后下载全文,论文总字数:25113字
相关图片展示:


您可能感兴趣的文章
- 甲基丙烯酸修饰氢氧化镁微粒及其表征开题报告
- 碳点修饰SiO2纳米球的制备与表征文献综述
- 二维VOPO4纳米片在水系锌离子电池中的研究文献综述
- 塑料注射成型的实验研究: 型腔压力和模具温度对产品质量的影响外文翻译资料
- 一种用于同时电化学检测铅(II)、镉(II)和锌(II)的具有分层MXene-铋纳米复合材料的微铣式微电网传感器外文翻译资料
- 日光驱动的可充电抗菌和抗病毒纳米纤维膜在生物保护中应用外文翻译资料
- 一种无金属的聚合物光催化剂,用于在可 见光下从水中制氢外文翻译资料
- 二维共价自组装:将共价有机骨架纳米球连接到晶体和多孔薄膜中外文翻译资料
- 模拟二维材料的粉末X射线衍射图外文翻译资料
- 基于碳化硅反应活性的烧结添加剂外文翻译资料




