氮及金属原子共掺杂石墨烯电催化还原二氧化碳反应的第一性原理研究毕业论文
2020-02-19 15:33:37
摘 要
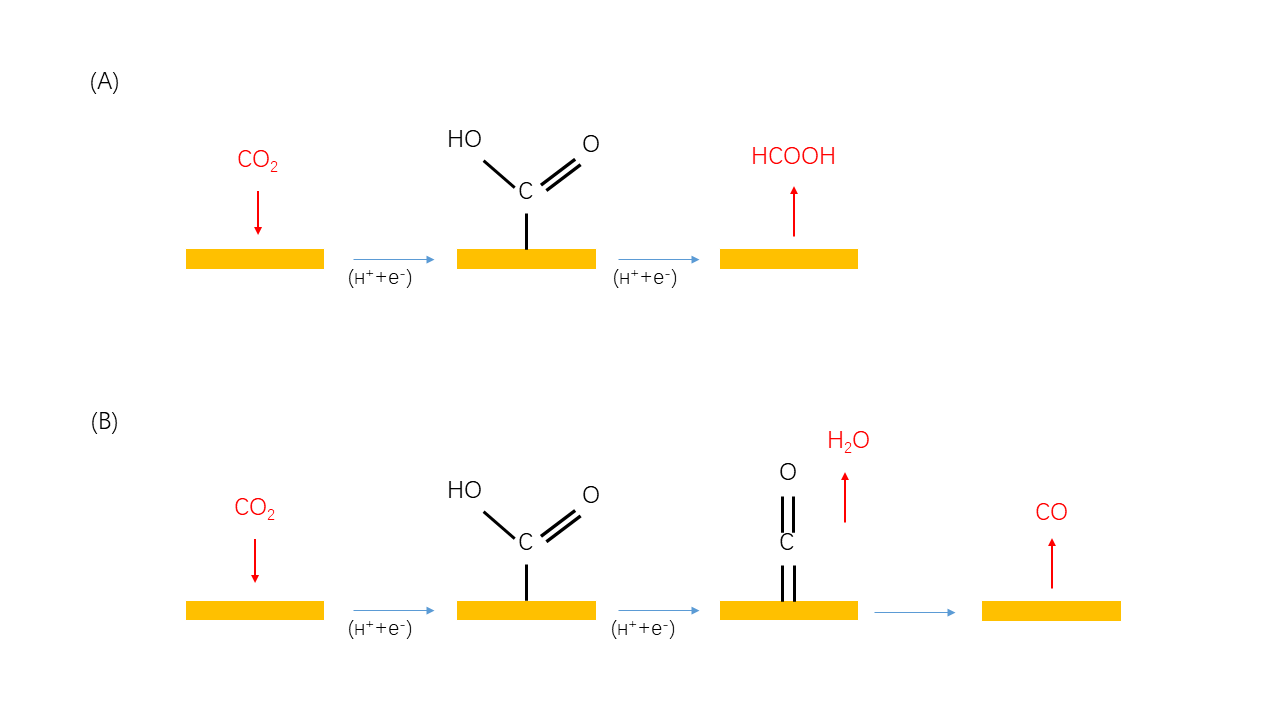
随着全球变暖的趋势越来越严峻,如何处理过量排放的CO2成为了一个热点话题。运用电化学催化还原CO2生成具有高附加值的化工原料 (如HCOOH或CO) 是一种可行的手段。本论文采用第一性原理密度泛函理论为研究方法,对Ni,Cu和Zn三种过渡金属与氮共掺杂石墨烯体系的电子结构性质进行了研究,并从理论上探索了利用它们作为催化剂还原CO2的反应机理。电子密度和差分电荷密度分析表明,CO2分别吸附到三种过渡金属掺杂体系后,均与掺杂金属形成了化学键,属于化学吸附。分波态密度分析表明,三种掺杂的过渡金属的s能带和d能带分别与CO2的σ*反键轨道和n非键轨道发生了杂化耦合。另外,对各个反应物、中间体和产物进行了结构优化,得到它们的Gibbs自由能,并绘制了它们的自由能阶梯图。对比三种体系的自由能阶梯图发现,对于三种过渡金属掺杂体系而言,CO2还原生成HCOOH比生成CO在热力学上更有利。对比这三种体系的催化性能发现,Zn和Ni掺杂体系在生成HCOOH和CO反应中比Cu掺杂体系表现更好。
关键词:氮与过渡金属共掺杂石墨烯;电催化还原CO2;第一性原理;密度泛函
Abstract
As global warming is getting an increasingly serious issue, how to deal with excessive CO2 emissions has become a hot topic. Converting CO2 into high value-added compounds (e.g. HCOOH or CO) via the electrochemical catalytic reduction is a feasible way. In this study, the electronic structure properties and the electrochemical reduction mechanism of three transition-metals (TMs) (such as Ni, Cu and Zn) and nitrogen co-doped graphene systems (in short, the TM-N codoped system) were investigated and compared, respectively, by means of the first-principles density functional theory (DFT) calculations. Electron density and charge density difference analysis show that chemical bonds were formed between CO2 and the doped TMs, when CO2 adsorbing on three TM-N co-doped systems. Partial density of states (PDOS) analysis reveals that the s-bands and d-bands of three TMs hybrid with the σ* anti-bond oribital and n nonbond orbitals of CO2, respectively. In addition, the Gibbs free energies of reactants, intermediates and products were obtained after geometry optimizations, and then the free energy diagrams of three systems were plotted. By comparing the free energy diagrams of these three systems, it shows that producing HCOOH is thermodynamically favorable than yielding CO for all studied systems. When comparing with three TMs doped systems, the Zn and Ni doped systems were better performed than Cu doped one.
Key Words:Nitrogen and Transition-Metal Co-doped Graphene;CO2 Elelctrochemical Reduction Reaction;First-principles;Density Functional Theory
目 录
第一章 绪论 1
1.1引言 1
1.2 CO2还原方法 2
1.2.1 热化学法还原CO2 2
1.2.2 光催化还原CO2 3
1.2.3 电催化还原CO2 4
1.3 本论文研究内容及工作 6
第二章 理论计算原理 8
2.1 第一性原理 8
2.2 密度泛函理论 8
2.3 材料模拟软件介绍 9
第三章 理论计算方法 10
3.1 催化剂模型的搭建 10
3.2 计算参数设置 11
3.3 CO2的吸附 12
3.4 几何优化 12
3.5 零点能计算 13
3.6 性质计算 14
第四章 计算结果与分析讨论 15
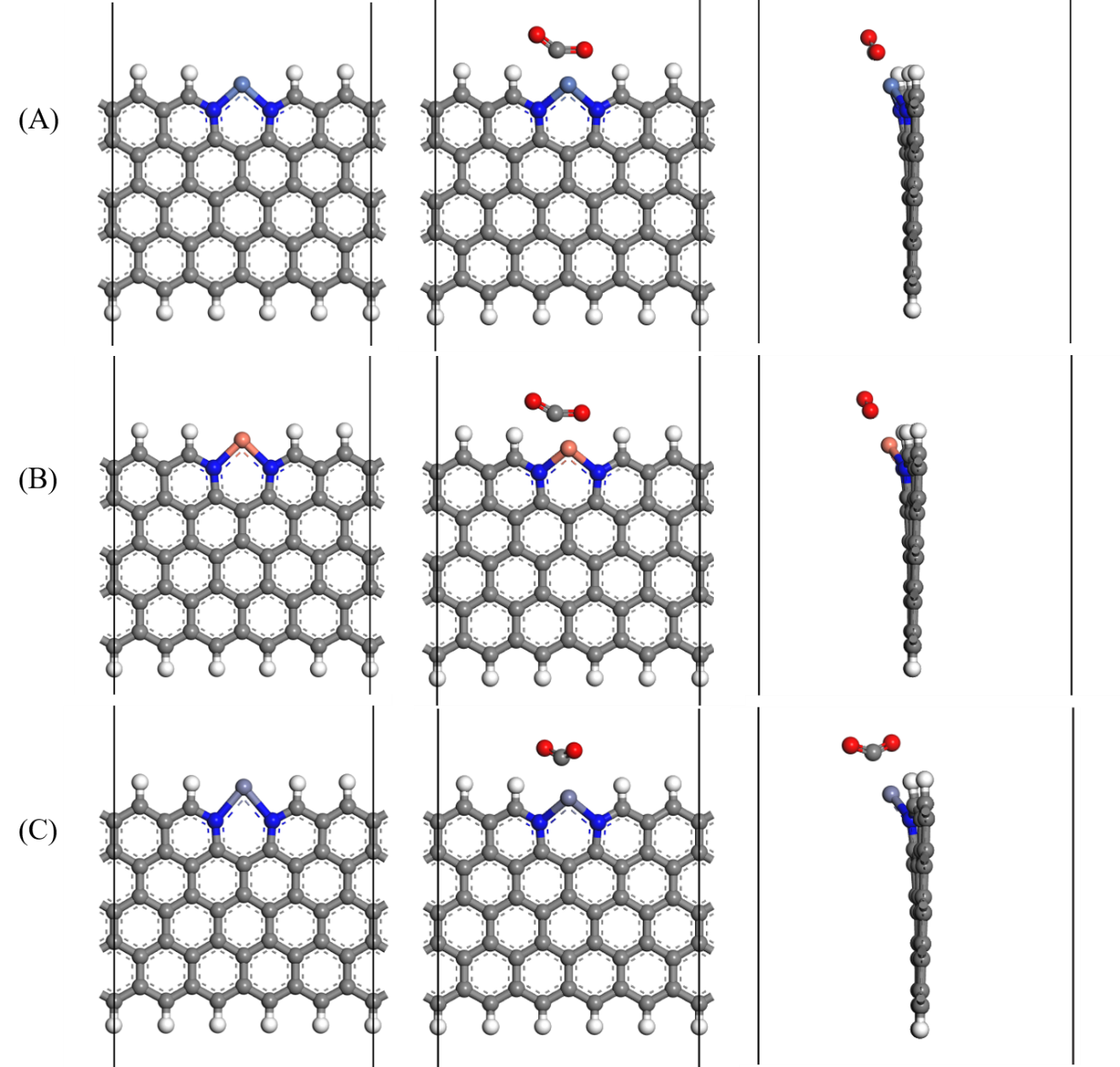
4.1 几何结构变化 15
4.2 电子结构分析 17
4.2.1 过渡金属原子的电荷变化 17
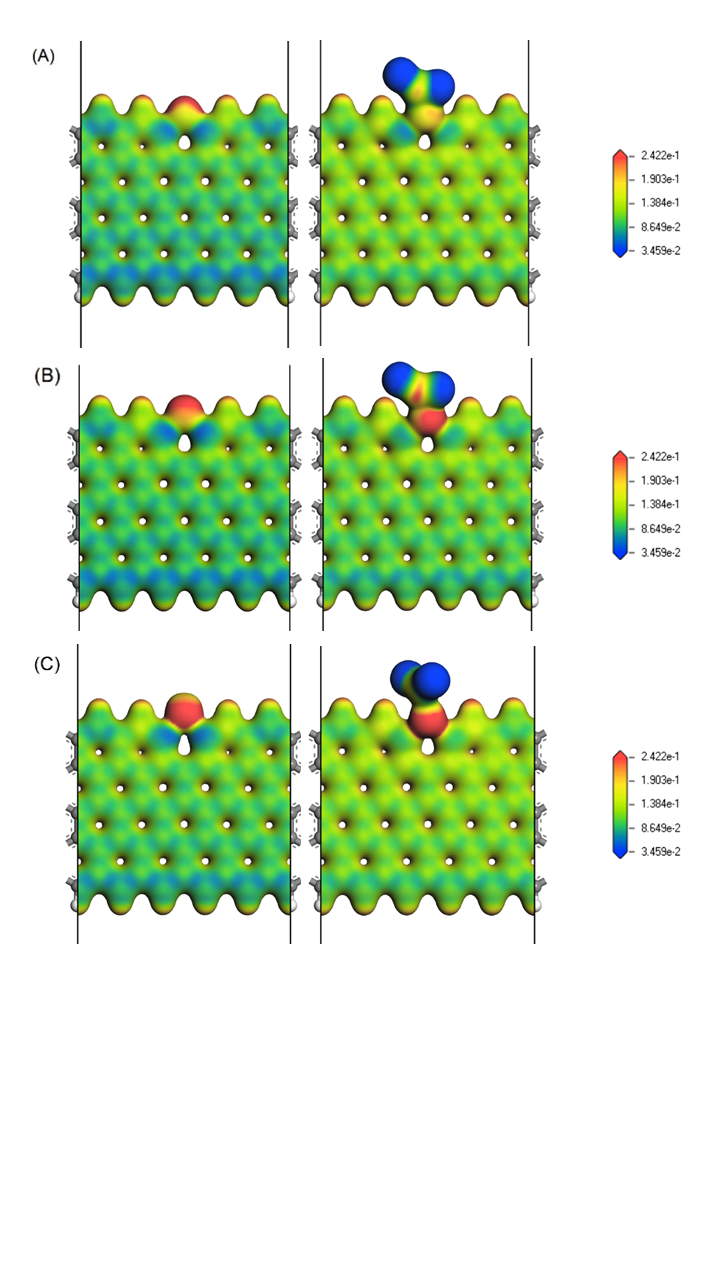
4.2.2 电子密度分析 17
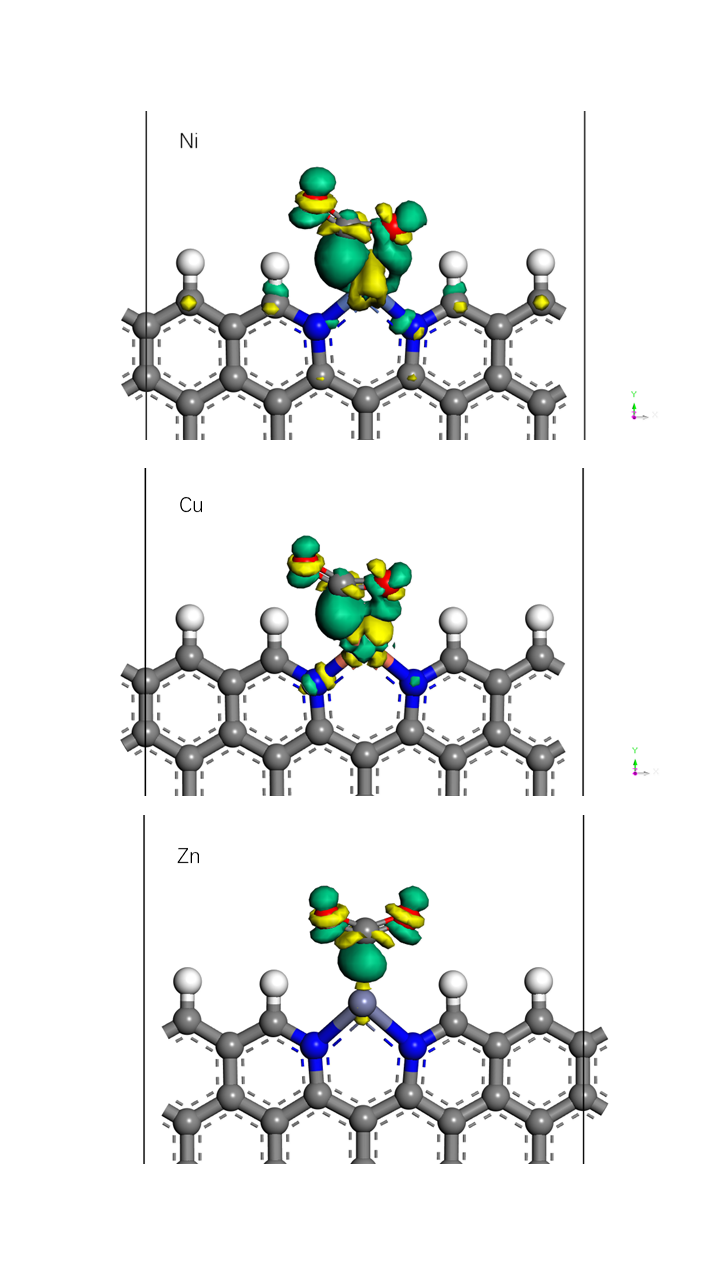
4.2.3 差分电荷密度分析 19
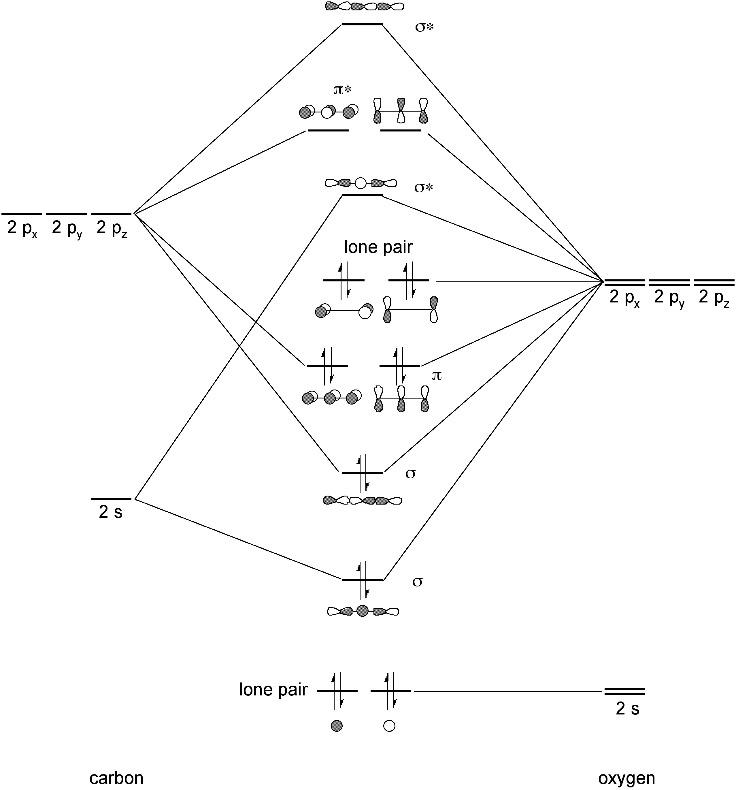
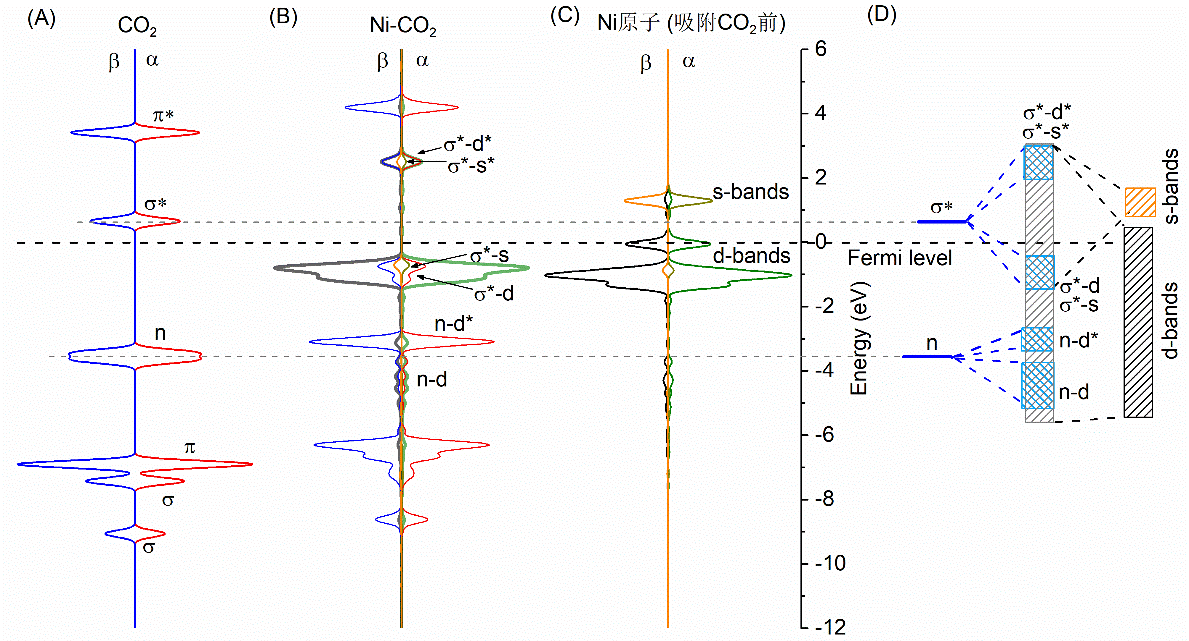
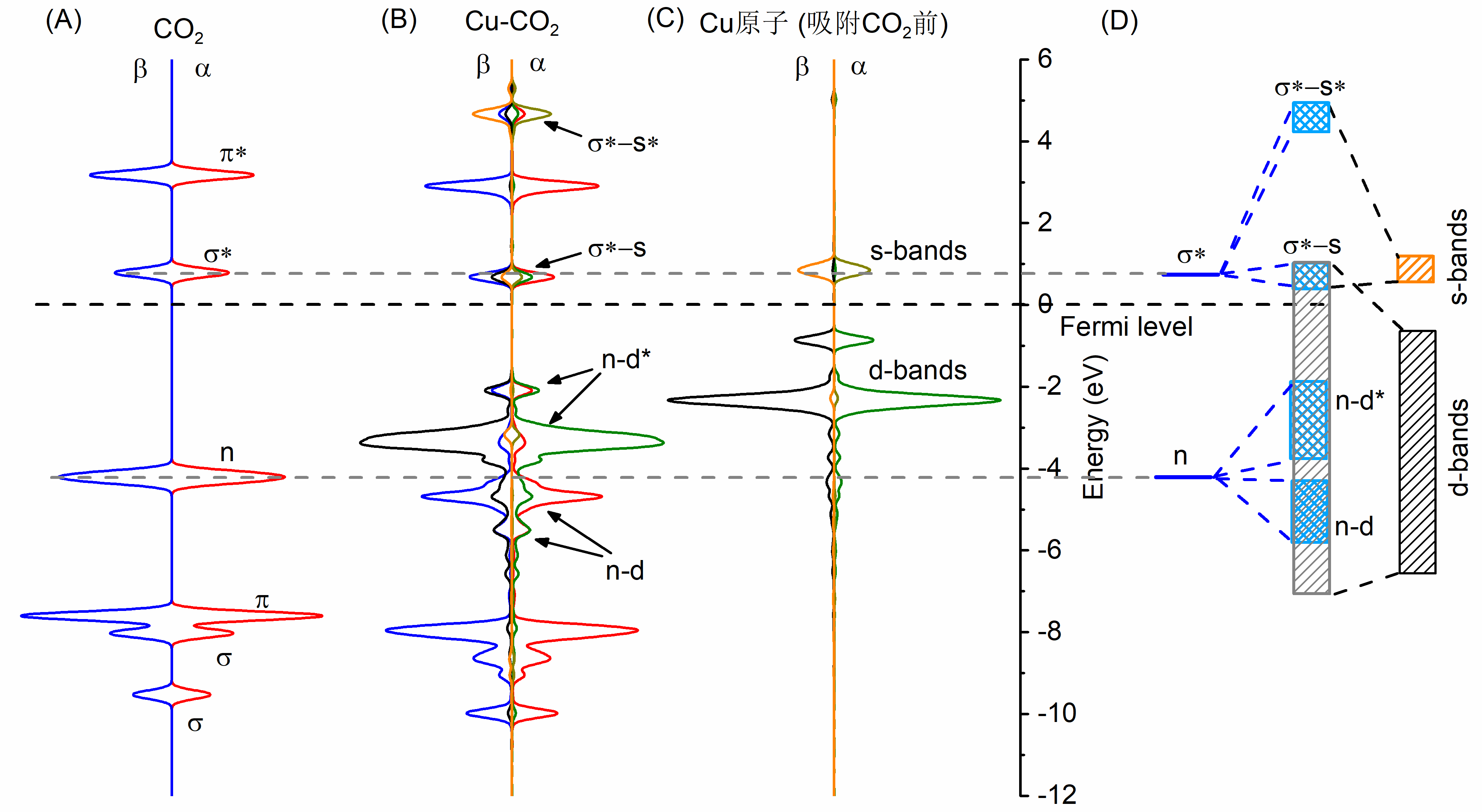
4.2.4 分波态密度分析 (PDOS) 21
4.3 CO2催化性能分析 25
4.3.1 CO2吸附性能分析 25
4.3.2 同种过渡金属掺杂体系对CO2还原的不同路径比较 26
4.3.3 不同过渡金属掺杂体系对相同CO2还原反应路径影响的比较 28
第五章 结论与展望 30
参考文献 32
致谢 34
第一章 绪论
1.1引言
进入21世纪以来,经济飞速发展,人类的生活水平进一步提高,生活方式也在逐步改进。但是当今人类社会仍然面临两大问题与挑战:能源短缺与温室效应[1]。一方面,由于煤炭、石油和天然气等的大量消耗引起了全球范围内的能源短缺问题,亟需寻找和开发新型能源;另一方面,也正是由于化石燃料被更加广泛地使用,大气中的温室气体浓度逐年迅速增加,这已成为威胁全球可持续发展的严峻问题。
温室气体种类主要包括水蒸气 (H2O)、臭氧 (O3)、二氧化碳 (CO2)、甲烷(CH4)、氧化亚氮 (N2O)、全氟碳化物 (PFCs)、氢氟碳化物 (HFCs)、含氯氟烃(HCFCs)、六氟化硫 (SF6) 等。2018年12月5日,荷兰环境评估署 (PBL) 发布的《全球二氧化碳和温室气体排放趋势报告:2018年》(Trends in Global CO2 and Total Greenhouse Gas Emissions: 2018 Report) 显示,2017年全球温室气体排放量正在以1.3%的速度增加,达到了50.9 Gt CO2 eq (十亿吨二氧化碳当量)。2017年的温室气体排放量约比1990年高55%,比2000年高40%。其中,二氧化碳、甲烷、氧化亚氮以及其他温室气体排放量占比分别为77%、15%、6%和2%。二氧化碳排放量增长了52%,占温室气体排放增量的85%。由此可见,CO2是温室气体中最主要的成分 (图1)。并且,CO2作为最简单的C1资源,可加氢合成醇类或其他碳氢化合物,这不仅成为实现二氧化碳循环的重要途径,也成为了未来新能源开发的一个重要方向[2] 。因此,对CO2进行有效回收和利用具有解决能源及环保问题的双重意义。如何有效地将二氧化碳作为原料“变废为宝”成为科学研究的一个热点。本文将着重讨论CO2还原成CO或HCOOH的反应机理。
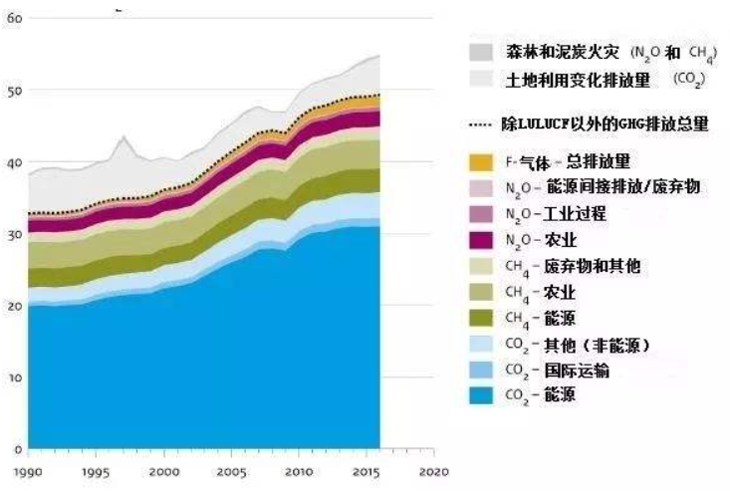
图1.1 温室气体主要成分(来源:和碳视角)
1.2 CO2还原方法
由于目前日渐增多的人类工业生产,过量的碳排放成为了威胁可持续发展的严峻问题,巨量排放的CO2造成了全球气温升高并打破了自然界原有的碳平衡。迄今为止,大气中CO2浓度已经达到400 ppm,相比19世纪末期的280 ppm增长了42.8%。在此背景下,如何降低CO2在大气中的浓度成为了各国科学家的研究重点。科学家们试图以自然界中光合作用为出发点,探索CO2还原方法和机理以实现人工光合作用,从而解决大气中过剩的CO2。
目前还原CO2的主要技术有热化学法,光化学法和电化学法。其中热化学法即在高温高压下对CO2混合气进行还原,目前工业中已成功应用于CO2还原为甲醇 (CH3OH)。至于另外两种方法,由于催化剂的限制,光催化和电催化还原CO2尚处于快速发展阶段,仍有较大的探索空间。
1.2.1 热化学法还原CO2
在高温高压条件下利用还原性气体与CO2进行混合是一种传统的CO2还原法,已在工业中得到多年的应用。比较有代表性的即在非均相催化剂的催化还原下将CO2与H2制成甲醇,这种方法也被叫作直接加氢法。该技术主要是从CO加氢工艺发展而来,具有一定的工业基础[3-4]。目前,通过混合气还原得到甲醇的效率还较低,只有10%左右。为了更加高效的利用原料以减少损耗,通常需要将产物分离以回收未反应的原料,然而这套设备和流程过于复杂,所以寻找合适的催化剂成为了当下的主要难题。
然而,以BASF公司开发的ZnO/Cr2O3催化剂为例,该技术同样还具有反应条件严苛、产物选择性低、反应温度高、反应压力大等明显缺点。只有在反应温度和压力同时达到590 K和25 MPa时,催化剂才能表现出较好的活性,如果采取升温和加压的方式来提高催化活性,则副反应也会不可避免地发生,从而造成甲醇选择性低下。此外,在固体氧化物催化剂上加氢还原CO2更易于得到C1混合物,如CO、CH3OH和CH4等,这也是非均相催化剂存在的问题。因此科研人员在此基础上还开发出了均相催化剂,来提高CO2加氢制甲醇的能源利用率和催化效率。
Sasaki等[5]第一次在CO2加氢还原的反应中使用了贵金属[Ru(CO)12]/KI混合物作为均相催化剂,虽然最终有甲醇产生,但产物选择性仍然较低。Kothandaraman等[6]也同样使用了Ru基均相催化剂来实现CO2还原制备甲醇。到目前为止,通过热化学法还原CO2已经进行了很多研究与实验,工艺也愈见成熟,但催化剂的效率还有待提高,因此催化剂的开发仍是这一技术领域的研究重点。
1.2.2 光催化还原CO2
对于CO2的还原,半导体催化剂是目前最实用以及效率最高的光催化剂[7]。1972年日本科学家Fujishima和Honda两人在一次试验中对放入水中的二氧化钛单结晶进行了紫外光照射,结果发现水被分解成了H2和O2。这一现象被称为“本多·藤岛效应”(Honda-Fujishima Effect)而闻名于世,并且他们在Nature上发表了一篇极具里程碑意义的文章,标志着多相光催化新时代的开始[8]。
半导体光催化剂主要以n型半导体材料为主 (目前使用最广泛的是TiO2),当一定波长的光照射到光催化半导体材料上时,光生载流子会发生分离,光生电子 (e−) 或空穴 (h ) 与分子或离子结合产生具有氧化或还原活性的自由基,这些自由基能够使有机大分子降解为CO2或其他有机小分子。另一方面,CO2和H2O可以与光生电子 (e−)、空穴 (h ) 相互作用,形成碳氢化合物,从而实现CO2的分解和氢气的制备。常见的宽带隙半导体的吸收波长大都集中在紫外区域,只有当入射光光子的能量大于半导体吸收阈值时,半导体价带中的电子才能从价带跃迁至导带,从而产生光生电子 (e−) 和空穴 (h ),使载流子发生运输转移。而未复合的e−和h 对将从半导体晶格转移到表面,依次与表面的电子受主和施主反应[9]。
半导体粉末 (TiO2,SiC,GaP等) 悬浮液被发现可用作光催化剂后,CO2便可在有水且被紫外光的照射下分解为HCOOH,CH3OH,HCHO,CH4等物质。另外,Liu等[10]发现,仅需在373~573 K的低温条件下,CO2在TiO2上即可发生光催化分解。Li等[11]首先采用水热法合成了TiO2纳米管 (TNTs),而后采用沉积法在TNTs表面负载具有异质结构的CdS或Bi2S3,并对获得的光催化剂进行了CO2加氢评价。评价结果表明,使用CdS或Bi2S3修饰后的TNTs在光催化活性、CO2吸附量以及可见光吸收能力等方面均有明显提升,其中Bi2S3/TiO2催化剂表现出最优的催化性能,在可见光照射下,其5小时CH3OH产率为224.6 μmol/g。
经过十几年的探索与努力,国内外均已在利用太阳能光催化降解CO2领域取得了不错的进展,不少优秀的论文也报道了许多高效率、高选择性的光催化剂。但提高CO2的转换效率和选择性以及寻找可见光频段下合适的光催化材料仍是目前的存在的最大问题,如何突破这一限制,是使光催化走向大规模实际应用的关键所在。
1.2.3 电催化还原CO2
电化学催化法相对其他两种方法条件相对简单、无污染,工艺过程所需的电可以直接从太阳能、风能等可再生能源中转化获取,能够实现真正意义上的碳循环利用,并且由于电催化反应系统的紧凑灵活、模块化、易于放大生产从而更具备实用性和潜在的工业价值,因此电催化CO2还原被认为是最具有应用前景的CO2转化技术之一。尽管人们很早就开始了这一领域的研究,但是现有催化材料和反应体系仍然面临反应过电位大、转化效率低、产物选择性不理想等一系列问题。如何寻找到新型高效的催化剂是电催化CO2还原亟需解决的关键科学问题。
近年来,尤其是从2008年开始,各国对于电催化还原CO2的研究热度上升极快。电化学兴起于国外,从上世纪六七十年代开始到现在,研究方法也是多种多样。有研究发现吡啶及其衍生物和巯基蝶啶等N杂环分子对CO2具有一定的催化效果,但是在这种均相体系中存在着一个明显的缺陷,催化剂分子每次都需要加入电解液中,且催化剂分子难以回收。为了解决上述问题,金属有机框架被开发出来,通过诱捕的方法将催化剂分子困在金属框架内,制备成一种复合材料的非均相催化剂,将其做成电极应用于CO2电催化还原,并取得了明显的催化效果[12]。另外,有研究发现杂原子掺杂的石墨烯往往可以获得更佳的电催化活性,其中,N、P、S等原子的掺杂最受关注,这是因为杂原子掺杂可以在石墨烯基表面产生缺陷,从而将完美石墨烯的能带隙被打开,进而提高其电化学的性能。
电化学催化CO2还原可产生CO或HCOOH等燃料或化工产品,但催化剂的选择一直是个问题。Hori在1985年的标志性地发现了Cu具有优于其他催化剂的CO2电催化还原能力,其催化产物为CH4,C2H4等碳氢化合物,并具有较高的法拉第效率[13]。早期工作表明,CO是CO2在Cu上还原过程中形成碳氢化合物的关键中间体。此外CO2还原过程中还会逐渐加氢或脱水,形成HCOOH、HCHO、CH4和C2H4等产物。后续的实验研究发现,电催化还原CO2的产物可达16种之多。虽然反应的产物众多,但Hori及其同事的早期工作也发现了Cu上CO2和CO的还原具有强烈的结构依赖性:甲烷优先在Cu (111) 面上生成,而乙烯则是Cu (100) 面上的主要催化产物。这表明催化剂的表面会对反应产物具有一定的选择性。利用这种选择性,我们可以针对地选择性还原CO2获得特定的产物,从而提高催化反应的法拉第效率。
目前电催化还原CO2存在的挑战是高效催化剂的开发以及催化反应微观机理的研究。根据Sabatier原理(Sabatier principle),催化剂与反应物及反应中间体之间的结合能既不能太大也不能过小。如果结合能太大,则反应物或反应中间体难以脱附,会导致后续反应持续进行,而无法获得预计的产物;如果结合能太小,则反应物或反应中间体难以与催化剂结合,会导致催化反应无法进行。因此,催化剂与反应物或反应中间体之间有合理的结合能是选择性催化的关键因素。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: