非金属掺杂镍基氢氧化物在电催化中的应用毕业论文
2021-12-10 17:48:16
论文总字数:30861字
摘 要
析氧反应 (Oxygen Evolution Reaction, OER) 作为限制电解水过程的关键反应,其非贵金属催化剂的开发成为近几年研究热点。其中镍基金属催化剂由于具有高导电性与亲氧性而吸引了众多科研人员,但对其元素掺杂带来的规律性影响却鲜有人关注。
论文研究了非金属掺杂对于镍基电催化试剂所带来的影响。通过水热法和高温煅烧分别在Ni(OH)2的基础上进行S、P元素掺杂,进而探究其性能变化规律。证明S元素可改变材料组成,进一步掺杂P能降低材料电阻,提升材料电催化活性。
同时为对实验进行拓展,拟探究S、P元素掺杂对多元金属镍基电催化剂带来的影响,将Fe、Al元素引入Ni(OH)2制备多金属镍基材料。其中Fe、Al共同引入的产物表现出最好的性能,其在达到10 mA cm-2电流密度下过电势仅为245 mV,此外,在析氧反应稳定性测试中,Ni2FeAl LDH可以保持约1.5 V 的电压 (相对标准氢电极)长达20 h以上。
实验结果表明,S的引入可以改变Ni(OH)2结构,提升镍基氢氧化物对于析氧反应的电催化能力。而P的进一步掺杂都可以增强这一效应。Fe、Al的引入具有类似的效果,而非金属元素对于多金属镍基催化剂的掺杂效应还需下一步的实验探究说明。
关键词:析氧反应;掺杂;镍基;多金属;电催化试剂
Abstract
Oxygen evolution reaction (OER) is a key reaction restricting the process of electrolyzing water. The development of non-noble metal catalysts has become a research hot spot in recent years. Among them, nickel-based metal catalysts have attracted many researchers due to their high electrical conductivity and oxygen affinity. But little attention has been paid to the regular effects of elemental doping.
The effect of non-metal doping on nickel-based electrocatalytic reagents has been studied. S and P elements were doped on the basis of Ni(OH)2 by hydrothermal method and high-temperature calcination respectively. And the regulation of its properties was explored. We found that S element can change the structure of Ni(OH)2 material. Further doping of P can reduce the resistance of the material and increase the electrocatalytic activity of the material.
In order to expand the experiment, we planned to explore the effect of S and P element doping on the polymetallic electrocatalyst. Fe and Al elements were introduced into Ni(OH)2 to prepare polymetallic Ni based materials. Among them, Fe and Al co-doped products show the best performance. Its overpotential is only 245 mV at a current density of 10 mA cm-2. In addition, in the stability test of oxygen evolution reaction, Ni2FeAl LDH can maintain A voltage of approximately 1.5 V (relative to a standard hydrogen electrode) for more than 20 h.
The experimental results show that the introduction of S can change the structure of Ni(OH)2 and improve the electrocatalytic ability of nickel-based hydroxides for oxygen evolution reaction. Further doping of P can enhance this effect. The introduction of Fe and Al has similar effects. The doping effect of non-metal elements on multi-metal catalysts needs further experimental investigation and explanation.
Key Words:oxygen evolution reaction; doping; nickel-based; polymetal; electrocatalyst
目 录
摘要 I
Abstract II
第1章 绪论 1
1.1 引言 1
1.2 析氧反应机理 1
1.3 析氧反应电催化剂 3
1.3.1镍基氧化物/氢氧化物 5
1.3.2镍基多元金属材料 5
1.3.3非金属掺杂镍基材料 5
1.3.4镍基缺陷/空位材料 6
1.4研究目的的意义和内容 6
第2章 实验材料的制备 8
2.1实验药品 8
2.2 Ni(OH)2的制备 8
2.3硫、磷的元素掺杂 8
2.4多元金属材料制备 9
2.5多元金属材料合成原理 9
第3章 硫、磷掺杂提升析氧性能 10
3.1结构表征 10
3.1.1 XRD测试 10
3.1.2 SEM扫描 11
3.1.3 红外测试 12
3.1.4 拉曼分析 12
3.2性能测试 13
3.2.1 OER测试 14
第4章 多元金属提升析氧性能 16
4.1 结构表征 16
4.1.1 XRD测试 16
4.1.2 SEM扫描 17
4.1.3 红外测试 17
4.1.4 拉曼分析 18
4.2 性能测试 19
4.2.1 OER测试 19
第5章 结果讨论 21
参考文献 22
致 谢 26
第1章 绪论
1.1 引言
由于科技工业的不断发展,现今世界能源消耗问题逐渐引起了人们的注意。虽然人类对于可再生能源的利用有所增加,但煤炭、石油、天然气等传统能源的使用总量却依旧在提升。目前全球40 %左右的电力均来源于碳,传统能源为主导的能源利用现状仍旧止步不前,也意味着世界能源格局并未从根本上进行转变。
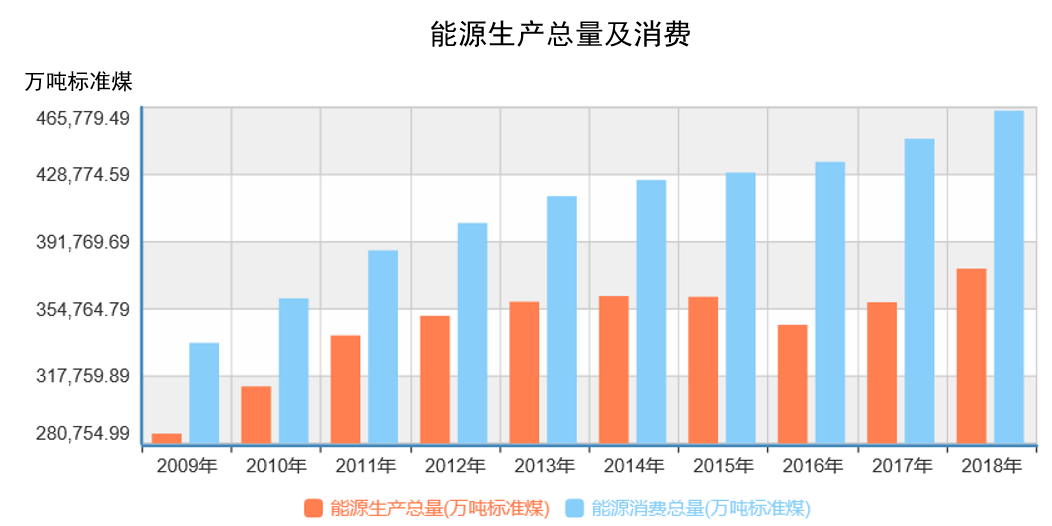
图1.1 2009-2018年全国能源生产总量与消费总量
国际能源署指出,预计到2040年,为实现“巴黎协定”规定的气候目标,全球石油消耗需要减少25 %,而煤炭则达到了50 %。同时要想与核能共同提供全球25 %以上的能源,预计可再生资源的水平需为现在的10倍。为此科研人员们也在努力探索其解决办法,以适应现代人类对于清洁能源的重大需求。
析氧反应(Oxygen Evolution Reaction, OER) 由于在各种能量转换和清洁能源存储技术(如电解水制氢,可再生燃料电池构筑和可充电金属-空气电池设计)中的重要作用,成为近年来引起了极大的研究关注[1]。而设计构筑价格低廉、原料广泛、合成简单的高性能析氧反应催化也至关重要。
1.2 析氧反应机理
析氧反应(Oxygen Evolution Reaction, OER)在电解水、燃料电池以及金属-空气电池中起着重要的作用。作为水电解反应的半反应之一,其与析氢反应 (Hydrogen evolution reaction, HER) 共同构成了电解水反应。
电解水反应式如下:
阴极:2H 2e→H2
阳极:2OH-→O2 H2O 2e
总反应式:H2O→H2 O2
但析氧反应与两电子转移的析氢反应不同,其涉及四电子转移过程,同时反应动力学迟缓,所需过电势相对较高,因此也成为了电解水制氢这一过程的瓶颈[2]。通常实验室析氧反应测试所需电解体系为三电极体系。同时为了提高溶液的电导率,经常选用含有大量可自由移动离子的溶液作为电解质。考虑需要避免由酸性电解质所带来的对电极等的腐蚀损失以及酸性条件下析氧过程动力学极为缓慢的因素,通常选取成本较低的氢氧化钾碱溶液。与我们熟知的只有正负极的二电极体系不同,三电极体系包括工作电极、对电极/辅助电极和参比电极。如果选择二电极体系,则对电极/辅助电极被默认成为参考电极,而在测试中体系中会有电流流过,对电极发生极化,导致电位变化,所测得的工作电极电位也会产生偏差。在三电极体系中,对电极只作为导通电流的电极而存在,工作电极和对电极构成回路,参比电极作为工作电极电势的基准较为稳定,即此时工作电极的电势为相对于参比电极的电势。析氧反应可能的反应机理如下:
* OH- → * OH e-
* OH OH- → * O H2O e-
* O OH- → * OOH e-
* O * O → O2 2 *
或
* OH- → * OH e-
* OH OH- → * O H2O e-
* O OH- → * OOH e-
* OOH OH- → * O2 H2O e-
* O2 → * O2
请支付后下载全文,论文总字数:30861字
相关图片展示: