过渡金属离子掺杂对钴酸钠电化学性能的影响毕业论文
2020-02-19 15:52:22
摘 要
由于经济的飞速发展,对能源的需求不断增加,化石燃料资源储备渐显不足,能源危机愈加严峻。作为传统能源的替代品,太阳能、风能、潮汐能和其他绿色能源技术各有其不足限制了大规模应用,因此对能源储存技术提出要求。其中钠离子电池以丰富的资源和优秀的电化学性能,在近几年受到广泛关注,成为具有巨大潜力的电化学储能选择之一。本课题研究钴酸钠正极材料的掺杂改性以期望获得稳定性更高的钠离子电池。
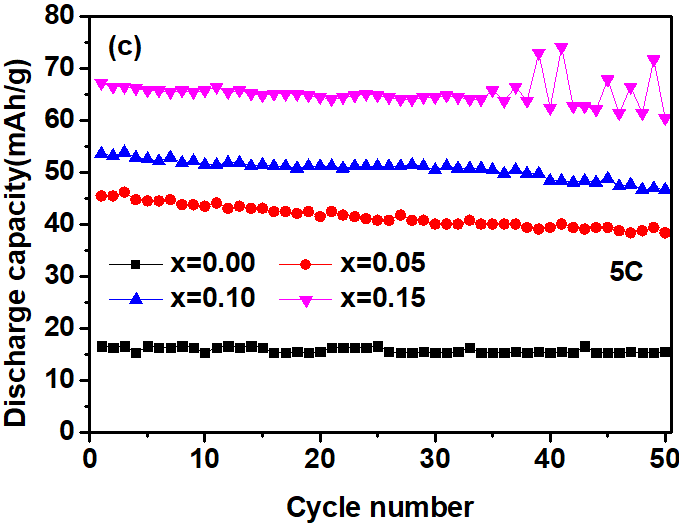
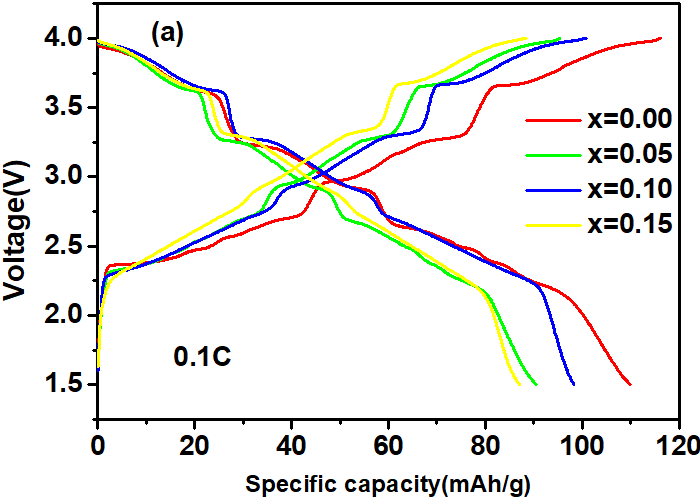
采用高温固相反应法制备了锰元素掺杂的钴酸钠正极Na0.74[Co1-xMnx]02材料,对Na0.74[Co1-xMnx]02正极材料的结构、形貌和电化学性能进行了表征。结果表明,锰元素掺入钴酸钠中,替换钴元素的位置,掺杂量的不同对固相反应开始温度没有明显影响;锰元素掺杂可以提高钴酸钠正极材料的稳定性,但初始比容量会有一定的降低。
关键词:钠离子电池;正极材料;钴酸钠;锰元素掺杂;电化学性能
Abstract
Due to the rapid development of the economy, the demand for energy is increasing, the reserve of fossil fuel resources is becoming insufficient, and the energy crisis is becoming more and more serious. As substitutes for traditional energy sources, solar energy, wind energy, tidal energy and other green energy technologies have their own limitations that limit large-scale applications, which puts demands on energy storage technology. Among them, sodium ion batteries have received extensive attention in recent years due to their abundant resources and excellent electrochemical performance, and have become one of the electrochemical energy storage options with great potential. This study investigated the doping modification of sodium cobaltate cathode materials in order to obtain a sodium ion battery with higher stability.
Mn-doped sodium cobaltate cathode Na0.74[Co1-xMnx]02 was prepared by high temperature solid-state reaction. The characterizations of structure, morphology and electrochemical properties of Na0.74[Co1-xMnx]02 cathode material were carried out. The results show that the Mn is doped into sodium cobaltate, and replaces the position of Co. The difference of doping amount has no significant effect on the onset temperature of solid phase reaction. Mn doping can improve the stability of sodium cobaltate cathode material, but there will be a certain reduction in initial specific capacity.
Key Words:Sodium ion battery;Cathode material;Sodium cobaltate;Mn doping;Electrochemical properties
目 录
第1章 绪 论 1
1.1 钠离子电池 1
1.1.1 钠离子电池简介 1
1.1.2 钠离子电池基本组成 1
1.1.3 钠离子电池工作原理 2
1.2 钴酸钠正极材料 2
1.2.1 层状过渡金属氧化物NaMO2 2
1.2.2 钴酸钠正极材料简介 3
1.3 过渡金属氧化物正极材料研究进展 4
1.3.1 层状正极材料 4
1.3.2 隧道型正极材料 5
1.3.3 过渡金属氧化物材料存在问题及改进方法 5
1.4 选题的目的及意义 6
第2章 实验部分 8
2.1 实验药品与实验仪器 8
2.1.1 实验药品 8
2.1.2 实验仪器与设备 8
2.2 钴酸钠正极材料制备方法 9
2.3 纽扣电池的组装 10
2.4钴酸钠正极材料性能表征 10
2.4.1 X射线衍射分析(XRD) 10
2.4.2 扫描电子显微镜(SEM) 11
2.4.3 热重分析(TG) 11
2.4.4 恒电流充放电测试 11
2.4.5 循环伏安测试(CV)和交流阻抗测试(EIS) 11
第3章 钴酸钠正极材料性能表征 12
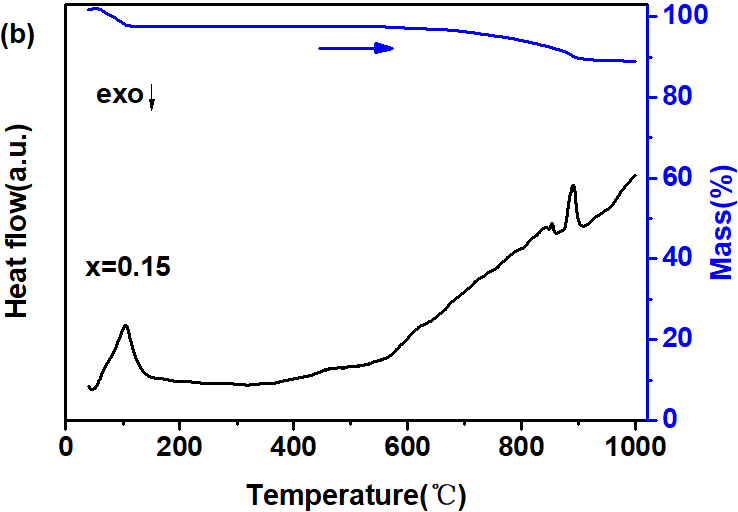
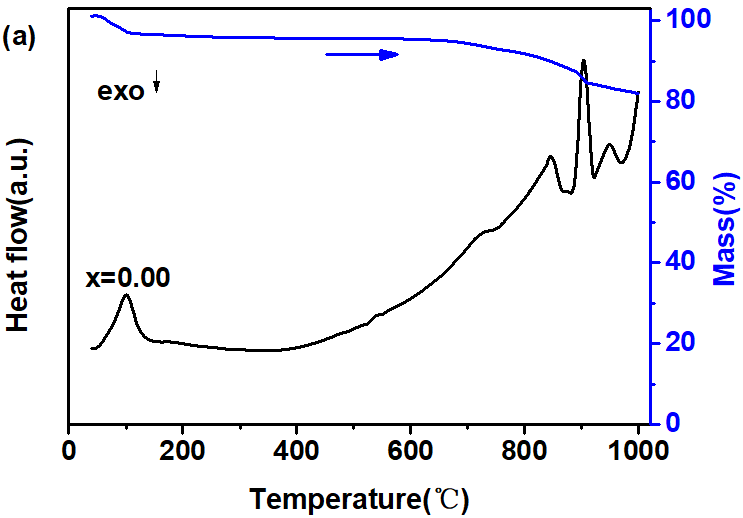
3.1 钴酸钠正极材料制备工艺的热力学探究 12
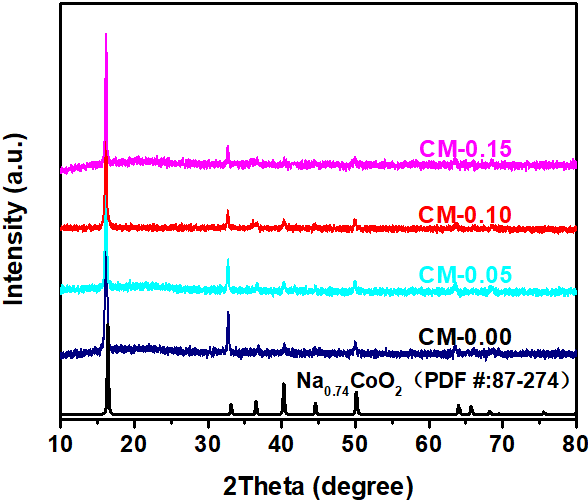
3.2 钴酸钠正极材料的X射线衍射分析(XRD) 13
3.3扫描电镜分析(SEM) 14
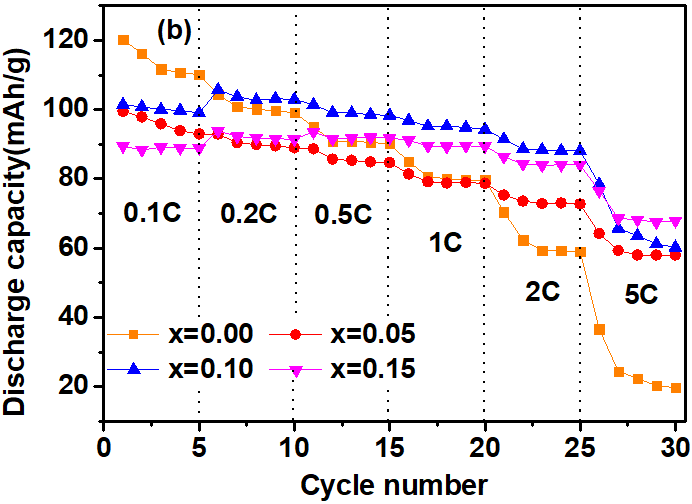
3.4 恒电流充放电测试 14
3.5循环伏安测试 16
3.6 交流阻抗测试 16
第4章 结 论 18
参考文献 19
致 谢 21
附录1 22
附录2 23
第1章 绪 论
本章主要介绍了本课题中的基本概念、理论前提以及发展现状和展望等。
1.1 钠离子电池
1.1.1 钠离子电池简介
钠离子电池实际上是一种浓差电池,正负极由两种不同的钠离子嵌入物质组成,钠离子在两个电极之间往返嵌入和脱嵌以实现能量的储存与释放,也因此被称为“摇椅电池”。钠离子电池具有极大的资源优势。钠元素在地球上分布极为广泛,在地壳中的储存量约为1%,且在海水中含量更丰富。而锂元素在地壳中含量仅为0.0065%,多分布于南美洲,因此锂资源相对昂贵。
钠离子电池具有一些吸引人的特性,例如钠离子电池与锂离子电池充放电原理相似,都是锂离子或钠离子在正、负极之间往返嵌入/脱嵌,形成电流传递能量;丰富的资源储备和较低的材料成本(碳酸钠的成本约195-234美元/吨),因此具有良好的经济效益;低毒性,良好的安全特性;以及标准电位低,在电极的选择上具有非常大的空间。
1.1.2 钠离子电池基本组成
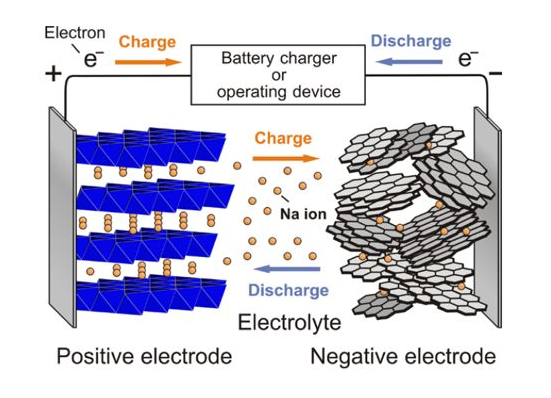 如图1.1所示,钠离子电池主要由四部分组成:正极、负极、电解液、隔膜。正极一般是嵌钠型化合物,由活性物质、粘结剂和导电剂按一定比例组成;负极材料为硬碳材料。正负极材料是钠离子电池核心部分,很大程度上决定了钠离子电池的性能。电解液一般为NaPF6或NaClO4等,而钠离子电池的隔膜则为玻璃纤维。
如图1.1所示,钠离子电池主要由四部分组成:正极、负极、电解液、隔膜。正极一般是嵌钠型化合物,由活性物质、粘结剂和导电剂按一定比例组成;负极材料为硬碳材料。正负极材料是钠离子电池核心部分,很大程度上决定了钠离子电池的性能。电解液一般为NaPF6或NaClO4等,而钠离子电池的隔膜则为玻璃纤维。
图1.1 钠离子电池基本组成
1.1.3 钠离子电池工作原理
钠离子电池通过钠离子在正负极之间反复的嵌入/脱出实现电荷转移和能量传输。充电时,正极发生氧化反应,钠离子从正极脱嵌经过电解液嵌入负极,负极进入富钠态,正极进入贫钠态,同时电子的补偿电荷通过外电路供给到负极,保证正负电极电荷平衡。放电时则相反,钠离子从负极脱嵌,经过电解质嵌入正极,正极处于富钠态,负极处于贫钠态。
例如,在以1mol/L NaClO4/PC为电解液,NaMO2为正极活性材料,硬碳为负极材料的钠离子电池中,其化学反应式可以表示为:
(-)C | 1 mol/L NaClO4/PC | NaMO2( )
正极反应:NaMO2⇌Na1-xMO2 xNa xe-
负极反应:6C nNa xe-⇌NaxC6
电池反应:NaMO2 6C ⇌Na1-xMO2 NaxC6
1.2 钴酸钠正极材料
1.2.1 层状过渡金属氧化物NaMO2
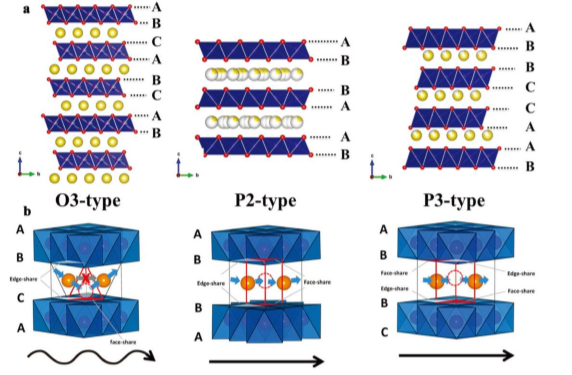 层状过渡氧化物拥有优秀的电化学性能,被广泛应用于正极材料之中。这种金属氧化物可以嵌入/脱出钠离子,成为输送钠离子的载体。但是与锂离子不同,由于钠的离子半径大于锂离子,在层状过渡金属氧化物中钠离子只能占据八面体的位置,而锂离子可以占据四面体和八面体的位置[1]。层状过渡金属氧化物有O2、 O3、P2、P3等类型,其中,O表示钠离子占据八面体中心,P表示
层状过渡氧化物拥有优秀的电化学性能,被广泛应用于正极材料之中。这种金属氧化物可以嵌入/脱出钠离子,成为输送钠离子的载体。但是与锂离子不同,由于钠的离子半径大于锂离子,在层状过渡金属氧化物中钠离子只能占据八面体的位置,而锂离子可以占据四面体和八面体的位置[1]。层状过渡金属氧化物有O2、 O3、P2、P3等类型,其中,O表示钠离子占据八面体中心,P表示
图1.2 (a)为三种晶体结构图 (b)为钠离子电池三种类型的钠离子迁移路径
钠离子占据三棱柱配位体空隙位置,2和3代表过渡金属离子占据不同位置的数目,是由氧离子的堆积方式决定的,2表示氧原子以ABBAABBA…排列,3表示氧原子按ABCABC…排列[2]。三种类型的结构图如图1.2所示。
层状过渡金属氧化物具有较高的理论比容量,但是单金属氧化物MO2(M为Fe、Ni、Co等)通常容易在深度脱钠时造成结构不可逆的变化,只能限制截止电压换取稳定性和循环性能,导致实际的比容量只有100 mAh/g左右[3]。而多金属氧化物可以解决一部分问题。Mn可以提高结构稳定性,Ni可以提高体积能量密度,Co可以提高循环性能。合理的掺杂形成多金属氧化物可以取长补短,弥补不足。
1.2.2 钴酸钠正极材料简介
钴酸钠属于层状过渡金属氧化物,P2型层状过渡金属氧化物相比于O3型具有更好的比容量和循环性能[4]。这是由于:(1)当P2相转变为其他相时,需要有足够的力使M-O键断裂,以使[MO6]八面体旋转,这使得P2相的转变相较于其他相更为困难,因此稳定性较高;(2) P2相金属离子占据的三棱柱空位有更大的层间距,P2相可以容易地掺杂其他过渡金属元素[5],改变其物化性质。
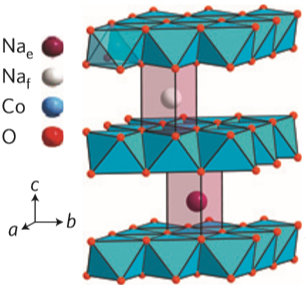 在钴酸钠正极材料中,钴离子占据了[CoO6]八面体中心位置,钠离子占据了三角形棱柱位点,由于P2相以ABBAAB…排列,钠离子在相邻两个层状结构中占据了不同的位置,如图1.3所示 [6]。
在钴酸钠正极材料中,钴离子占据了[CoO6]八面体中心位置,钠离子占据了三角形棱柱位点,由于P2相以ABBAAB…排列,钠离子在相邻两个层状结构中占据了不同的位置,如图1.3所示 [6]。
图1.3 钴酸钠晶体结构
钴酸钠用于电池正极材料具有很多优势,如:电化学性能优秀,首次放电比容量高,放电平稳,循环性能好等;电池性能稳定,一致性好。但也具有一些不足之处,如:反复充放电后会导致活性物质的结构在膨胀和收缩后发生改变,导致钠离子运动阻力增大,容量减少;且相对其他过渡金属,钴元素价格比较昂贵,资源不够丰富。关于电化学性能方面的不足之处我们可以通过改性方法使其得到改善,以有更大的应用空间。
1.3 过渡金属氧化物正极材料研究进展
1.3.1 层状正极材料
层状正极材料主要介绍O3型和P2型两种类型材料。
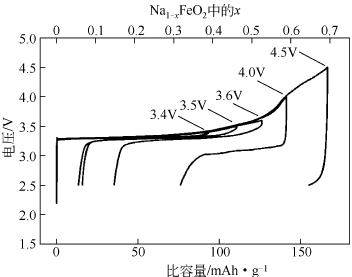 (1) α-NaFeO2是一种典型的O3型正极材料,可以通过固相反应制备。在各个不同的截止电压下,单相α-NaFeO2 材料的比容量如图1.4所示。随着电压的不断升高,导致晶格中的钠离子的脱出数量逐渐提高,使该类正极材料所释放的容量能够不断提高,但是材料的循环稳定性能也随之降低。Komaba等人为了解决这个问题,他们用 LiCoxFe1-xO2正极材料模型阐述了该类材料中钠离子的嵌入/脱出机理,解释其在高充电电压下材料稳定性降低的原因:当晶格中的钠离子脱出后,会导致四面体空隙在共边的 [FeO6]八面体内产生,若从能量角度上分析,在四面体空隙中的三价铁离子更加稳定,这会导致三价铁离子容易迁移至共面点。每当充电电压逐渐升高时,四面体空隙上铁离子更容易影响到钠离子的固态扩散,因此使得该类正极材料在放电这一过程中的容量逐渐降低。并且由图1.4可以得到,虽然其比容量较小,但是考虑到该类材料在充放电过程中只有非常小的极化,所以该材料仍然具有较大潜力[7]。
(1) α-NaFeO2是一种典型的O3型正极材料,可以通过固相反应制备。在各个不同的截止电压下,单相α-NaFeO2 材料的比容量如图1.4所示。随着电压的不断升高,导致晶格中的钠离子的脱出数量逐渐提高,使该类正极材料所释放的容量能够不断提高,但是材料的循环稳定性能也随之降低。Komaba等人为了解决这个问题,他们用 LiCoxFe1-xO2正极材料模型阐述了该类材料中钠离子的嵌入/脱出机理,解释其在高充电电压下材料稳定性降低的原因:当晶格中的钠离子脱出后,会导致四面体空隙在共边的 [FeO6]八面体内产生,若从能量角度上分析,在四面体空隙中的三价铁离子更加稳定,这会导致三价铁离子容易迁移至共面点。每当充电电压逐渐升高时,四面体空隙上铁离子更容易影响到钠离子的固态扩散,因此使得该类正极材料在放电这一过程中的容量逐渐降低。并且由图1.4可以得到,虽然其比容量较小,但是考虑到该类材料在充放电过程中只有非常小的极化,所以该材料仍然具有较大潜力[7]。
图1.4 NaFeO2正极材料在不同截止电压下比容量-电压曲线
(2) P2型层状金属氧化物的[MO6]八面体结构以ABBAABA…的形式排列堆积,钠离子位于MO2层间的三棱柱位点上,最小重复单元层数为两层。P2类正极材料的可逆容量大于其它类型的材料,据猜想是由于不同的MO2层之间Na 可以进行传递造成的。由于P2 结构中存在钠离子扩散通道,因此在 P2 型材料中Na 扩散时有较 O3 相更低的能垒,Na 从一个三棱柱位点迁移至毗邻的位置时经过4个氧原子的矩形狭通道,因此氧原子的斥力对其影响就更小。所以,Na 在嵌入/脱出时受到更小的阻力,因此可能具有更大的比容量[8]。
1.3.2 隧道型正极材料
Morcrette等人制备出一类具有较大的S形孔道结构的正极材料Na0.44MnO2,该材料具有较好的电化学性能,该材料具有130mAh/g左右的初始比容量,且在0.50C倍率条件下进行100次充放电后其仍有75%的比容量。然而由于该类材料的循环性能较差,能够可逆循环的钠离子最多只有0.22mol,因此其容量问题制约其在钠离子电池中的广泛应用。然而该类正极材料可以应用于水系钠离子电池中,可以降低电池成本和解决环境污染等问题[9]。
1.3.3 过渡金属氧化物材料存在问题及改进方法
虽然在电化学性能方面具有很大的优势,但过渡金属氧化物材料都存在一些相似的问题:(1)随着充放电的进行,内部结构会不断地收缩和膨胀,加速其结构的坍塌,导致比容量缩减;(2)由于钠离子的半径较大,钠离子的扩散较慢,会导致倍率性能较差;(3)过渡金属氧化物的合成方法也会对正极材料有一定的影响,不同的合成方法合成的材料在性能方面有很大的差别。
掺杂是过渡金属氧化物材料的众多改性方法中的一类常用手段。譬如在正极材料中掺杂Ti元素,可以使其在充放电过程中结构更加稳定,从而减少由于材料的结构坍塌导致的不可逆容量。陈明哲等人研究制备了一种缺钠O3型层状结构过渡金属氧化物Na0.8Ni0.4-xCo2xTi0.6-xO2,这种材料的比容量比较小,然而其循环稳定性能优秀,在0.10C倍率条件下进行90次充放电后容量保持仍能保持95%。因此Ti元素虽然不会使容量增加,但在钠离子迁移过程中可以起到稳定结构的作用[10]。
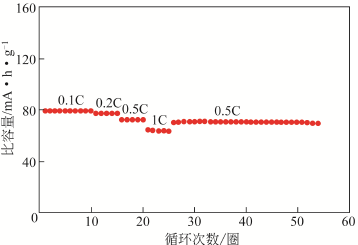
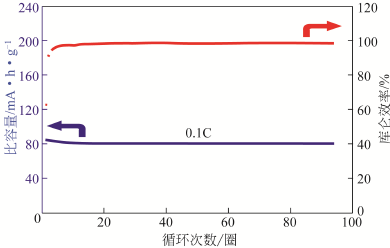
图1.5 缺钠型Na0.8Ni0.4-xCo2xTi0.6-xO2倍率循环曲线以及长循环曲线
其他掺杂如Ni和Cr等元素可以利用其较多价态的变化使材料的比容量提高,掺杂Fe元素有利于材料导电性能的提高,而掺杂Mn元素有利于材料稳定性的提高。
层状过渡金属氧化物的合成方法对其电化学性能也有一定的影响,因此可以调整合成方法来改善材料的性能。例如,Shaijumon 等人制备了P2结构材料Na0.5Ni0.25Mn0.75O2,从图1.6可以看出,该类材料具有比较高的比容量,在1.50-4.40V电压区间内在0.10C倍率条件下充放电循环时的可逆容量为210mAh/g,循环50圈后仍保持有大约80%的比容量[11]。
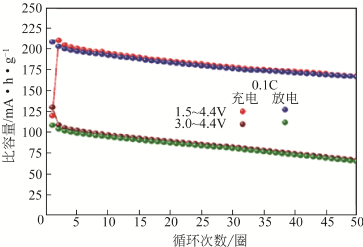
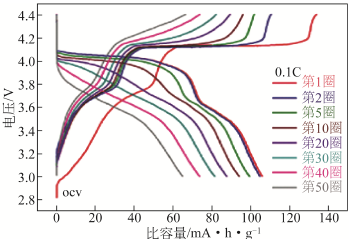
图1.6 Na0.5Ni0.25Mn0.75O2的比容量电压曲线以及在不同电压区间的循环倍率性能。
1.4 选题的目的及意义
如今,化石能源仍然是维持现代社会的最主要的能源,清洁能源如风能、太阳能、地热能、等虽有快速发展,但因为受大自然环境影响大,有很多的不稳定性,而核能因为会排放放射性核废料,以及潜在的风险,容易受到政治及舆论影响,大规模应用难以实现。而对化石能源过度的消耗,以及对清洁、资源广泛的能源的迫切需求,使研究人员对新能源的开发抱有极大的热忱。其中,最为简便、高效的二次电池展示了广阔的应用前景和潜在的经济效益[12]。锂离子电池从40年前开发以来,经过多年的科学研究和升级换代,已经成为现代社会不可或缺的能源存储设备。锂电池具有工作电压高、循环性能好、比容量大等优点,广泛应用于各种新能源汽车以及便携式移动设备,甚至航空航天等高科技领域中。然而,随着社会的快速发展,对能源的需求量不断扩张,锂离子电池逐渐暴露出锂资源相对不足和价格比较昂贵且不断上涨等问题,开发廉价高效的新型储能设备迫在眉睫。在其他众多不同的电池中,钠离子电池在近几年受到广泛关注,成为具有巨大潜力的电化学储能选择之一[13]。
钠离子电池具有很多显而易见的优势,首先,钠元素和锂元素同属ⅠA族,物理化学性质相似,且钠离子电池与锂离子电池结构和充放电原理相似,都是锂离子或钠离子在正、负极之间往返嵌入/脱嵌,形成电流传递能量,因此可以类比比较成熟的锂离子电池来对钠离子电池进行研究,缩短研究时间及成本;其次,钠离子电池相比于其他电池有较高的比容量和较快的充放电过程;以及钠元素在地球上储量极大,是世界上第四大广泛的元素,这使价格低廉的钠离子储能设备在大规模应用方面成为了可能。但是由于钠离子质量大于锂离子,使钠离子电池的能量密度小于锂离子电池,因此钠离子电池体积相对较大,不适于轻便的设备,而钠离子大的离子半径和体积,使钠离子在充放电的脱嵌过程中,更易造成层状通道的坍塌,因而其稳定性和循环性能等相比于锂离子电池还有所欠缺,因此研究能量密度高、稳定性好的钠离子电池是研究的关键。
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: