ZnFe2O4CdS磁性复合材料的制备与性能研究毕业论文
2020-05-12 22:13:42
摘 要
最近几年来,半导体光催化技术作为新能源的发掘和环境治理的一种有效的途径受到了越来越普遍的关注。ZnFe2O4/CdS复合材料作为一种复合型可见光响应半导体催化剂,具有较高的研究价值和应用前景。
本文采用水热法合成 ZnFe2O4/CdS,通过改变 ZnFe2O4和 CdS的比例,研究了其对 ZnFe2O4/CdS光催化性能的影响,并得出产氢最优的条件。本文通过X射线衍射仪(XRD)、X射线光电子能谱分析(XPS)、透射电子显微镜(TEM、扫描电子显微镜(SEM))等仪器对制备的样品的晶体结构、表面形貌、可见光吸收等性能进行了表征。得出的了产氢性能最优的比例为ZnFe2O4/CdS=1:4,异质结的形成促使了复合体系产氢性能远远优于 ZnFe2O4或 CdS单组份催化剂。
关键词:光催化 异质结 可见光 产氢
ABSTRACT
In recent years,the semiconductor photocatalysis technology is an effective way of new energy development govenance,which has concerned more and more attention.As a visible light responsive semiconductor catalyst,ZnFe2O4/CdS has high value and application prospect.
In this study,hydrothemal method is used to synthesize ZnFe2O4/CdS.By changing the ratio of the ZnFe2O4 and CdS ,these variables are studied on ZnFe2O4/CdS photocatalytic performance.As a result,we could get the best factor of the hydrogen production.In this paper,by means of X ray diffraction (XRD),scanning electron microscopy (SEM),transmission electron microscopy (TEM),and X ray photoelectron spectroscopy(XPS) on samples,the crystal structure,surface morphology optical absorption properties were characterized.Getting the best factor of the hydrogen production is the ZnFe2O4/CdS=1:4.Forming the heterojunction make that ZnFe2O4/CdS photocatalytic performance is better than ZnFe2O4 or CdS catalyst.
Keywords: Photocatalysis;Heterojunction; Visible light; Hydrogen production
目 录
摘 要 I
ABSTRACT II
第一章 绪论 1
1.1 研究的背景及意义 1
1.2 光催化原理 1
1.2.1 光催化的基本原理 1
1.2.2 影响光催化剂的因素 2
1.3 光催化剂的制备与改性方法 3
1.3.1 光催化剂的制备方法 3
1.3.2 光催化剂的改性方法 4
1.4 本课题研究的主要内容 9
第二章 实验部分 11
2.1 试剂与药品 11
2.2 实验仪器与设备 11
2.3 样品的制备 12
2.3.1 ZnFe2O4-CdS磁性复合材料的制备 12
2.3.2 CdS纳米棒的制备 12
2.4 实验测试方法 13
2.4.1 物相分析(XRD) 13
2.4.2 形貌分析(SEM、HRTEM) 13
2.4.3 XPS, PL测试 14
第三章 结果与讨论 16
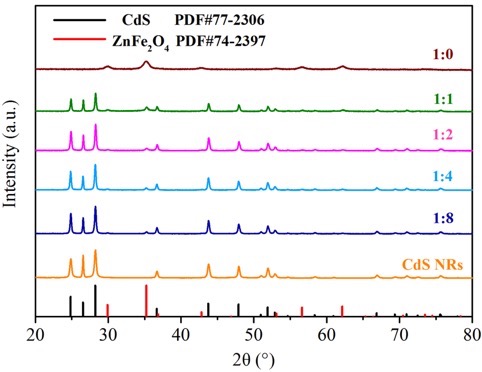
3.1 XRD分析 16
3.2 SEMamp;TEM分析 16
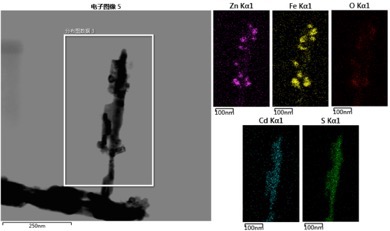
3.3 ZnFe2O4/CdS的元素分布图 17
3.4 磁性特征 19
3.5 不同配比的 ZnFe2O4/CdS产氢性能和产氢量 20
3.6 不同配比的 ZnFe2O4/CdS紫外可见光谱吸收光谱 17
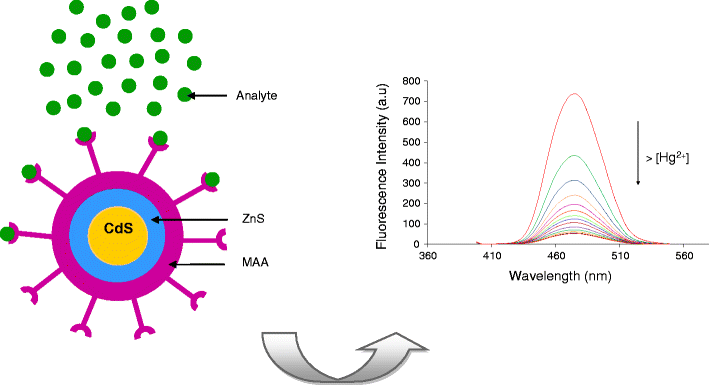
3.7 不同配比的 ZnFe2O4/CdS荧光图谱 22
第四章 结论 23
4.1 结论 23
4.2 展望................................................................................................................................28
参考文献 24
致谢 26
第一章 绪论
1.1 研究的背景及意义
首先,21世纪全世界面对的能源危机和环境污染问题各位都耳熟能详了,所以未来的发展中,能源是必不可少,并且是清洁能源。氢能作为一种二次能源,它具有诸多优点。例如:可靠安全、清洁无污染、可方便贮存运输等众多优点。因此人们认可它是新时代的一种最理想的绿色能源。因此它受到了各国的高度重视。光催化材料又称为光触媒。他是使用半导体材料作为光催化剂,在光照的驱动下进行的催化的一种新兴技术。光解水制氢技术始自1972年,由日本东京大学 Fujishima A和 Honda K两位教授首次报告发现 TiO2单晶电极光催化分解水从而产生氢气这一现象[1],从而使大家了解到利用太阳能来分解水产生氢气的可能性,为我们开辟了光解水产生氢气的研究道路。随着电极电解水向半导体光解水产氢的多相光催化(heterogeneous photocatalysis)的转变和不断发现 TiO2以外的光催化剂,对光解水产氢的研究正在逐步发展,并在光催化剂的改性、利用效率、合成等方面取得了很大发展。
1.2 光催化原理
1.2.1 光催化的基本原理
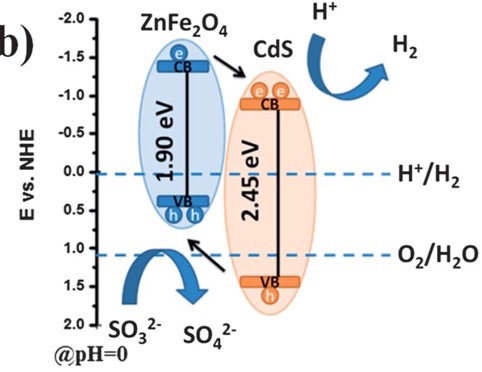
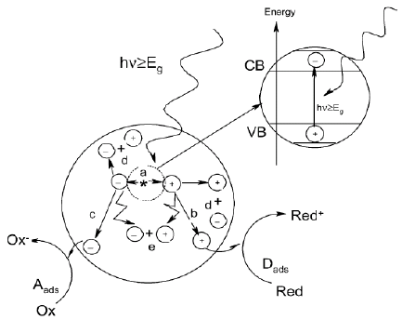
在很大程度上,半导体材料的光催化特性取决于它的能带结构。根据固体能带理论可知,半导体的能带是不连续的。低能价带(valence band, VB)充满电子和空的或不满的高能导带(conduction band, CB),他们之间存在着禁带,他的大小称为禁带宽度,又称为带隙(Eg)。要使水分解生产氢气,在热力学上,需要氢电极电位EH /H2要比作为光催化材料的半导体材料的导带电位稍稍正一些,而氧电极电位 EO2/H2O应该比价带电位稍负。光解水的原理:当光照射在半导体上,照射的能量大于等于半导体的禁带宽度的时候,半导体内电子会因此受到激发而从价带跃迁到导带,而空穴仍然留在价带,使得电子和空穴分离,然后分别在半导体的各个位置将水氧化成氧气或者水还原成氢气。一般来说,半导体光催化反应过程分别有以下几个步骤:(1)产生光生电子-空穴对(fs);(2)载流子在颗粒的内部重新结合后释放热量;(3)载流子转移到颗粒表面并且被捕获(10 ns~100 ps);(4)被捕获的载流子和自由的载流子重新结合(10 ns~100 ps);(5)界面间电荷转移,并发生氧化-还原反应(100 ns~100 ms)。[2]具体的光催化反应过程如图1-1所示[3],其中a代表电子-空穴对的产生;b代表光生空穴在半导体表面作氧化电子的供体;c代表光生电子在半导体表面作还原电子的接受体;d代表电子空穴对在表面的复合;e代表电子-空穴对在内部的复合。
相关图片展示: