电化学处理废水: 选择性的重金属去除过程外文翻译资料
2023-01-03 12:25:18
电化学处理废水:
选择性的重金属去除过程
Thien-Khanh Tran a,b, Kuo-Feng Chiu b, Chiu-Yue Lin c, Hoang-Jyh Leu c,*
a Faculty of Applied Sciences, Ton Duc Thang University, 19 Nguyen Huu Tho Street, Tan Phong Ward, District 7, Ho Chi Minh City 70000, Viet Nam
b Department of Material Science and Engineering, Feng Chia University, Taichung City 407, Taiwan
c Green Energy Technology Research Group, Ton Duc Thang University, 19 Nguyen Huu Tho Street,
Tan Phong Ward, District 7, Ho Chi Minh City 70000, Viet Nam
摘要:电化学过程被认为是一种非常有效的工业废水处理方法,尤其是去除重金属离子。在本研究中,我们想要提供一种不仅能有效处理重金属,并且在这个过程中有一个显著的选择性的方法。一个电化学池,阴极布满导电碳布,阳极为铂涂层钛板阳极(5times;5cm),低压供电能量为10v,pH值为6.8,设计为去除铜,而处理后的镍则含有硫酸镍和硫酸铜(0.06M)。
关键词:电化学过程;微分脉冲伏安法;循环伏安法
为了提高电极的导电性和耐用性,在电极上做了修改,这两个因素可能会直接影响整个过程的效率。我们的研究结果表明,在20h的工作时间内,该方法具有较高的去除效率(>97%),具有良好的应用前景。结合去程过程,电极材料的性质也得到了较好的研究。由于导电碳纤维体现了它的优越性,电化学池在此项研究中成为了一个多功能系统。以这种方式,我们提供了一种不仅能处理废水并且可以产生氢气和氧气等能源的系统,以氢氧根的形式收集重金属,并且可以很容易地改进成一个更高效、适应更大应用范围的连续过程。
此外,本研究还对电极排列的影响进行了细致的研究和揭示。它的特性,提供了将该方法应用于实际工业用途的机会。对于近、中、远三种不同距离的两个点击的排列方式,其重金属的去除效果是不同的(97、96.5和71%)。在这个过程中出现的技术问题似乎是次要的,可以通过一个简单的解决方案迅速解决,这将在后面的部分中描述。然而,我们在这里介绍的一种有效的废水处理方法只是一个开始。我们欢迎探讨可以长时间使用、效果更佳,并且能够产生相当数量的能量的操作系统。
引言
重金属造成的水污染是一个全球性的问题,并且应该受到全世界的关注。自20世纪末以来,由于公众希望生产洁净、无色、澄清、无味、无臭,并且不含其它有害重金属离子的水,废水处理成为了一个需要关注的关键任务。含有重金属离子的水需进行妥善处理,否则会对环境造成严重破坏,如对人类和其他生物的健康造成长期影响[1]。
近年来,作为一种资源集约型和成熟的工业废水处理技术,电化学过程引起了许多关注。相比其他方法,电化学系统具有几个优势[2],例如能在环境温度和压力下操作,并且具有良好的性能和容纳量以适应于进水成分和流量的变化。该方法本身被认为能够降解大范围的污染物,包括耐火材料、羧酸[3,4]和全氟羧酸[5,6]。电化学过程的本质是电力的应用,即在一个同样布有一个阴极管和一个不溶性阳极管的水性金属轴承中通过电流。该处理是使重金属在弱酸液或含氢氧化物的中性电解质中沉淀。如此一来,电极材料的选择就不仅仅只是提供特定的应用方式,并且在提高该方法针对各种被污染的化合物的熟练程度上也具有重要意义。此外,处理后的出水水质取决于产生的离子或荷电载荷的数量、产生的电流及反应的时间[7],因此该过程中任何对电荷量产生影响的因素也可能会对该过程最终的效率造成影响。
导电炭布被广泛用作高分子复合材料中的加固材料,在所有加固纤维中提供一个更强的强度系数和模量[8-11]。因此,使用导电碳布作为电化学过程中的电极去仔细研究其性能会非常有趣。在这项研究中,电化学方法以一个高选择性被用于处理含重金属的溶液,这是依次去除废水中铜和镍的结果。此外,我们还指出了去除过程的反应表现及其在电极性能间的关系——电荷负载。
实验部分
电化学电池是用导电碳设计的,阴极布有碳布,阳极为铂涂层钛阳极,用于在20h内处理500mL含有0.06M硫酸铜和0.06M硫酸镍的溶液。实验装置如图1所示。
图1 电化学电池原理图
所有的实验都在室温、常压下进行,溶液的初始pH为6.6,供应能量为10伏特电流,不添加NaCl等助剂。在这个过程中,由于半电池反应,在阴极和阳极分别会产生氢气和氧气。这些生成的气体将大部分产生的污泥推动到液相表面,然而其余残留在液相中的气体则会由于阴极的还原反应而被其聚集。此外,生成的气体被分开收集和测量(可用一个小的注射器来取出被测气体);这些气体可以存储并且之后可以用于不同用途。在这个过程中气体的产生使得这个系统变得多功能性,使之不仅可以被用于处理废水,并且可以被用于生产氢气和氧气等绿色能源。之后,收集到的气体被分开测量,结果显示含有62%的氢气和34%的氧气。
生成的污泥是一个需要谨慎处理的问题;虽然,电化学过程和与其相似的化学沉淀过程相比,产生较少的副产品。在一段反应时间后,液相表面的污染物被收集起来,同时阴极表面的重金属也同样被收集起来,使得导电碳布阴极在解构之前可以多次使用。
为了提高该过程的效率,我们采用了可以增加电导率和耐久性的导电碳墨水溶液的阴极材料。在实验结束后,将会根据差分脉冲伏安法测量结果(DPV),循环伏安法(CV)和能量分散x射线能谱(EDS)给出该电极的性能及其比较。根据它们之间的距离有三种不同的电机设置,即近距离(2cm)、中等距离(5cm)、远距离(10cm)。不同的电极设置会影响过程中的电荷量和最后的去除效率。在20h的处理过程中,采样时间分别为0 h、10 h和20 h用于监测溶液中的金属离子浓度以及测量阴极处收集的重金属。
表1 原始溶液(处理前)的细节:
结果与讨论
去除过程的机理:
在本实验中,使用硫酸铜和硫酸镍溶液作为整个过程的电解液。当电流通过后,发生以下反应:
CuSO4→Cu2- SO42- (1)
NiSO4→Ni2- SO42- (2)
阴极的反应为:
Cu2 (aq) 2e-→Cu (s) E0= 0.340V (3)
Ni2 (aq) 2e-→Ni (s) E0 =-0.257V (4)
由于反应在阴极产生氢气:
3H2O 3e-→2H2 (g) 3OH- (5)
具有较高还原电位的元素有获得电子然后被氧化还原过程消耗的趋势。因为
还原电位较高,铜会比镍先在溶液中去除。随着反应的进行,几分钟后可以在阴极和阳极收集到氢气和氧气。
在本实验中,镀铂钛板阳极体现了其优越性。它不仅提供了较好的电导率,
也表现出了其优秀的耐久性。显然,无须担心电极会被破坏或者电化学性能会降低,我们可以长时间地进行实验。不同于传统的电化学过程,铂不参与还原反应(这需要一个非常大的电流来减少铂),因此,在阳极发生的反应是一个简单的水电解过程。
阳极的反应为:
2H2O (aq)→O2 (g) 4H (aq) 4e- (6)
因此,保持并提高阴极的质量是唯一重要的任务。Naohide [12], Kobya[13]
和Kashefialasl[14]等之前的研究结果表明电流密度决定凝固剂的用量和气泡的产生率,不仅如此,还会影响电极上溶液的混合和传质。在这种情况下,电荷量是影响整个过程效率的主要因素,而电荷量本身受到阴极和阳极反应的影响,阴极和阳极的反应则取决于电极的性能[15]。因此,在这种情况下,任何一个可以扩展阴极还原反应的改进都可以考虑作为一个替代因素。
电极材料的影响
我们设计了一个布有导电炭布阴极和铂涂层钛板阳极的电化学反应池,用于处理含重金属的溶液。虽然铂涂层材料体现了其作为阳极材料的优越性,导电炭布似乎需要更多的关注。为了提高阴极的性能,我们在其表面涂上了一层导电碳墨。碳材料的应用是建立在它的双层电容机制的基础上的[16-18]。它通过可逆吸附离子的方式储存电荷,与进入稳定且具有较大比表面积的活性材料的离子进行电化学反应[19]。
导电碳布的多孔结构能够促进电解质在电极材料中的扩散,也为离子交换提供更多的通道。碳墨水溶液也提高了碳布中碳纤维管之间的连接。图2显示了循环伏安法测量涂层导电碳纤维布阴极电导率的结果并附一张展示涂层材料表面的SEM照片。
图2 CV测量描述涂层导电碳纤维布阴极的电导率和扫描电镜显示阴极涂层表面的电导率
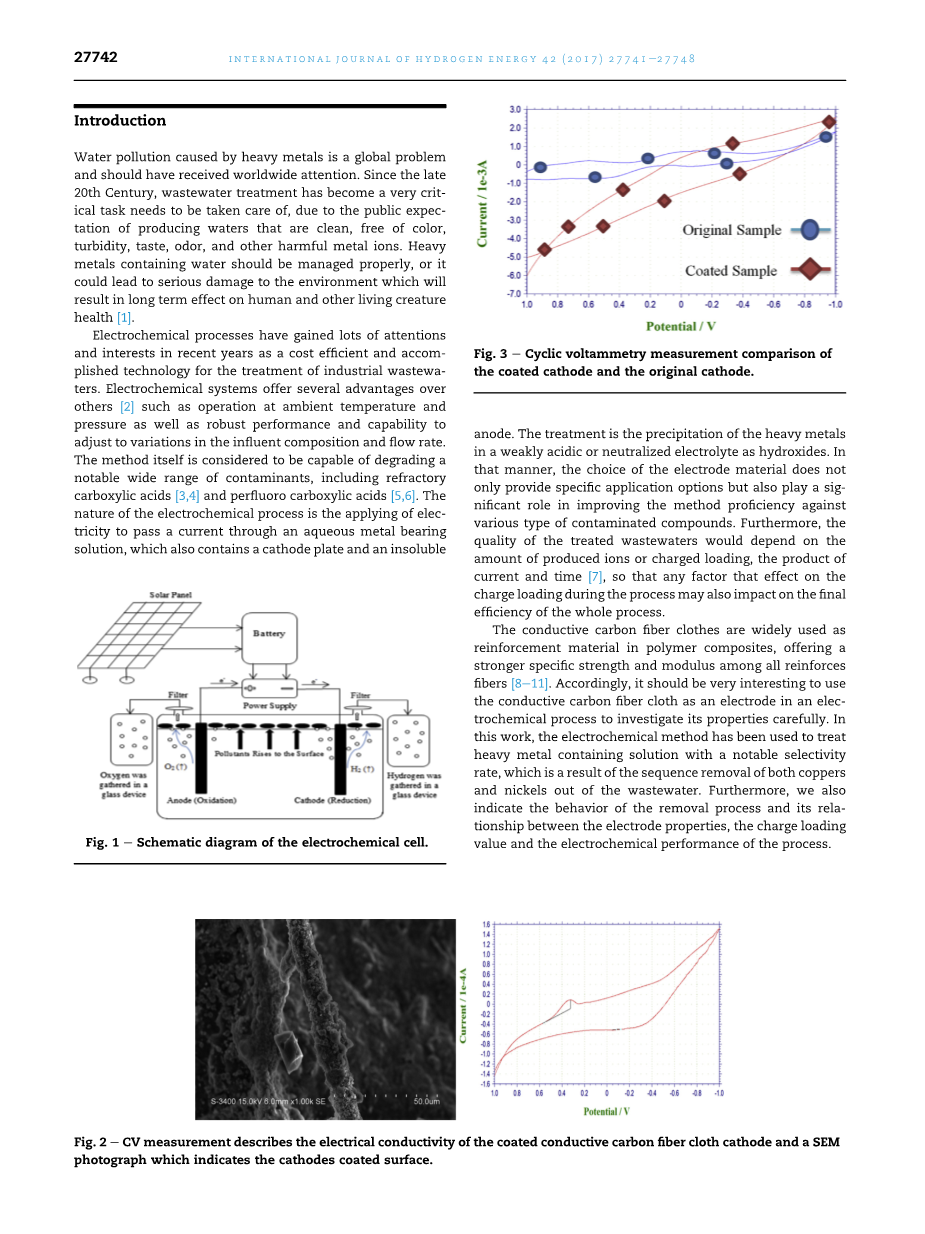
在这个过程中,与原来的相比,涂层阴极体现出了更好的电化学性能和耐久性。这两种阴极性能的比较基于它们的耐久性和电导率。图3为涂层导电碳纤维布阴极和原来的阴极的循环伏安法测量结果。
图3 涂层阴极和原阴极的循环伏安测量比较
显而易见,涂层样品是一种更先进的材料,它提供了一个更大的电导率范围。不仅如此,涂层导电碳纤维布阴极样品被强化的碳墨层紧密填充,以任意的方式在宏观上形成一个为电解质提供更好的可及性的结构,如图4展示的SEM照片。
图4 (a)涂层导电碳纤维布阴极和(b)原导电碳布阴极的SEM图像
选择碳墨溶液作为增强材料是有原因的。然而,提供一种坚固耐用、低成本、可以重复使用几次的材料的设想已经实现。事实表明,对材料进行适当的表面处理,增强其亲水性,是涂层样品性能优于原样品的原因。涂层导电碳层的厚度可以通过浸没时间和电镀液的浓度来调节。
电极排列的影响
本研究使用总量为500Ml,含有0.06M硫酸铜和0.06M硫酸镍的重金属溶液。
因此,总固体重金属含量应为3.9 g(2g铜和1.9 g镍)。表1列出了溶液处理前的详细情况,在使用前混合物被仔细制成并存储了24h。微分脉冲伏安法(DPV)用于研究经10h和20h处理后的重金属浓度,而采用分散x射线光谱学(EDS)测量由于阴极还原反应而在涂层碳布表面收集到的重金属。
在这个过程中,在符合两个阳极排列的相似条件下进行。样品在10h和20h
后提取,用于研究湿法处理重金属的浓度和收集到的固体含量。溶液中重金属含量的减少可以通过分析DVP结果得出。伏安法理论指出DVP结果中的单峰标志着元素的含量和种类。基于这个理论,可以揭示从DVP测量得出的单峰值之间的关系,并且反应时间也应该被用来描述溶液中重金属浓度的降低。单峰取决于它的高度,并且可以通过测量与预期峰值与背景值之间的距离轻易地计算得到。图5将以远距离电极排列展示如何在10小时后使用DPV结果获得峰高。
图5 经10h处理后样品峰值信号的DPV测量结果
正如图5所示,预期值与背景值之间的距离代表了该峰所代表的元素的浓度。因此,
a1,a2,a3,a4显然代表了原始溶液中(a1)铜的浓度,处理液中(a2)的浓度,原始溶液中(a3)镍的浓度,处理液中(a4)镍的浓度。从DPV测量结果只能得出溶液中重金属浓度的变化,但无法显示哪种金属先被处理。因此,附上被收集到的金属的EDS结果,用来显示去除过程中铜
剩余内容已隐藏,支付完成后下载完整资料

英语原文共 8 页,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[282017],资料为PDF文档或Word文档,PDF文档可免费转换为Word




