基于金属-有机骨架混合基质膜的涡流辅助膜萃取技术在尿液雌激素分析中的开发与应用外文翻译资料
2023-09-05 10:00:17

英语原文共 39 页,剩余内容已隐藏,支付完成后下载完整资料
基于金属-有机骨架混合基质膜的涡流辅助膜萃取技术在尿液雌激素分析中的开发与应用
摘要:首次提出了一种基于几种金属-有机骨架混合基质膜(MOF-MMMs)的涡流辅助膜萃取(VA-ME)方法,并将其应用于人体尿液中4种雌激素的分析。通过在聚偏二氟乙烯基体中嵌入MOFs,制备了MOF负载较高(~67 wt%)的MOF-MMMs。该方法适用于多种MOF材料,所合成的MOFs保持了其独特的性能。作为模型分析物,这些雌激素吸附在涡流搅拌的样品溶液中的MOFs上,然后在甲醇中解吸,用高效液相色谱法进行荧光检测分析。MIL-53(Al)-MMM的性能和耐久性特别值得注意,因此选择从儿童的尿液和绝经后妇女中提取雌激素酮,17beta;-雌二醇,雌三醇,炔雌醇。优化了各种提取条件,分析方法在0.02 - 200ng mL-1的线性范围内显示良好,从80.4%恢复到102.7% (RSDle;11.4%)以及低检测限为(0.005-1 ng mL-1 )。VA-ME是一种简单,准确,经济有效的预处理方法,其吸附性能好,操作简单,能从溶液中直接去除分离等优点突出了其在水样预处理中的广泛应用。
关键词 涡流辅助膜萃取 混合基质膜 金属有机骨架 雌激素 人类的尿液
1.简介
金属有机骨架(MOFs)是一类具有较大表面积和可控孔隙率的多孔晶体材料,由于其在储气[1],分离[2],催化[3]方面的应用而得到广泛研究。在分析化学领域,MOFs在采样[4,5],样品制备[6,7],分析物分离[8]和检测[9]方面具有广阔的应用前景。对于所有这些应用,MOFs可以直接使用,也可以在额外处理后使用,如颗粒上的MOF生长[10-13],整体结构[14-18]或固相微萃取纤维[19,20]或MOF磁化[21,22]。MOFs也可以通过不同的方法加入到膜中。关于混合基质膜(MMMs)的研究大多集中于其在气体分离[24-26]和分子尺寸选择性过滤[27]中的应用。然而,MMMs对于提高MOFs的可加工性和处理能力,以及执行液相分离或萃取也很有价值。最近,在聚偏二氟乙烯(PVDF)基质中夹带高负荷的分散良好的MOF晶体,用于制备功能性膜。该方法在MOF含量较高(~ 67 wt%)的MMM中成功地集成了MOF粒子,使用了广泛的MOFs;值得注意的是,合成的MMMs被证明是可伸缩的,它们可以很容易地处理和操作。此外,这些MMMs中的MOFs保持了它们的高结晶性,多孔性,结构和高比表面积[28]。这些金属-有机骨架混合基质膜(MOF-MMM)已被用于分子大小选择性过滤[28],并被开发为支持取代酚的固相萃取(SPE)[29]。但是,上述两种方法都将MMM的应用局限于MOFS的过滤,然而吸附能力并没有完全发挥作用。如果将这个自由的MOF-MMM直接放在涡流搅拌的样品溶液中,可以获得与分散微固相萃取同样高萃取效率。进一步说,由于MOF-MMM很容易从液相中分离出来,因此可以减少离心产生的能量消耗和材料损失。此外,它操作简单,不需要特殊设备。在此基础上,开发了一种新型的涡流辅助膜萃取技术(VA-ME)。该方法将MOF-MMM直接放入液体样品中,在涡流作用下自由翻滚,完成提取。然后将MOF-MMM移出并置于合适的溶剂中进行解吸。这个方法是类似于由Hian Kee Lee在2006年开发的著名的多孔膜保护微固相萃取(mu;- SPE)方法[30]并且将其广泛用于样品制备[31]。与mu;- SPE方法相比,VA-ME中的MOF-MMM可以分批制备,减少了要一个接一个的装入材料薄膜包膜的需要,节省了准备时间。此外,MOFs在MOF-MMM可以直接与样品中的目标物接触,避免了聚丙烯膜的阻碍,促进了目标物的吸附和解吸。这些优点对液相中微量物质如尿液中雌激素的富集十分有利。
众所周知,雌激素在人类发展的不同阶段发挥着重要作用。虽然青春期前的儿童雌激素水平较低,但它们对儿童的生长发育仍是至关重要的。由于代谢或过量摄入,儿童雌激素水平的增加可能导致女孩性早熟和男孩的女性化。对于绝经后女性,雌激素水平较低,其紊乱可能与乳腺癌的发生有关[32,33]。由于与血液样本相比,绝经后女性的尿样更容易获得,且无损伤,所以我们选取了儿童和绝经后妇女的尿液作为样本。因此,本研究开发了一种基于MOF-MMMs的新型VA-ME,为儿童和绝经后妇女尿液样本中微量雌激素的提取提供了机会。在数千MOFs中,根据上述方法,选择NH2-MIL-53(Al),MIL-53(Al),MIL-53(Fe),MIL-100(Fe),MIL-101(Cr),UiO-66(Zr)等几种水稳定的MOFS来制备MOF-MMMs, 并对其提取能力进行了研究,筛选出最适合的吸附剂。在MOF-MMMs基础上的VA-ME方法是从儿童和绝经后妇女尿液中提取4种雌激素(即雌激素酮,17beta;- 雌二醇,雌三醇,炔雌醇),并且其通过常用的高性能液相色谱荧光检测(HPLC-FLD)进行分析。
- 实验
2.1 化学品和试剂
雌激素标准(纯度ge;98%),其包括雌激素酮(E1),17beta;-雌二醇(E2),雌三醇(E3)和炔雌醇(EE2),购自Aladdin Chemistry Co.,Ltd(中国上海)。其化学结构如图1所示。制备这四种雌激素的储备溶液的甲醇以1mg mL-1在4℃下储存。对苯二甲酸(H2BDC),2-氨基对苯二甲酸(NH2- H2BDC),氯化铁(FeCl3·6H2O),非水合物硝酸铝(Al(NO3)3·9H2O)和氢氟酸(HF)为Sinopharm Chemical Reagent Co.,Ltd(中国上海)生产。盐酸(HCl),氢氧化钠(NaOH),氯化钠(NaCl)均购自Damao Chemical Reagent Factory(中国天津)。上述试剂均为分析级试剂。采用HPLC级甲醇,乙腈,二甲基甲酰胺(DMF)和乙醇来自禹王集团(中国山东)。采用自动再蒸馏的方法获得了超纯水水系统。聚偏二氟乙烯(PVDF)是从当地一家五金店购买。
2.2 仪表
采用X Pert Pro衍射仪(PANalytical,Netherlands)进行X射线衍射(XRD)测量。MOFS和MIL-53(Al)-MMM的扫描电子显微镜(SEM)图像记录在Shimadzu SSX-550仪器(日本京都)上。在SEM测量中,样品被固定在双面胶带上,然后用SBC-12自动精密涂布机(KYKY)涂铂30秒。氮的物理吸附等温线是在SA-3100表面积和孔隙分析仪(Beckman Coulter,美国)上测量的。进行色谱分离和测定雌激素在Shimadzu LC-20A(Shimadzu,日本)进行的,其配备一个荧光检测器(FLD-20A)以及使用Diamonsil C18分析柱(150mmtimes;4.6mm i.d,5micro;m)来自Dikma(中国北京)。采用MDS-8G微波装置(上海中诺微波化学技术有限公司)合成了MIL-53(Al)。用于制备样品的附加设备如下:XW-80A旋涡混合器(Sartorius, 德国哥廷根)和PHS - 3CF pH计(中国上海电子科技有限公司)。
2.3 MOFS的合成
NH2-MIL-53(Al)是由Ahnfeldt等人报道的水热法合成的。将Al(NO3)3 ·9H 2O(4.63g)和NH2- H2BDC (2.75 g)与超纯水(30 mL)混合,然后将所得混合物转移到聚四氟乙烯内衬的高压釜反应器中。然后,Teflon-lined bomb被密封,放入烤箱,并在150℃下保持 5 h。获得的黄色结晶粉末通过用DMF和乙醇洗涤以及离心收集在4000 rpm 下保持5min而得以进一步纯化。这个过程重复三次以除去NH2-MIL-53(Al)的未反应物质,以及将残余物在120℃下真空抽空12h。
根据Millangeetal.[35]合成了MIL-53(Fe)。FeCl3·6H2O (1 mmol) ,H2BDC (1 mmol),HF (1 mmol)与DMF (5 mL)在聚四氟乙烯内衬不锈钢高压釜中混合。混合物被密封并在150℃下加热3天。然后将密封的高压釜冷却到室温。用乙醇和水冲洗得到的黄色粉末。最后,粉末分散在水中自然干燥。
用于微波合成MIL-53(Al)的工程中,将3.25g Al(NO3)3·9H2O和1.44 g H2BDC溶解在高压釜中Teflon衬里的25mL水中。反应在微波炉(300 W)210℃下进行90分钟。合成水晶产物被离心分离,然后用DMF和乙醇清洗三次。在进一步的实验之前,在300℃ 空气中下加热2 h以除去未反应的HBDC。
UiO-66(Zr)是在原方法[36]的基础上合成的。ZrCl4 (0.318g)和H2BDC (0.204g)与40mLDMF混合。涡流混合后10分钟后,然后放入Teflon-lined钢制高压釜中,在120℃下反应24h。将高压釜冷却至室温下,获得的产物用DMF洗涤三次,然后浸入用乙醇过夜用乙醇代替空腔中的DMF分子。随后,混合物以4000rpm离心10分钟。最后,UiO-66(Zr)是通过在200°C在空气中干燥2 h获得的。
我们之前合成了MIL-100(Fe)和MIL-101(Cr),并在实验室[37]中进行了表征。
2.4 MOF-MMMs的合成
MOF-MMMs采用之前说的方法制备。在一个典型的配方中,将150mg的干MOF粉末分散在5mL丙酮中,同时用超声法处理30min。然后将PVDF溶液(1.0 g,7.5 wt% in DMF)加入到MOF悬浮液中,使MOF: PVDF比为2:1 (w/w)。将MOF/PVDF复合悬浮液进行超声处理在超声波浴中保持30分钟,然后用旋转蒸发法去除丙酮,得到MOF和PVDF在DMF中的MOFlsquo;inkrsquo;。取其0.2 g定量均匀涂在玻璃基板(尺寸:2.0cmtimes;1.0cm),就像薄层板的制备。然后涂膜加热去除溶剂(在设定为70℃的等温烘箱中1h)。将独立薄膜浸入甲醇中,使其与玻璃基板脱层,在空气中干燥,每片MOF-MMM的质量为 ~0.032 g。由于油墨质量相同,玻璃衬底尺寸相同,得到的每个MOF-MMM的厚度基本相同。根据MOFs的颜色和产品的柔韧性,MOF-MMMs的颜色有所不同(图2a - 2f)。另外,用同样的方法制备无MOF的“空白”膜,即在无MOF情况下将5mL丙酮与1.0 g PVDF溶液直接混合,以下操作与MOF-MMM的制备相同。
2.5 色谱条件
采用Shimadzu LC-20A荧光检测仪进行HPLC分析。当优化色谱条件时,分离过程进行了使用Diamonsil C18分析柱(150mmtimes;4.6mm i.d.,5 mu;m)。水(A)和乙腈(B)作为流动相:0-3 min,25-60% B;3-8min,60% B;8 - 10min,60 - 25%B。注射量为20mu;L。总流动相的流速保持在1.0mL min-1,柱温维持在30℃。对E3、E2、EE2、E1进行监测,荧光检测固定在280 nm的激发波长和发射波长310 nm处。
2.6 样品收集
早上的尿液样本由25名健康儿童和19名绝经后妇女提供。过滤尿液样品,然后在使用前储存在-20℃下,无需任何进一步处理。
2.7涡流辅助膜提取程序
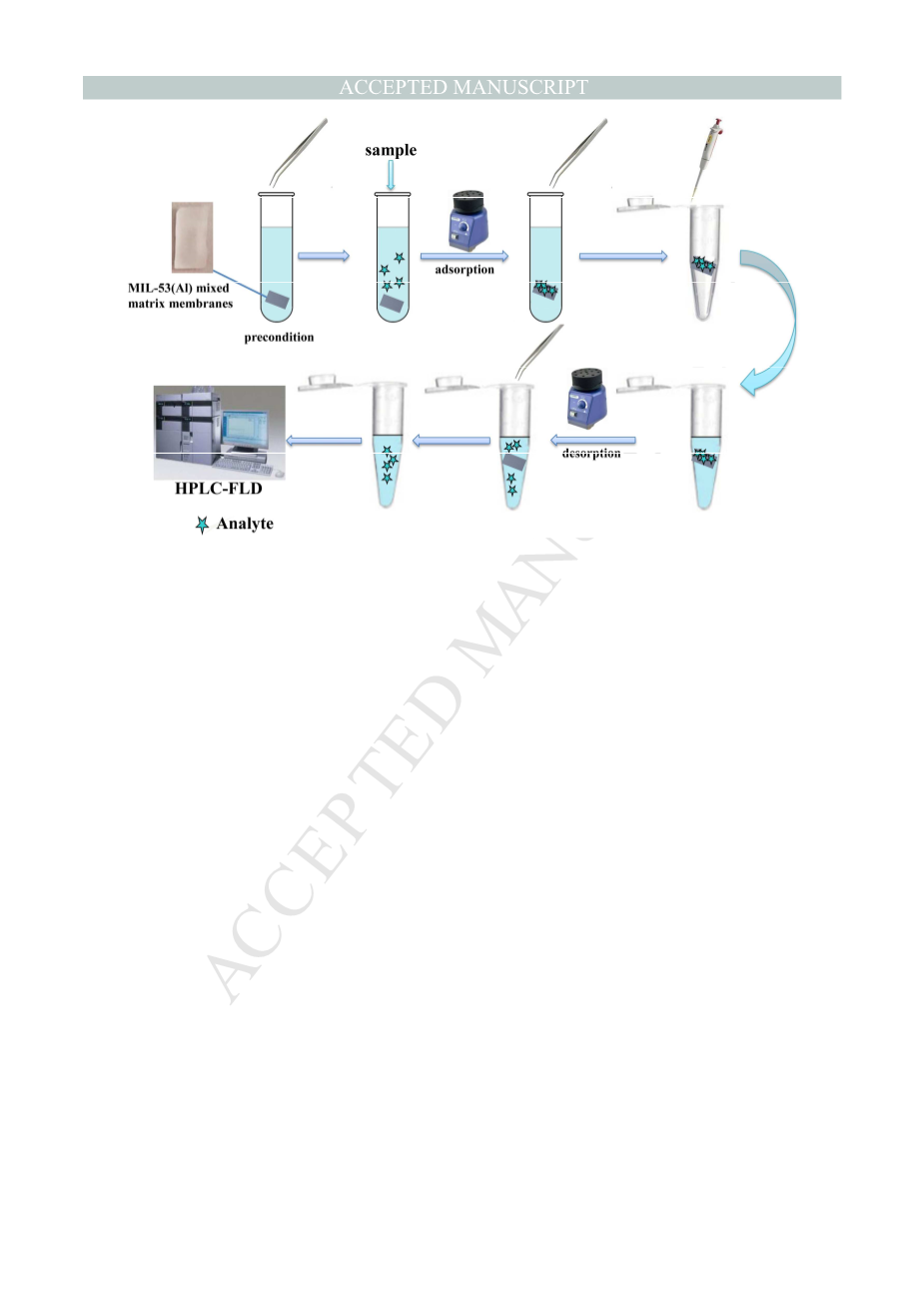
该方法的一个关键步骤是,在使用前,每个MOF-MMM都要通过甲醇和水的连续涡流进行预先调节,每次1分钟。每次提取时,将MOF-MMM置于20 mL制备好的样品(pH 4.0)中,涡流30 min。提取过程中MOF-MMMs 在尿液样品中自由翻滚。提取后取出MOF-MMMs,用镊子夹入2mL离心管(Eppendorf管)中,滤纸干燥。通过在1mL甲醇中涡旋15分钟使分析物解吸。随后,通过一个0.22micro;m有机膜过滤后移除MOF-MMMs以及20micro;L洗脱液被注入到高效液相色谱系统。提取过程如图3所示。
3.结果与讨论
3.1 MOF的表征
采用XRD、SEM和N2吸附等温线对微波合成的NH2-MIL-53(Al),MIL-53(Fe),MIL-53(Al),UiO-66(Zr)进行了表征(图1-图4)。合成的MOFs的XRD图谱和SEM图像与之前报道的一致[34- 36,38],说明合成程序是成功的。表面NH-MIL-53(Al),MIL-53(Fe),MIL-53(Al)和UiO-66(Zr)的区域相应的N2吸附等温线分别为733msup2; g -1,10.3msup2; g-1,1015msup2; g-1和669msup2; g-1。显然,MIL-53 (Fe)的表面积比MIL-53 (Al)的表面积要小得多,虽然两者都表现出呼吸特性,即在引入简单客体分子时,都可以可逆的扩张/收缩其单位细胞体积。这可能是因为MIL-53(Fe)的孔隙在表面积测量条件下可以完全封闭,这意味着它不允许氮进入材料的孔隙,因此表现为无孔材料。相反,MIL-53(Al)呈现完整的结构开口形式,导致表面
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[608808],资料为PDF文档或Word文档,PDF文档可免费转换为Word




