FeC微电解协同降解对硝基苯酚毕业论文
2020-04-19 21:22:49
摘 要
采用铁碳微电解法对硝基苯类废水进行还原性的考察研究,以对硝基苯酚的还原率以及对氨基苯酚的生成率作为评价指标,通过单因素实验方法采用铁碳微电解协同降解对硝基苯酚,并对反应条件进行研究,通过单因素实验法初步研究铁碳比,pH,温度,铁碳的投加量,转速对降解效果的影响。研究结果表明,以200ml的500ppm对硝基苯酚溶液为例,当铁碳比为2:1,反应温度为60℃,转数为400r/min,铁碳投加量为6g,初始pH为2时,降解效果最好,对硝基苯酚在2h内还原效率可达100%。
关键词:铁碳微电解法 硝基苯 对硝基苯酚 单因素实验法;
Optimization of Reduction of Nitrobenzene Organic Compounds by Fe/C Microelectrolysis
Abstract
The reduction of nitrobenzene wastewater was studied by iron-carbon microelectrolysis. The reduction rate of p-nitrophenol and the formation rate of p-aminophenol were used as evaluation indexes. The single factor experiment method was used to synergistically degrade the iron-carbon microelectrolysis. P-nitrophenol, and the reaction conditions were studied. The effects of iron-carbon ratio, pH, temperature, iron and carbon dosage and rotation speed on the degradation were studied by single factor experiment. The results show that 200mg of 500ppm p-nitrophenol solution, for example, when the iron to carbon ratio is 2:1, the reaction temperature is 60 ° C, the number of revolutions is 250r / min, the iron carbon dosage is 6g, the initial pH is 2 The degradation effect is best, and the reduction efficiency of p-nitrophenol can reach 100% within 2 hours.
Key words: iron-carbon microelectrolysis; nitrobenzene; p-nitrophenol; single factorexperimental method
目 录
摘 要 I
Abstract II
目 录 i
第一章 研究背景 2
1.1 前言 2
1.2对硝基苯酚的性质. 2
1.3硝基苯废水的主要处理方法 2
1.4本课题的研究意义 3
1.5铁碳微电解机理 4
1.6微电解填料研究体系 6
第二章 实验部分 8
2.1 实验仪器与实验试剂 8
2.2 实验步骤。 8
第三章 结果与讨论 12
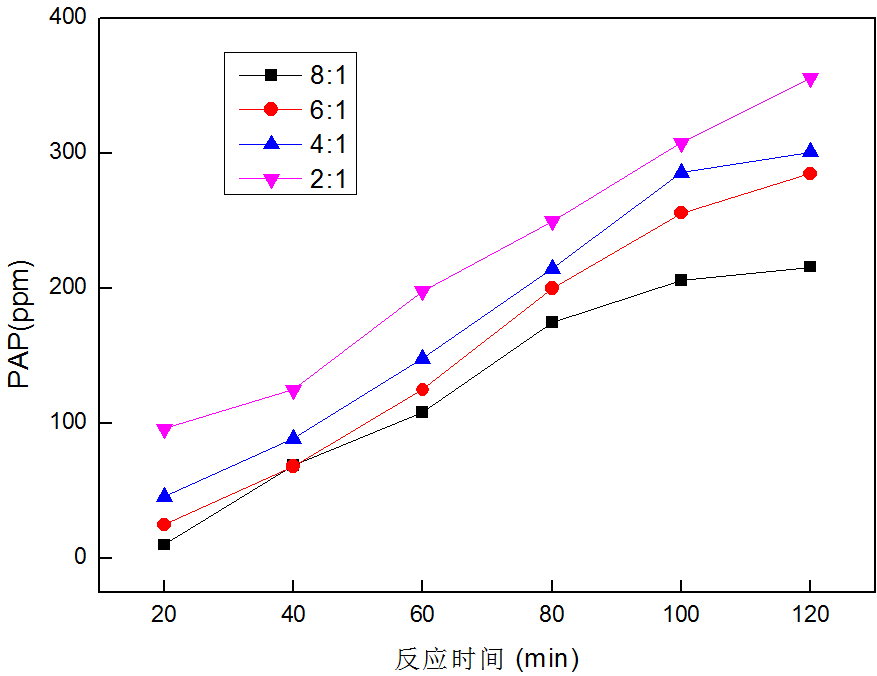
3.1铁碳比对降解效果的影响 12
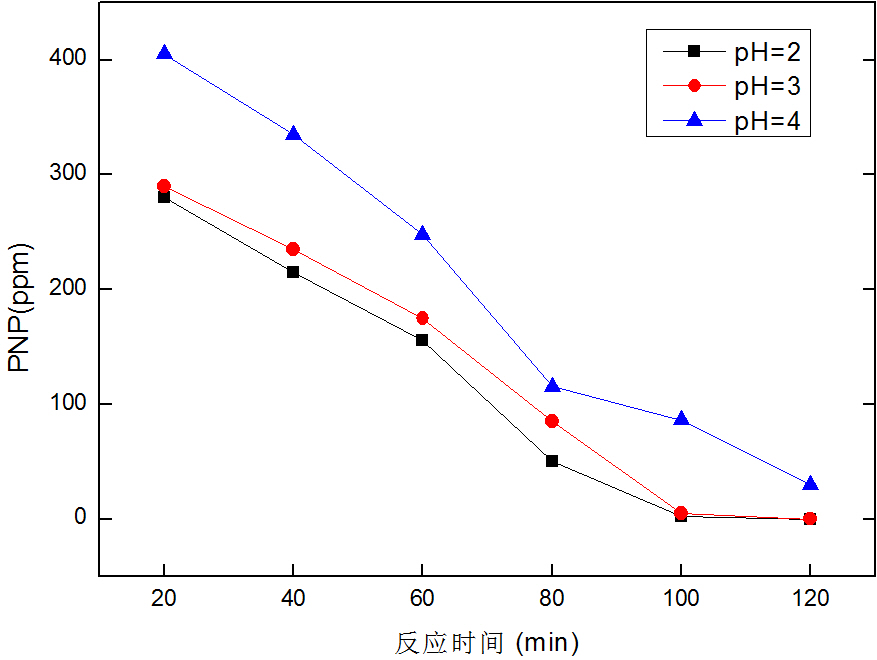
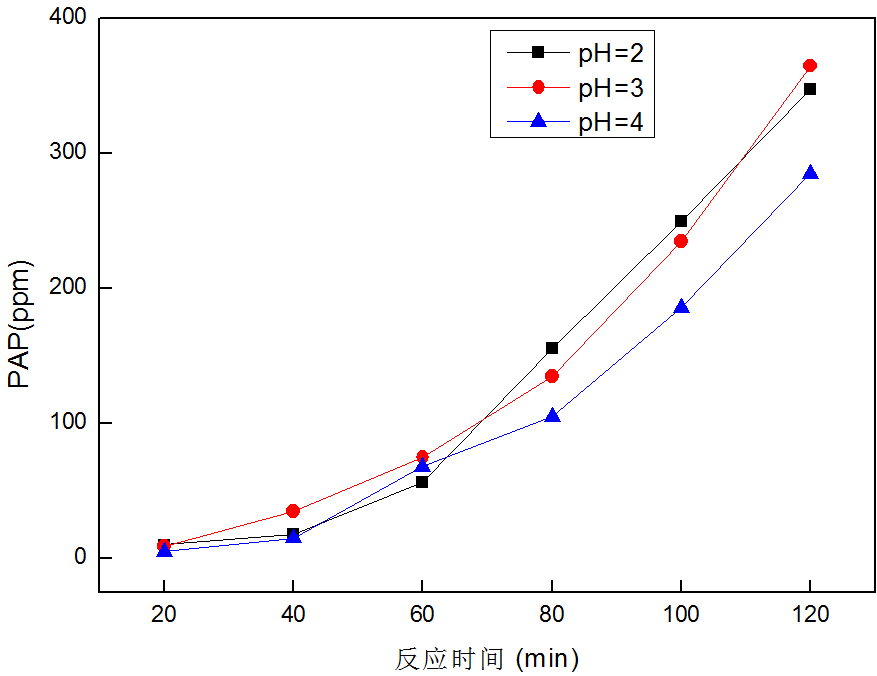
3.2 pH对降解效果的影响 13
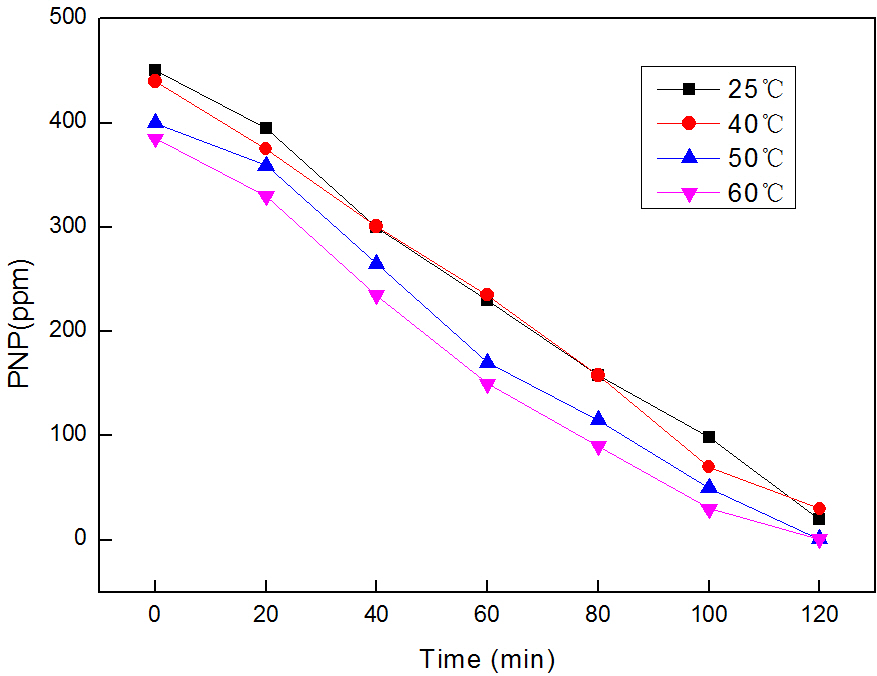
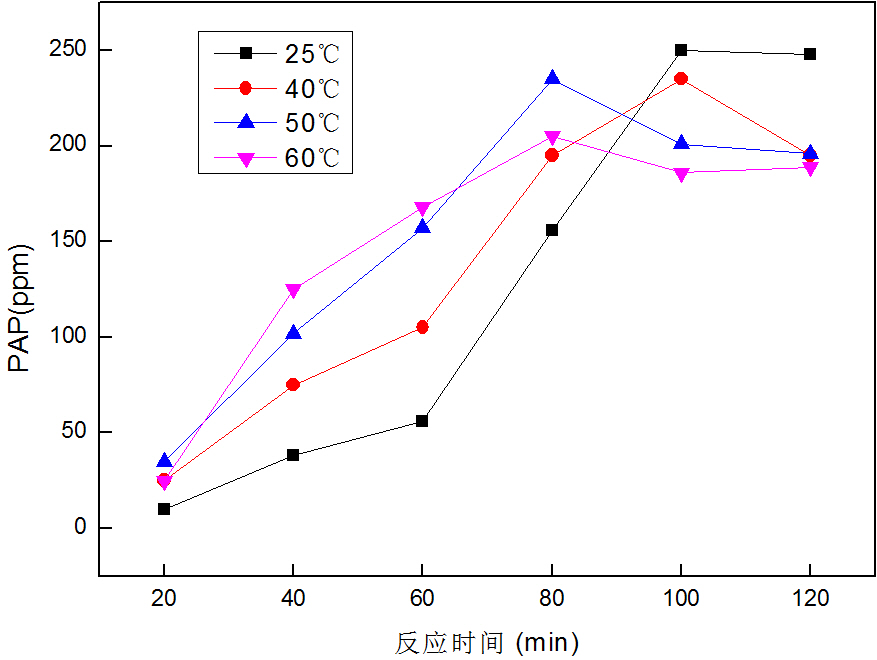
3.3温度对降解效果的影响 15
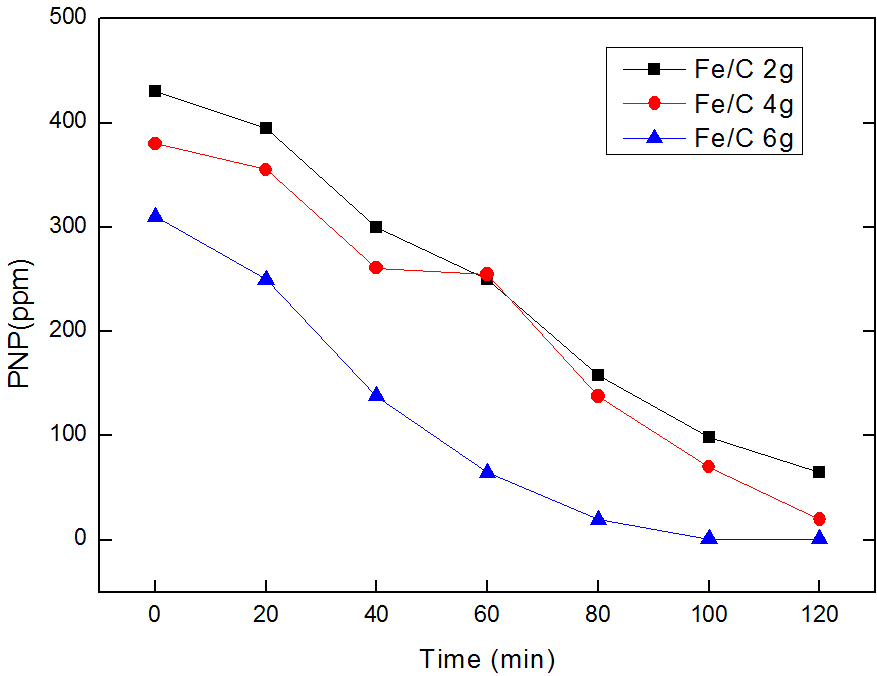
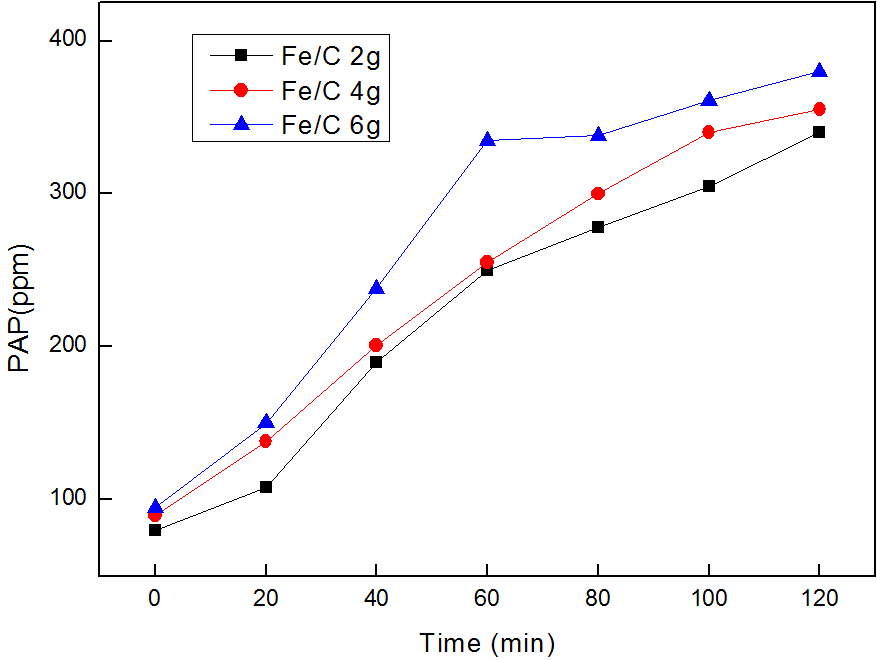
3.4铁碳投加量对降解效果的影响 17
3.5转数对降解效果的影响 18
第四章 结论与展望 21
4.1结论 21
4.2展望 22
参考文献 23
致 谢 26
第一章 研究背景
1.1 前言
我国是一个拥有众多大型化工企业的国家,诸如炼油厂、石油化工厂、合成纤维厂、炼油厂等化工企业每年会排出大量的废水,使水体污染问题日益严重,加快了我国水资源短缺与经济高速发展的矛盾,水体污染问题已经成为制约我国社会和经济发展的重要因素。硝基苯类废水是是废水中较为难处理的一类,是用于农药生产和染料合成工艺中不可缺少的原料物质或中间产物,这类废水具有优秀的稳定性,不易被降解,所以硝基苯类废水的降解一直是废水处理中的难题[1]。对硝基苯酚是典型的硝基苯类化合物,在化学工艺生产中应用广泛,所以对硝基苯酚的降解问题也就变得日益严重起来。
1.2对硝基苯酚的性质.
对硝基苯酚(p-nitrophenol)简称为PNP,分子量为139.11,共有三个同分异构体。PNP被广泛用作皮革防霉剂、酸值指示剂,也被用于滴定分析用标准溶液,用作医药等精细化学品的中间体。由于对硝基苯酚有毒且具有强烈的刺激作用,吸入、皮肤接触及吞食都有害。此外,对硝基苯酚废水的处理难度大,而且对硝基苯酚一般可以随着生活污水及工业废水一起排放,如果未经处理就排放到环境中,将会造成严重的生态环境问题,危害极大。在实际生活中,由于硝基苯类化合物工艺工序的不同,导致水质差别也很大,随着技术的发展,加入了大量的染料和助剂等,使废水中的难降解物质量增加。
1.3硝基苯废水的主要处理方法
为解决硝基苯的水体污染问题,多年来,世界各国的科学家为此做出了不懈的努力,研究出了多种方法,大体分为以下类。
1.3.1物理法
物理法降解硝基苯废水,其主要原理就是利用物理方法将污染物从废水中分离出来。物理法的优点是能简便的分离原混合物,缺点是对某些物质有局限性,无法分离。廖伟[2]等以煤油作为稀释剂,磷酸三丁酯作为作为萃取剂,使用萃取法对硝基苯生产废水进行处理,得出在最佳工艺条件下,经萃取后经萃取后废水的生化性由0.13提高到0.2,废水的色度由10000降到2000左右,COD去除率达67.2%。 庹必阳等[3]利用锆/钛聚合羟基阳离子插入到钠基蒙脱石(Na-MMT)层间,制备出了新型的锆/钛柱撑蒙脱石(Zr/Ti-MMT)材料。得出在最佳工艺条件下,对硝基苯酚的吸附量和去除率分别为17.59 mg/g和87.94%。 陈天崖[4]等利用活性炭固定床吸附硝基苯废水,研究发现流量越低、活性炭填充量越高、硝基苯废水浓度越低,越有利于吸附溶液中的硝基苯。物理法还可以利用微生物的絮凝性和吸附性 对污染物进行降解,郑莹[5]等利用硝基苯废水对生物海绵铁体系进行驯化,结果表明:生物海绵铁对硝基苯有更强的适应性及氧化作用,对300mg/L 硝基苯废水的降解率在98%以上,为经济有效地处理硝基苯废水提供了新思路。
1.3.2化学氧化法
传统氧化法的基本原理时利用强氧化剂氧化分解水中的污染物,现在最为流行的是高级氧化工艺,如电化学氧化等,这些工艺的优点是氧化性强,它们的强氧化性主要得益于其在化学反应的工程中,能产生一种具有强氧化性的基团—羧基自由基,高级氧化工艺可以将废水中的一些大分子大部分分解为可降解吸收的小分子物质。刘青松[6]对微波强化Fenton氧化降解水中硝基苯进行了研究。得出在最佳工艺条件下,初始浓度为80ppm的硝基苯降解率达到98.1%,低于国家一级排放标准。
1.4本课题的研究意义
水是一种容易受到污染的可再生资源,随着我国的经济和工业的飞速发展,水资源的污染问题越发严重起来,可利用的水资源日益短缺,而硝基苯类废水由于其具有良好的生物、化学稳定性,以及有害性,国家对此类废水的排放标准越来越严格,因此必须对此类废水进行处理。使清洁、干净的水资源回归于自然界。由于硝基苯类废水每年的排放量较大、成分复杂,且水质变化大,采用传统的物理、化学或生物的方法直接处理硝基苯类废水,处理效果不够理想。近年来,研究发现使用微电解法降解硝基苯类废水是一种非常高效可行的办法,而且该技术可以与其他不同的处理方法进行耦合,已达到最佳的处理效果。如在微电解反应后,通过添加过氧化氢构成芬顿反应,或是通入臭氧进行氧化等,经过耦合工艺处理的废水其生化性大大优于没经过耦合工艺处理的废水。俸志荣[7]等使用铁碳微电解法处理含硝基苯类废水,考察了部分反应因素对还原效果的影响。李水秋[8]等研究了铁碳微电解技术处理难降解废水的进展,介绍了铁碳微电解技术在部分难降解废水处理中的应用[9]。在处理硝基苯类废水时采用微电解工艺作为处理手段,主要是因为通过铁碳微电解中原电池反应产生的[H]破坏硝基苯类分子中的不饱和共轭结构,从而达到降解的目的。本文以对硝基苯酚溶液作为模拟硝基苯类废水,研究铁碳微电解对对硝基苯酚模拟硝基苯废水的处理效果。采用单因素实验法,考察了铁碳比、pH值、温度、铁碳投加量以及搅拌器转数对其处理效果的影响,确定得出最佳制备工艺条件。
1.5铁碳微电解机理
铁碳微电解法,又叫零价铁法、内电解法,是降解有机污染物的一种优秀技术。铁碳微电解法的基本原理是利用金属的腐蚀性,将难处理的污染物还原成易处理、吸收?的其他物质。该技术在上世纪七十年代应用到废水治理中,由于可以带来良好的环境和经济效益,并且具有设备简单、使用寿命长、成本,易操作维护、适用范围广等优点。这项技术自诞生以后,很快便在德、英、日、美等国家引起了广泛的重视,并且取得了一些非常显著的成果。我们国家自上世纪八十年代开始这一领域的研究,目前微电解技术已经成功应用于重金属、电镀、印染纺织化工等废水处理的预处理阶段,展现出了良好的应用前景。微电解技术处理废水的机理反应较为复杂,废水种类不同,起主要作用的机理也不同,主要可分为以下几种:
1.5.1原电池反应
铁碳微电解技术一般是采用活性炭作为阴极,铁作为阳极,这两种物质在目标溶液中会生产大量的微小原电池[10],其具体反应式如下所示:
阳极:Fe-2e→ (/Fe)=﹣0.44v
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: