助剂Cu2(OH)PO4和石墨烯协同增强TiO2光催化制氢性能的研究开题报告
2020-02-20 09:57:17
1. 研究目的与意义(文献综述)
随着工业革命进程的不断推进,世界各国在各种风险挑战中积极谋求发展。化石能源锐减和由使用化石能源引起的大气污染
随着工业革命进程的不断推进,世界各国在各种风险挑战中积极谋求发展。化石能源锐减和由使用化石能源引起的大气污染,温室效应等环境问题可以说是人类面临的各类挑战中的两大巨头。化石能源的不可再生,环境问题的不断恶化,使得寻找绿色清洁型、环境友好型的可再生二次能源成为人们关注的焦点。氢能,除了具备人们所期待的绿色清洁、环境友好的特点外,还具有燃烧性能好,放热效率高的优点1。1g的h2燃烧放出的热量为14×104j,这相当于3倍的1g汽油燃烧放出的热量2。且氢能应用模式丰富,能够帮助工业、建筑、 交通等主要终端应用领域实现低碳化。总而言之,若能实现氢能的大范围推广应用,我国的能源结构将得到很大的改善。
当前制氢较为成熟的技术是矿物燃料制氢和水电解制氢3,但这两项技术都基于传统非再生能源的使用,制氢过程伴有其他污染物产生,并达不到完全的绿色清洁。1972年,日本东京大学学者fujishima h k和honda k 首次报道了tio2光催化分解水制氢的实验4,这种通过光催化剂直接将太阳能分解水制氢的方法使得制氢技术向着绿色环保的目标迈出了开拓性的一步。
2. 研究的基本内容与方案
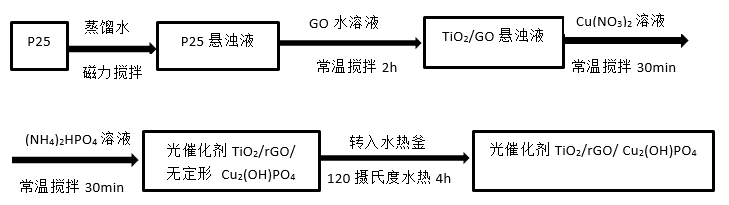
| 2.1. 实验流程图 2.2. 具体实验步骤: |
⒈溶液的配制:
0.01 mol #8226;L-1 Cu(NO3)2溶液: 0.2497 g Cu(NO3)2 100 mL H2O
0.01 mol#8226; L-1 (NH4)2HPO4溶液:0.1321 g(NH4)2HPO4 100mL H2O
10 vol%甲醇溶液:50 ml 甲醇 450 mL H2O
0.5 mg #8226;mL-1氧化石墨烯水溶液(GO):25 mg 氧化石墨烯 50 mL H2O 超声2 h
⒉光催化剂的制备
2-1:TiO2/rGO/ Cu2(OH)PO4的制备:
实验步骤:
(1) 三口瓶中加入300mg P25,加60mL蒸馏水分散,加入3mL 0.5mg/mL GO,室温下搅拌2h。
(2) 在搅拌下加入计算好的Cu(NO3)2室温下搅拌0.5h,加入(NH4)2HPO4 (Cu2(OH)PO4生成量相比于TiO2的比例0.5 wt%,0.8wt%,1 wt%,1.5wt%,2.0wt%),室温下搅拌30min。各样品用量如下表所示:
| 样品编号 | 0.01M Cu(NO3)2 /μL | 0.01M (NH4)2HPO4/μL |
| TiO2/rGO/Cu2(OH)PO4 (0.5%) | 1035 | 690 |
| TiO2/rGO/Cu2(OH)PO4(0.8 %) | 1657 | 1104 |
| TiO2/rGO/ Cu3(PO4)2 (1wt%) | 2071 | 1380 |
| TiO2/rGO/Cu2(OH)PO4 (1.5%) | 3106 | 2071 |
| TiO2/rGO/Cu2(OH)PO4(2.0 %) | 4142 | 2760 |
(3) 所得悬浊液转入水热釜中,鼓风干燥箱中120℃水热反应4h。
(4) 自然冷却,过滤,用蒸馏水洗涤3次,真空干燥12 h得到样品。实验过程中注意拍照记录反应过程中的颜色变化。
2-2:TiO2/rGO的制备:
实验步骤:
(1) 三口瓶中加入300mg P25,加60mL蒸馏水分散,在搅拌下加入计算好的Cu(NO3)2室温下搅拌0.5h,加入(NH4)2HPO4,室温下搅拌30min。
(2) 所得悬浊液转入水热釜中,鼓风干燥箱中120℃水热反应4h。
(3) 自然冷却,过滤,用蒸馏水洗涤3次,真空干燥12 h得到样品。实验过程中注意拍照记录反应过程中的颜色变化。
2-3:TiO2/ Cu2(OH)PO4的制备:
实验步骤:
(1) 取80 mg P25分散到80 mL H2O中三口瓶中。
(2) 在搅拌下加入计算好的Cu(NO3)2和NaH2PO2(Cu3P生成量相比于TiO2的比例0.1 wt%,1 wt%,5 wt%),室温下搅拌0.5h。
(3) 用封口膜密封三口瓶,通N2 15 min除尽瓶内空气。
(4) 用4个365 nm 100%功率的LED灯光照60 min。
(5) 过滤,用无水乙醇洗涤几次,真空干燥3h得到样品。
| 2.3. 光催化制氢性能的测试 |
(1)将50 mg所制备的光催化剂放入100 mL平底三口烧瓶中,通过搅拌或超声处理使材料分散于80 mL10 vol%甲醇水溶液中。
(2)通入氮气15 min,除去反应器中的空气和水中溶解的氧。
(3)将反应体系密封后,采用边搅拌边在LED灯照射下的方式进行光催化制氢反应,其目的是使光催化剂悬浮在牺牲剂体系中,使反应得以充分进行。
(4)每30 min用微量气体进样器插入到烧瓶封口处的硅胶塞从体系中抽取400μL气体,用气相色谱仪测出所生成氢气的含量,气相色谱仪型号为日本岛津GC-2014C,配置TCD检测器,载气为氮气,毛细管柱为5 Aring;分子筛。
2.4. 样品的表征
对TiO2、TiO2/rGO/Cu2(OH)PO4、TiO2/rGO和TiO2/Cu2(OH)PO4样品采用XRD、SEM、EDX、UV-vis进行表征和分析,分析助剂Cu3P和石墨烯表面修饰TiO2增强其可见光光催化制氢性能的机理。
| 3. 可行性分析 (1) 已有大量文献表明TiO2是一种高效的光催化剂,且以 Cu2(OH)PO4和石墨烯作助催化剂表面修饰 TiO2增强光催化制氢性能有理论基础。 |
3. 研究计划与安排
| 第1-2周:与导师见面,查阅相关文献资料,明确研究内容,了解研究所需条件。确定方案,完成开题报 告。 第3-4周:完成任务书和开题报告并准备实验仪器及药品,探索实验方法; 第5-11周:按研究方案开展实验,并结合实际情况进行优化和改进; 第12-14周:分析所得数据,制备样品进行相关测试;学会用软件处理实验数据,画出相应图形,并分析讨论。 第15周:整理实验数据,完成并修改毕业论文。 |
4. 参考文献(12篇以上)
|
|