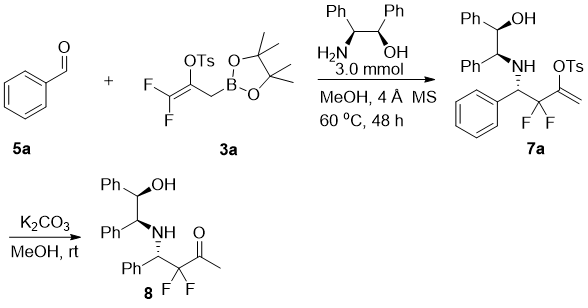
邻羟基促进亚胺的偕二氟烯丙基硼基化反应毕业论文
2020-04-06 11:15:49
摘 要
在有机化合物的特定位置引入偕二氟亚甲基可以显著改善母体化合物的亲脂性、生物活性以及代谢稳定性。偕二氟高烯丙基胺骨架广泛存在于许多药物分子中,此类化合物的合成吸引了许多有机化学工作者的关注。目前合成偕二氟高烯丙基胺类化合物的方法存在使用超过当量金属试剂、底物适用范围受限等问题。因此,开发一种绿色有效的合成此类化合物的方法具有重大的意义。
本文采用稳定、无毒的偕二氟烯丙基硼酸频哪醇酯试剂,在亚胺的邻位引入羟基,活化偕二氟烯丙基硼酸频哪醇酯,促进亚胺的偕二氟烯丙基硼基化反应,最终,在无催化剂且温和的条件下成功获得了多种消旋偕二氟高烯丙基胺类化合物。进一步,通过使用商业购买的手性氨基醇,经三组分反应,以高达97%产率、99:1 dr值获得了手性偕二氟高烯丙基胺化合物。除此之外,反应可扩大至克级规模,并且催化产物可以进一步转化为α-偕二氟亚甲基-β-胺基羰基化合物。
关键字:偕二氟高烯丙基硼酸酯;偕二氟高烯丙基胺;邻羟基;非对映选择性
Abstract
Incorporation of difluoromethylene group (CF2) into organic molecules can greatly modify their lipophilicity, biological activity and metabolic stability. Therefore, the development of efficient synthetic route to obtain such types of compounds has flourished in recent years. The skeleton of gem-difluorohomoallyl amine is widely found in many biologically active compounds, and it has attracted great attention from many organic chemists. However, the reported approaches to synthesize gem-difluorohomoallyl amines are far from ideal duo to the requirement for stoichiometric amounts of metals and the limited substrate scope of gem-difluoroallyl species. In this context, the discovery of an efficient and environmentally-benign preparation method for gem-difluorohomoallyl amine is highly desirable.
We herein reported a gem-difluoroallylboration of imines enabled by the neighboring hydroxyl group under no-catalyst reaction conditions, affording various racemic gem-difluorohomoallyl amine derivatives in good to excellent yields (up to 98% yield). Besides, the diastereoselective Petasis-type reaction accelerated by commercially available chiral amino alcohols was achieved, which provided diverse chiral gem-difluorohomoallyl amines in good yields (up to 98% yield) and diastereoselectivity (up to 99:1 dr). Furthermore, the gram-scale syntheis and synthetic application to enantioenriched α-CF2-β-amino carbonyl compound were demonstrated. Based on the control experiments and stereochemistry of an addition adduct, a plausible transition state model was proposed to elucidate the significance of the neighboring hydroxyl group and high stereoselectivity.
Key word: gem-difluoroallylboronate, gem-difluorohomoallyl amine, neighboring hydroxyl group, diastereoselectivity
目录
摘要 I
Abstract II
第1章 绪论 1
1.1 引言 1
1.2 含氟化合物之偕二氟亚甲基化合物 1
1.3 偕二氟高烯丙基胺化合物的合成方法 3
1.4 偕二氟烯丙基硼化合物的反应进展 5
1.5 亚胺的烯丙基硼基化反应 7
第2章 实验部分 9
2.1 引言 9
2.2 实验仪器及试剂 9
2.2.1 实验仪器 9
2.2.2 实验药品 10
2.3 偕二氟高烯丙基硼酸酯的合成 11
2.3.1 -OTs取代的偕二氟高烯丙基硼酸酯的合成步骤 11
2.3.2 其他取代基的偕二氟烯丙基硼酸酯的步骤 13
2.4 偕二氟高烯丙基硼酸酯与胺反应探究 14
2.4.1 实验操作方法 14
2.4.2 结果讨论 15
第3章 总结展望 25
参考文献 26
致谢 29
绪论
引言
含氟化合物因为引入氟原子而使其具有特殊的物理化学性质,一直是有机化学家研究的重点。一般,将偕二氟亚甲基结构引入化合物中,可以显著改变化合物的性质使其有特定的应用,其中偕二氟烯丙基胺化合物的合成更是吸引了众多有机化学工作者的关注。虽然这类骨架存在于许多具有生物活性的分子中,但是这类化合物的合成研究报道还较少,发展一种高效的合成这类化合物的方法是有机化学工作者的追求目标。通过搜索文献,我们发现目前报道的偕二氟烯丙基胺化合物的合成均有一些显著的弊端,我们设想通过偕二氟烯丙基硼化合物与亚胺反应得到目标产物,并沿着这条思路设计一个高效的合成反应方案。
含氟化合物之偕二氟亚甲基化合物
我们知道氟位于元素周期表中第二周期、ⅦA族,作为元素周期表中电负性最大的元素,它具有和氢原子相近的范德华半径。由于氟原子特殊的电子结构和较小的半径,具有强的吸电子能力和弱的可极化性,当它被引入化合物中时能显著地改变化合物的物理和化学性质[1]。在众多的含氟官能团中,氟烷基的研究比较多。
氟烷基选择性地整合到生物活性化合物中往往会产生许多有益的效果,如结合亲和力,代谢稳定性,亲脂性,膜通透性和生物活性的提高[2]。药物设计来调节生物活性分子的化学,生物和物理性质,这为合成氟烷基团的方法的发展提供了动力[3]。尽管选择性三氟甲基化,包括不对称催化型,已经被深入研究[4],然而对于偕二氟烷基选择性结合到有机分子的研究还处于初始阶段[5]。
一般,偕二氟烷基可以看作是被氢原子、烷基或其他官能团取代的偕二氟亚甲基。几种普通类型的偕二氟烷基(I-IV)显示在图 1.1中。掺入二氟烷基后,例如α,α-二氟羰基III和含杂原子的IV基团可以用作合成的多功能结构单元的其他氟化部分。
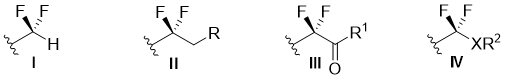
图 1.1不同类型的偕二氟烷基
由于它们的结构多样性,引入偕二氟烷基已经在药物设计[6]和催化剂开发(图 1.2)中得到广泛的应用[7]。还应该指出,在被它们掺入的有机化合物中,不同类型的二氟烷基可以带来不同有益的影响。例如,CF2H基团可以作为比-OH或-NH更亲脂的氢键供体[8],对于药物设计非常有意义。泮托拉唑[7]和依氟鸟氨酸[9]是两个合理设计的药物,具有CF2H基团。偕二氟亚甲基的强吸电子效应可以影响其相邻基团的电子性质,如,它可以增加吉西他滨(作为用作化学疗法的核苷类似物)中的负电荷密度。在这种情况下,拓扑异构酶
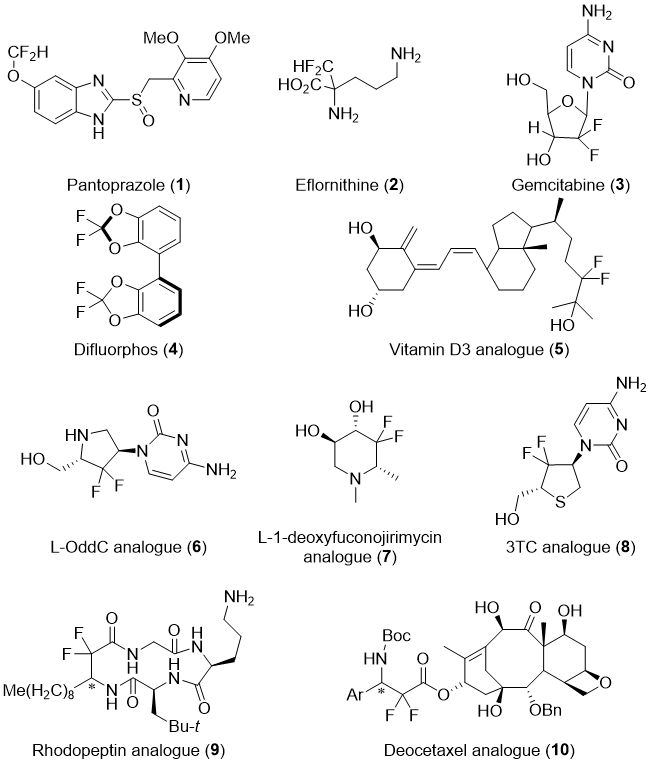
图 1.2出现了偕二氟结构片段的重要化合物
I的带正电荷的催化位点与取代位点附近的DNA的结合增强[10]。使用偕二氟亚甲基调节配体的电子性质有助于强有力的二膦配体4[11]。通过用偕二氟亚甲基取代亚甲基得到的化合物5-8在相应的生物活性化合物中的二氟亚甲基基团均具有改善的性质[12; 13]。偕二氟亚甲基还可以增加相邻羰基的亲电性。这使α-二氟代羰基化合物能够形成稳定的水合物或半缩酮,其模拟了参与肽键酶裂解的四面体中间体,从而抑制了许多水解酶的活性[10]。红光肽素的二氟类似物(9)具有增强的物理和生物学特性,如急性毒性和溶解性,同时保留其抗真菌活性。
具有偕二氟烷基的手性碳中心也是药物和生物活性化合物中的常见结构基元,如图 1.2所示。在不对称合成具有二氟烷基手性中心的对映异构体化合物方面许多化学工作者已经做出了巨大的努力,并且通过使用手性催化剂进行合成控制取得了一定的进步。[10; 14]由于含偕二氟亚甲基化合物地特殊性,所以这类物质的合成是目前有机氟化学中的一个研究热点。
偕二氟高烯丙基胺化合物的合成方法
在文献调研中,我们发现,已报道的合成偕二氟高烯丙基胺化合物的方法一般均通过使用偕二氟烯丙基金属试剂和亚胺进行反应。
在2006年,Zhu课题组发展了锌促进的偕二氟烯丙基溴试剂(12)与亚胺(11)的串联反应[15]。首先发生烯丙基化反应,这步反应存在区域选择性,接着进行取代反应,这步反应又存在化学选择性。因此,反应最终获得了三种产物,分别是:γ-位的烯丙基化接分子内的胺基进攻酯基后的产物(13)、γ-位的烯丙基化接分子内的胺基取代苄氧基的产物(14)以及α-位的烯丙基化接分子内的胺基进攻酯基后的产物(15),如图 1.3所示。
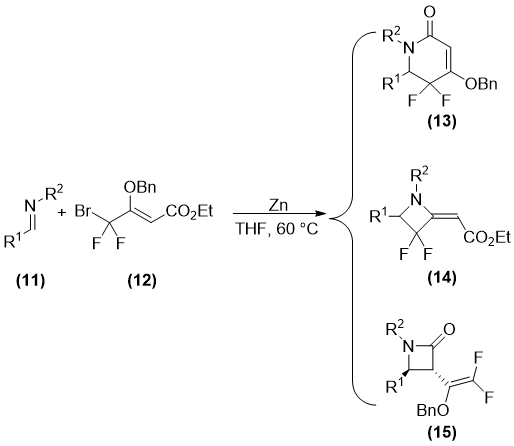
图 1.3锌促进的亚胺的偕二氟烯丙基化反应
2008年,Wang和Zhao课题组合作,通过加入锌粉促使偕二氟烯丙基溴试剂(17)与亚胺的前驱体α-苯砜基胺(16)发生反应(如图 1.4)得到了偕二氟高烯丙基胺化合物(18)[16]。该反应的产率较高(76-99%),但是,使用超过当量的金属锌试剂以及偕二氟烯丙基溴底物范围相当有限的问题使得该反应的应用受到了限制。
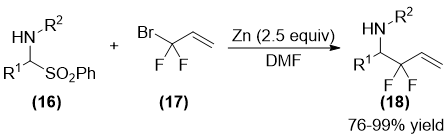
图 1.4锌促进的胺基砜的偕二氟烯丙基化反应
2009年,Qing课题组采用金属铟促进的偕二氟烯丙基溴试剂(17)与亚胺(19)的加成反应(反应式如图 1.5),得到偕二氟高烯丙基胺化合物(20)[17]。由于该反应需要使用超过当量的金属铟时,才能获得较好的结果。同时,和之前所报道的采用偕二氟烯丙基溴进行反应的方式一样,偕二氟烯丙基溴的底物范围有待进一步拓展。同年,该组报道了偕二氟烯丙基锌试剂与手性亚胺(21)在二氯化锡催化下的非对映选择性加成反应[18](反应式如图 1.6)。最终以42%-86%的产率和高非对映选择性(最高可以得到单一非对映异构体)得到了手性偕二氟高烯丙基胺化合物(22)。
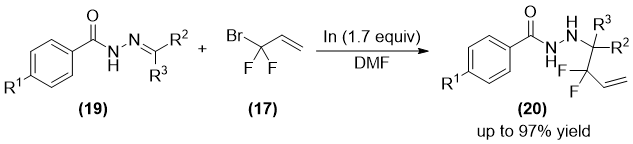
图 1.5铟促进亚胺的偕二氟烯丙基化反应
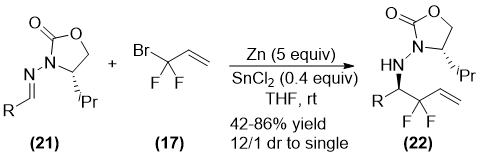
图 1.6二氯化锡催化亚胺与偕二氟烯丙基锌试剂的反应
以上方法均使用了金属试剂,以及底物使用范围有限,因此发展一种绿色高效合成偕二氟烯丙基胺化合物的方法具有重大的意义。
偕二氟烯丙基硼化合物的反应进展
目前,偕二氟烯丙基硼化合物还只用于和羰基化合物发生加成反应,对于和亚胺发生类似加成反应的报道几乎没有。
2008年,Ramachandran课题组首次合成了偕二氟烯丙基硼酸酯(23),并实现了其与醛(24)的加成反应[19],以很好的产率得到了一系列偕二氟高烯丙基仲醇化合物(25)。接着在2009年,将(23)与酮(26)进行反应[20],在温和条件下以较高的产率得到了一系列偕二氟高烯丙基叔醇化合物(27)。在2011年,该课题组又合成了手性偕二氟烯丙基硼酸酯(28),将它和苯甲醛(29)进行反应[14],结果以68%的产率、93% ee值获得了手性偕二氟高烯丙基仲醇化合物(30)。然后,在此化合物的基础上经多步反应以gt;99% ee值获得了偕二氟的六元环内酯化合物(31)。同年,他们又合成了手性偕二氟烯丙基硼烷(32),通过它与醛(24)的不对称加成反应[21],获得了各种各样的手性偕二氟高烯丙基仲醇化合物(33)。(如图 1.7)
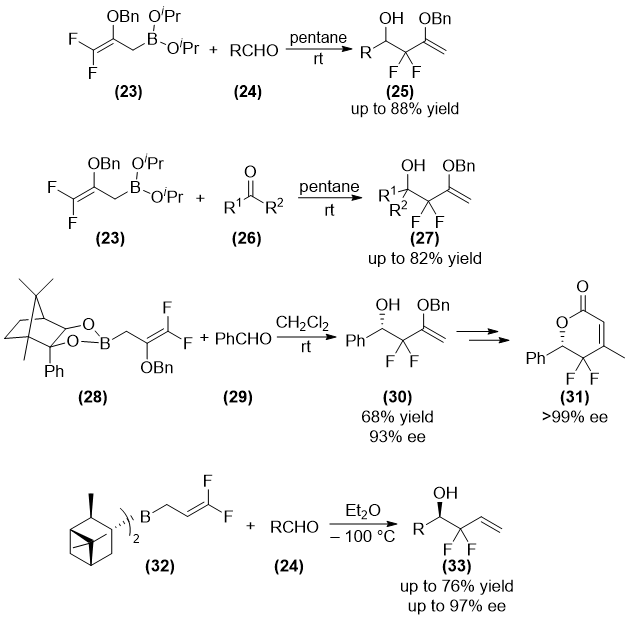
图 1.7 Ramachandr课题组对偕二氟烯丙基硼基化反应的研究
随着研究的深入,关于偕二氟烯丙基硼酸酯合成报道越来越多,2016年,Zhang课题组合成了具有相当稳定性的-OTs取代的偕二氟烯丙基硼酸酯(34),在温和条件,以苯甲酸作为催化剂,它可以与醛发生反应,得到偕二氟高烯丙基仲醇类化合物(如图 1.8)[22]。该反应的底物适用范围广,反应的产率可以高达95%。
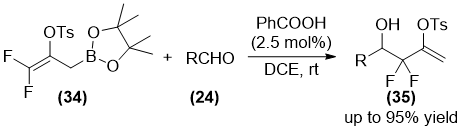
图 1.8稳定的偕二氟烯丙基硼酸酯和醛的反应
亚胺的烯丙基硼基化反应
我们知道,亚胺与羰基化合物相比而言,由于氮原子的电负性比氧原子小,其碳氮双键的极化相对弱一些,所以亲电性差[23]。因此,亚胺的烯丙基硼基化反应对烯丙基硼基化化合物有要求,一般采取的方式是可以采用活化的烯丙基硼酸酯,或者活性较高的烯丙基硼化合物。对于亚胺的烯丙基硼基化反应的研究,已经有不少课题组进行了相关报道。
Schaus课题组发现3,3-二取代的BINOL催化剂对加速烯丙基硼酸酯、胺、醛,三组分发生反应生成高烯丙基胺所必不可少。2007年,他们通过这种催化剂使烯丙基硼酸二异丙酯和亚胺发生加成反应得到手性的高烯丙基胺化合物[24]。2017年,他们又实现了催化醛、胺、烯丙基硼酸酯三组分的不对称加成反应[25]。(如图 1.9)
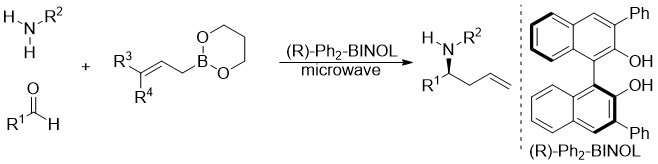
图 1.9 BINOL催化亚胺的烯丙基硼基化反应
除此之外,Zhang课题组报道了手性氨基醇、烯丙基硼酸酯、氧化吲哚三组分的非对映选择性加成反应(如图 1.10)[26]。这是一个邻羟基促进的生成手性高烯丙基胺化合物的反应,首先手性氨基醇和氧化吲哚反应制备亚胺,接着氨基醇中的羟基与烯丙基硼酸酯发生酯交换反应,得到一个新的烯丙基硼化合物,最后在分子内发生反应,得到目标物。
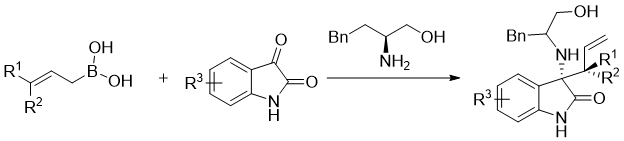
图 1.10邻羟基促进亚胺的硼基化反应
对于活性更低的的烯丙基硼酸频哪醇酯与亚胺的加成反应,可想而知需要特定的条件进行活化反应。由文献调研,活化烯丙基硼酸频哪醇酯的方法均是采用金属试剂。而我们由Zhang课题组的报道得到灵感,期望通过采用邻羟基促进偕二氟烯丙基硼酸酯与亚胺的加成(如图 1.11),避免使用金属试剂。

图 1.11邻羟基促进稳定的偕二氟烯丙基硼酸酯与亚胺的反应
实验部分
引言
偕二氟高烯丙基胺是许多生物活性分子中的核心骨架。目前,合成偕二氟高烯丙基胺化合物的方法比较少,现已报道的合成偕二氟高烯丙基胺化合物的方法均是采用偕二氟烯丙基金属试剂与亚胺进行反应,除此之外,该类方法还存在底物适用范围比较有限等问题。[27]因此,发展一种高效的方法学合成偕二氟高烯丙基胺化合物尤其是合成手性偕二氟高烯丙基胺化合物具有重要的意义。通过文献调研,借鉴文献已报道的方法合成偕二氟烯丙基硼酸酯,然后将得到的偕二氟烯丙基硼酸酯与亚胺进行加成反应,进行反应条件优化,得到了高效合成偕二氟高烯丙基胺类化合物的方法。
实验仪器及试剂
实验仪器
表 2.1 实验仪器列表
名称及型号 | 生产厂家 |
BSA224S分析天平 | 赛多利斯科学仪器(北京) 有限公司 |
YP2002 电子天平 | 上海佑科仪器仪表有限公司 |
ZF-20D暗箱式紫外分析仪 | 上海科兴仪器有限公司 |
2XZ-4型旋片式真空泵 | 中国临海市谭式真空设备有限公司 |
GM-1.0A隔膜真空泵 | 天津市津腾实验设备有限公司 |
DZX-3 型真空干燥箱 | 上海福玛实验设备有限公司 |
DHG-90543A电热恒温鼓风干燥箱 | 上海精密实验设备有限公司 |
08-2G恒温磁力搅拌器 | 上海驰久仪器有限公司 |
DF-101S集热式恒温加热磁力搅拌器 | 上海卫凯仪器设备有限公司 |
DLSB-5L/20低温冷却液循环泵 | 上海予华仪器设备有限公司 |
SHZ-D(Ш) 循环水式真空泵 | 上海予华仪器设备有限公司 |
RE-52AA旋转蒸发仪 | 上海予华仪器设备有限公司 |
ZNCL-B 智能恒温磁力搅拌器 | 巩义市予华仪器设备有限公司 |
高纯氮 | 武汉市明辉气体科技有限公司 |
TCL 硅胶板GF254 | 青岛海洋化工厂分厂 |
实验药品
表 2.2 实验药品列表
药品名称 | 分子式 | 规格 | 生产厂家 |
三乙胺 | Et3N | 分析纯 | 上海秦巴化工有限公司 |
对甲苯磺酰氯 | C7H7ClO2S | 分析纯 | 上海秦巴化工有限公司 |
氯化铵 | NH4Cl | 分析纯 | 上海秦巴化工有限公司 |
氯化钠 | NaCl | 分析纯 | 上海秦巴化工有限公司 |
三氟乙醇 | CF3OH | 分析纯 | 上海秦巴化工有限公司 |
二氯甲烷 | CH2Cl2 | 分析纯 | 上海秦巴化工有限公司 |
四氢呋喃 | C4H8O | 分析纯 | 国药集团化学试剂有限公司 |
正丁基锂 | n-BuLi | 分析纯 | 上海秦巴化工有限公司 |
异丙氧基硼酸频哪醇酯 | C9H19BO3 | 分析纯 | 上海秦巴化工有限公司 |
二溴甲烷 | CH2Br2 | 分析纯 | 上海秦巴化工有限公司 |
溴亚甲基硼酸频哪醇酯 | C7H14BO2Br | 分析纯 | 上海秦巴化工有限公司 |
苯甲醛 | C7H6O | 分析纯 | 上海秦巴化工有限公司 |
甲醇 | CH4O | 分析纯 | 国药集团化学试剂有限公司 |
碳酸钾 | K2CO3 | 分析纯 | 上海秦巴化工有限公司 |
石油醚 | --------- | 化学纯 | 武汉欣申试化工科技有限公司 |
乙酸乙酯 | C4H8O2 | 化学纯 | 武汉欣申试化工科技有限公司 |
无水硫酸钠 | Na2SO4 | 分析纯 | 国药集团化学试剂有限公司 |
无水硫酸镁 | Mg2SO4 | 分析纯 | 国药集团化学试剂有限公司 |
氢氧化钠 | NaOH | 分析纯 | 国药集团化学试剂有限公司 |
实验中所用的溶剂THF是用金属钠经过无水处理的,TLC监测用的硅胶板和柱层析所用硅胶(200-300目)均是直接购买使用。试反应产物提纯所采用的硅胶板是实验室制备。
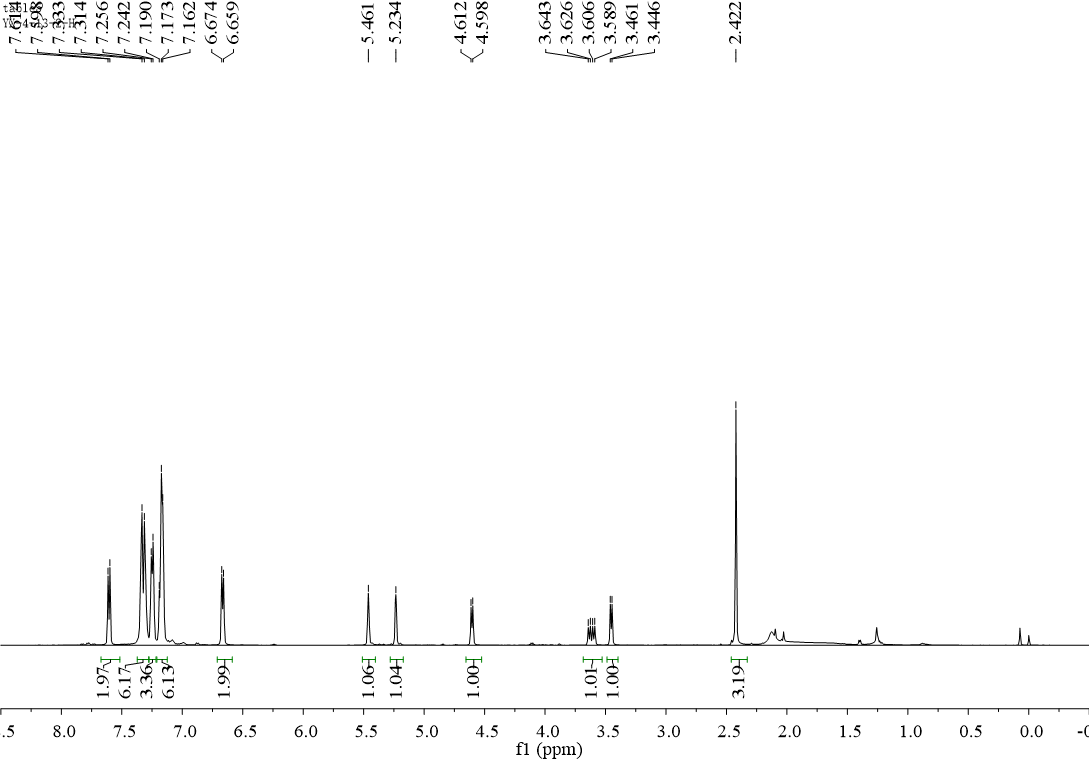
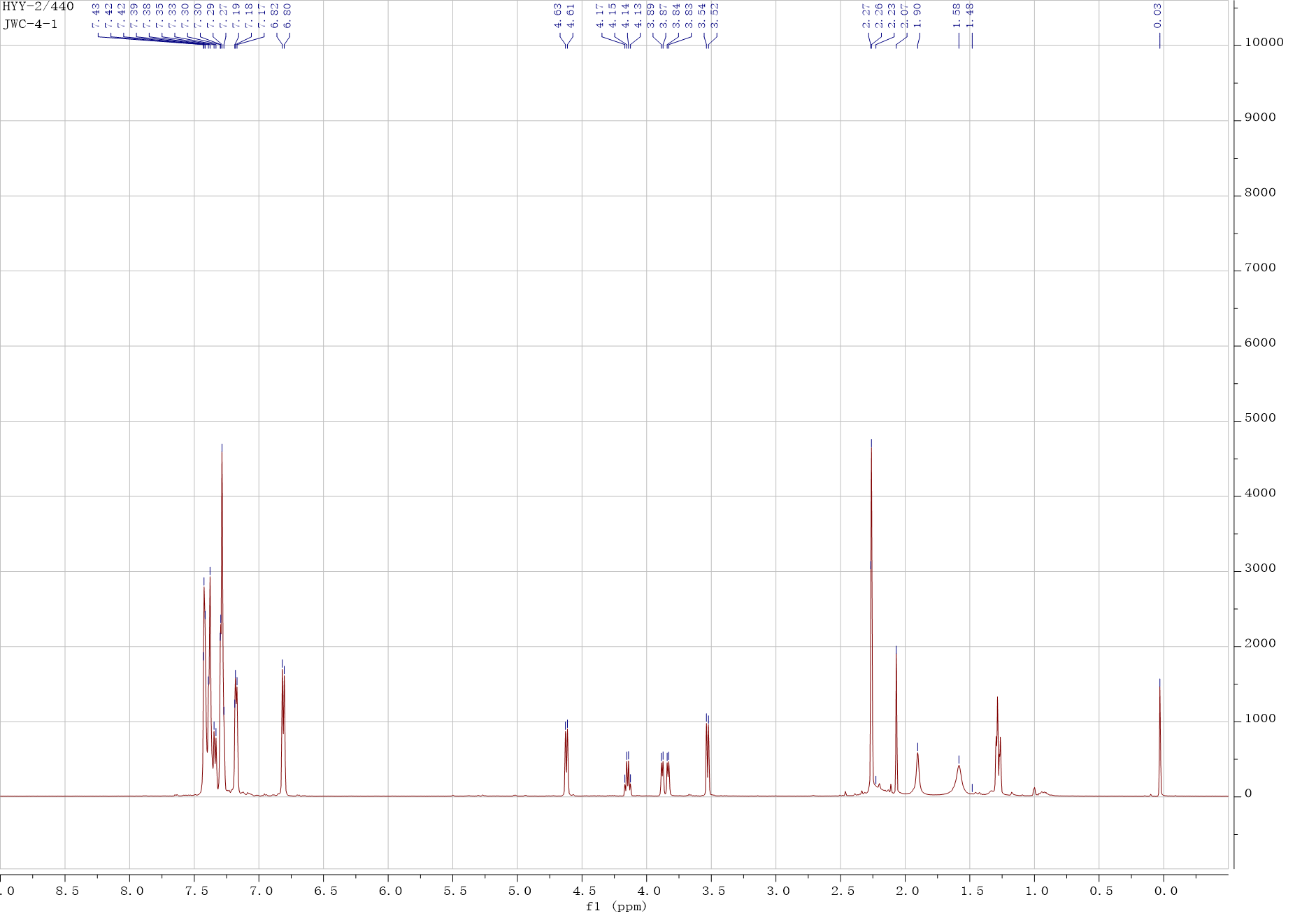
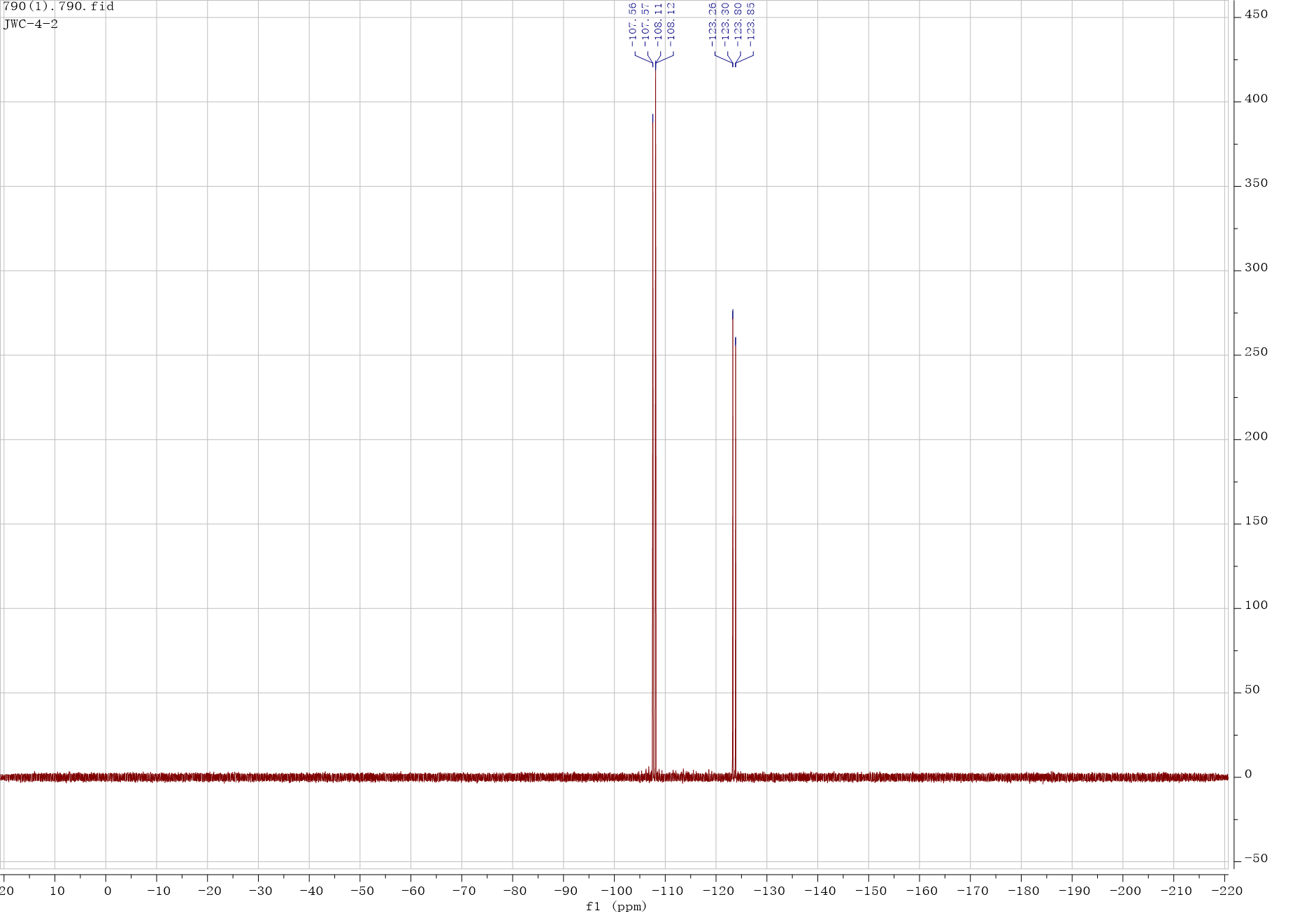
1H NMR、13C NMR和19F NMR采用Bruker Avance III 500 MHz (1H NMR, 500 MHz; 13C NMR, 126 MHz; 19F NMR, 471 MHz) 核磁共振波谱仪测定。高分辨质谱采用AB SCIEX TripleTOF 5600仪器测定。
偕二氟高烯丙基硼酸酯的合成
-OTs取代的偕二氟高烯丙基硼酸酯的合成步骤
对甲苯磺酸(2,2,2-三氟)乙酯的制备
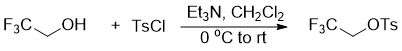
以上是毕业论文大纲或资料介绍,该课题完整毕业论文、开题报告、任务书、程序设计、图纸设计等资料请添加微信获取,微信号:bysjorg。
相关图片展示: