中空介孔硅的药物载体的制备及其载药量的研究毕业论文
2020-04-07 14:04:28
摘 要
药物传递系统对于药物的治疗效果有着至关重要的作用,尤其在抗癌药物方面,药物传递系统的选择起着更加重要的作用。在现代药物研究领域,基于中空介孔硅纳米颗粒构建的药物控释系统受到了广泛关注,本文设计并构建了中空介孔硅纳米颗粒的药物控释系统,并对其载药量进行研究,希望得到的药物载体可以针对恶性肿瘤组织或肿瘤细胞实现“定向爆破”释药。介孔硅材料所特有的、在纳米范围内规则排列且可调节的孔道结构,无疑对人们研究控释药物提供了良好的物质条件。
中空介孔硅材料中研究最为广泛的是M41S系列的介孔硅纳米材料。1992年mobil公司首次以十六烷基三甲基溴化铵(CTAB)为模板,结合溶胶凝胶法合成了代号为MCM41的有序介孔硅材料,它的合成方法简答,重复性好,并且具有粒径、孔径大小及孔壁组成和性质均可调等特点。介孔硅材料的表面含有大量的OH﹣活性基团,使得MSN的表面可以容易的进行特定的生物和化学修饰,从而实现介孔硅纳米材料的特异功能化。因此,介孔硅纳米材料被广泛用于构建具有特定功能的药物控释系统。
本文主要介绍了介孔硅纳米材料在药物载体方面的应用和制备方法,由于其含有丰富的硅羟基,具有良好的生物相容性和易于修饰的表面,所以在肿瘤治疗等领域有着广阔的应用前景。但是,基于介孔硅纳米材料的药物转运体仍处于研究阶段,并在该领域中,进一步提高介孔二氧化硅的纳米颗粒的载药量及其生物相容性仍是亟待解决的难题。
关键词:中空介孔硅,药物载体,纳米颗粒,载药量
Abstract
Drug delivery systems play a crucial role in the therapeutic efficacy of drugs.The selection of drug delivery systems plays a more important role, especially in the field of anti-cancer drugs.In the field of modern drug research, drug controlled release systems based on hollow mesoporous silica nanoparticles have attracted extensive attention.In this paper, the drug controlled release system of hollow mesoporous silica nanoparticles and its drug loading were designed and constructed.The desired drug carrier can achieve " directional blasting" drug release for malignant tumor tissues or tumor cells.The pore structure of porous silicon materials, which is arranged regularly and adjustable in the nanometer range, undoubtedly provides good material conditions for people to study controlled-release drugs.
M41s series mesoporous silicon nanomaterials are widely studied in hollow mesoporous silicon materials. In 1992, Mobil first synthesized ordered mesoporous silica material named MCM 41 by using CTAB as template and sol-gel method. its synthesis method was simple and repeatable, and its particle size, pore size, pore wall composition and properties were adjustable. The surface of the mesoporous silicon material contains a large number of oh - active groups, so that the surface of MSN can be easily subjected to specific biological and chemical modification, thereby realizing the specific functionalization of the mesoporous silicon nano - material. Therefore, mesoporous silicon nanomaterials have been widely used to construct drug controlled release systems with specific functions.
In this paper, the applications and preparation methods of mesoporous silicon nanomaterials in drug carriers are introduced. because of their abundant silicon hydroxyl groups, good biocompatibility and easily modified surface, mesoporous silicon nanomaterials have broad application prospects in tumor treatment and other fields. However, drug transporters based on mesoporous silica nanomaterials are still in the research stage, and in this field, further improving the drug loading and biocompatibility of mesoporous silica nanoparticles is still a problem to be solved.
Key words:hollow mesoporous silica nanoparticles,drug carrier,nanoparticle,drug-loading rate
目 录
摘 要 I
Abstract .Ⅱ
第一章 绪论 1
1.1 引言 1
1.2 介孔硅简介 1
1.3 基于介孔硅的药物控释系统 2
1.4 介孔硅纳米阀的种类 4
第二章 实验方案 6
2.1 实验目的 6
2.2 试剂和仪器 6
2.3 实验方案 6
第三章 中空介孔硅的制备 9
3.1 实验过程记录 9
3.2 问题和解决方案 17
第四章 载药量研究 19
4.1 载药量研究 19
第五章 结论 21
参考文献 22
致谢 24
第一章 绪论
1.1引言
癌症是目前最难治疗的疾病之一,据联合国文卫组织调查显示,恶性肿瘤每年引起的死亡人数已超过1000万例。因此,癌症是人类必须要攻克的顽疾,现阶段的医药学技术水平尚不能完全治疗癌症,仍以化疗和放疗为主。众所周知,这样的疗法不能根治癌症,而且有很多副作用,传统有效药物又会损伤正常细胞。因此,能否使药物实现定位释放是治疗癌症的关键。当前对于药物缓控释放是医药学研究的热点,相关领域的研究方兴未艾。
传统给药方式在面对癌症时出现了很多瓶颈,首先,手术切除有很多局限性,而且会给患者带来极大的痛苦,加之癌症一般发现时已经是中晚期,手术切除虽然能缓解病情,但是癌细胞时常伴有病灶转移及扩散的现象,很少有癌症得到根治。其次,传统的化疗方式在给药时多用静脉注射,使抗肿瘤药物随着血液分布至全身,在杀死癌细胞的同时会对很多正常细胞起到杀灭作用,对身体危害较大,加上很多抗癌药难溶于水,并且经过身体的代谢和排泄作用,很难达到有效治疗浓度,需要重复给药,增加治疗负担。
因此,研究药物靶向定位治疗和缓释控释系统是治疗癌症的关键,所以,研发能够起到药物靶向定位和缓控释放的药物载体,是当前研究的首要任务。
1.2介孔硅简介
中空介孔硅纳米材料为药物载体提供了广阔的应用前景,它的合成方法简单,重复性好,具有粒径、孔径大小及孔壁组成和性质科调节等特点。首次合成的介孔硅纳米材料是1992年mobil公司以十六烷基三甲基溴化铵(CTAB)为模板,用溶胶凝胶法合成的代号为MCM-41的有序介孔材料,其尺寸在20-500nm,孔径在2-6nm。这种介孔硅材料呈六方形结构,平行排列,这样的结构决定了介孔硅材料具有比表面积大和孔容积大的特点,易于同细胞接触并发挥作用;载药量大,可以大大提高药物的生物利用度,明显降低药物副作用以及辅料带来的其他不良反应。因此,中空介孔硅纳米材料被广泛应用于抗癌药物构建的靶向和缓控释系统。
图1.2.1 介孔硅材料微观示意图
如上图所示,中空介孔硅纳米材料是一种中空的多孔药物载体,由于介孔材料的表面含有大量的OH-活性基团,使得介孔硅材料可以容易地进行生物和化学修饰,从而实现其特异功能化,实现药物的控制释放。其包封材料目前有很多种,为了实现药物在介孔硅材料中有良好的包封率,做到零提前释放,设计刺激响应型的包封材料成为了研究热点。
有序介孔硅材料含有从一维到三维的有序孔道结构,其孔径分布均匀,可调控,介孔硅纳米颗粒由于其有序的均匀孔道和几何结构,使其运载的药物尺寸也可控制在纳米级别,并且具有一定的结构和体积,空间排列有序可调,我们可以形象地理解为“闭门造车”。中空介孔硅因其比表面积大、具有独特的孔道结构、可调的表面特性、无生物体毒副作用以及其良好的生物相容性等特点,在当前医药学领域有广阔的应用前景,尤其对于癌症的靶向治疗,可谓是一大突破。
另外,层层自组装技术可以提高介孔硅纳米颗粒的载药性能,通过改变组装的构筑单元及组装层数,调控多层膜组装的物化性能,从而改善介孔硅纳米颗粒的载药量。层层自组装技术可以对生物材料表面进行改性,构筑纳米粒子复合涂层引入药物,改善材料的生物相容性和功能特异性。层层自组装技术的涂料选材广泛,被广泛应用于生物医学研究领域,其膜表面的性能可以通过改变组装的构筑单元实现精确调控。以十六烷基三甲基溴化铵(CTAB)为模板,和硅酸四乙酯(TEOS)用溶胶凝胶法制得介孔硅,再将带负电的中空介孔硅和带正电的聚二烯丙基二甲基氯化铵(PDDA)交替组装,得到介孔硅纳米涂层。该技术可以使载体可吸附药物量大大增加,因此成为当今医药学领域的研究热点,但是,如何利用介孔硅的介孔以及与药物之间的氢键、静电相互作用等,将药物分子引入介孔硅载药涂层,并对其实现紧密包封,以及药物的靶向定位、控制释放,仍是该技术亟待解决的技术难题。
1.3基于介孔硅的药物控释系统
2003年,Tanaka等利用香豆素作为包封材料,将药物分子有效地封装在了介孔硅的孔道内部,构建了光敏感的可逆型介孔硅纳米药物控释系统,实现了基于介孔硅的药物载体的可控释放。同时,Victor Lin等提出了“纳米阀”的概念,顾名思义,纳米阀就是利用介孔硅的纳米分子包裹物将药物分子封堵在介孔硅孔道内部。这样的由纳米阀封堵的基于中空介孔硅的药物载体系统有效地实现了药物的控制释放,其良好的包封率,保证了药物分子的零提前释放,提高了药物的利用率,降低了药物对人体的毒副作用。其对癌细胞的靶向释放是由刺激响应机制实现的,具体的刺激形式有很多,常见的有光敏感性纳米阀、温度敏感性纳米阀、PH敏感性纳米阀、磁场敏感性纳米阀、氧化还原反应纳米阀、酶反应纳米阀、竞争性结合纳米阀等,这样的刺激响应型的纳米阀对于以中空介孔硅材料为载体的药物控释系统的治疗效果起着决定性的作用,非常适用于有毒性药物大分子和难以吸收的不溶性药物的治疗。
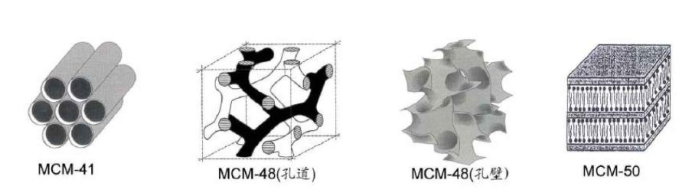
有序介孔硅材料大致可分为三类。第一类是上文提到的以表面活性剂为结构导向模板剂合成的MS41系列介孔硅材料,常见的有六方体型MCM-41、立方体型MCM-48以及层状的MCM-50等,其结构模板导向剂是十六烷基三甲基溴化铵(CTAB),配合硅酸四乙酯(TEOS)合成的具有一维孔道结构的介孔硅纳米颗粒,其合成方法简单,结构简单,产品收率好。本文设计的中空介孔硅合成路线就是选用这种方法,具体合成步骤下文会谈到,这里不再赘述。第二类是以伯胺或聚氧乙烯为结构导向模板剂,利用具有中性的氢键键合作用,以及非离子型的自组装作用合成的HMS和MSU-x系列介孔硅材料,其产物常见为具有蠕虫状的孔道结构,有序度比较低,其原因可能是氢键的弱相互作用不足以使之形成有序的孔道结构,加上二维孔道结构相较于一维孔道结构更为复杂,很难形成像一维孔道结构一样的有序孔道。其孔壁较厚,且孔径分布较为集中,不够均匀。第三类是以二嵌段或者三嵌段聚合物作为结构导向模板剂合成的介孔硅材料,常见的有六方体型的氧化硅SBA-15,其优点是热稳定性和水稳定性较前两种都有所提高,因此,这种二嵌段或者三嵌段聚合物作为结构导向模板剂合成的介孔硅材料被很多研究学者认为是介孔硅材料合成方面取得的突破性成果。SBA-15型介孔硅孔径较大,孔道分布均匀,重复性好,因此常被用作主体组装客体应用于环境净化和生物医药领域。
据研究显示,改变中空介孔硅的组装层数可以改变中空介孔硅的载药性能,即上文提到的层层自组装技术。实验表明,利用层层自组装技术对介孔硅纳米涂层层数进行控制,随着层数的增加载药量提高,但载药量与组装层数也不是完全的线性关系,原因可能是载药分子数量并不与组装层数成正比,会有其他的影响因素共同决定载药量,例如PH、温度、电解程度等。载药量研究对于中空介孔硅的载药性能起着决定性作用,在相同条件下,尽量多的载药量将成为中空介孔硅最具竞争力的优势。在后面的研究中,成功制备中空介孔硅纳米颗粒之后,会对其载药量进行更加具体细致的研究。
1.4介孔硅纳米阀的种类
如上文所述,中空介孔硅纳米材料在被用作药物载体时,需要配合“纳米阀”这样的介孔包封分子来实现药物在体内的控制释放,因此纳米阀就像是药物控释系统的“钥匙”,需要体内特定的位置打开,将药物全部释放。上文说到,纳米阀在目前有很多种,下面简单地介绍几种常见的适用于介孔硅纳米颗粒的纳米阀。
1.无机纳米粒子作为纳米阀的介孔硅纳米控释系统
2003年,首次研发出了以无机纳米粒子硒化镉量子点作为介孔硅的纳米阀,构建了还原响应型的介孔硅纳米药物控释系统。他们以三磷酸腺苷和万古霉素为药物模型,然后将硒化镉量子点通过双硫键键合在介孔硅表面,从而将药物分子封堵在介孔硅孔道内部。实验显示,硒化镉封堵的介孔硅药物载体在体内可以实现零提前释放,具有良好的包封率。当加入DTT时,硒化镉与介孔硅表面的双硫键断裂,阀门打开,药物得到释放。据文献报道,人体细胞内部含有大量的谷胱甘肽,同样可以将双硫键打断,实现控制释放,因此,该系统还可用于细胞内环境刺激响应性释药行为。此外,磁性纳米粒子四氧化三铁也可以作为介孔硅的纳米阀,实现细胞还原环境响应的药物控制释放。磁性纳米粒子作为纳米阀,可以使系统在外加磁场的作用下定向移动,有助于靶向癌变位置。
金纳米粒子因其独特的物理、化学性质,良好的生物相容性和稳定性,也是优秀的介孔硅纳米阀材料,在相关领域得到了广泛的关注。2009年,Victor Lin团队利用化学反应是金粒子带上正电荷,然后通过静电作用力将其吸附在介孔硅表面,在光照条件下,是金粒子的电荷反转,由于静电排斥作用,Au粒子纳米阀打开,释放药物,由此构建了光敏感性纳米阀。
还有氧化锌量子点也可以作为介孔硅纳米阀材料,由于其在微酸性环境下可以溶解,由此可以构建氧化锌量子点作为纳米阀的药物载体系统,利用其PH响应性,实现药物控制释放,并且氧化锌自身具有细胞毒性,可以提高对癌细胞的杀灭效果。无机分子作为纳米阀的优点是,粒子尺寸可调易于合成。但多数无机纳米粒子不能被生物降解,易于在人体内富集,对机体产生较多毒副作用。
2.有机分子作为纳米阀的介孔硅纳米控释系统
研究人员利用有机分子链的交联作用,实现以有机分子链作为纳米阀的介孔硅药物控释系统,通过偶氮苯与β-环糊精的主客体相互作用,将聚合物交联成网状结构,从而封堵介孔硅孔道。在紫外光照、加入α-环糊精、加入DTT等外界条件下,使可聚物分子间的化学键打断,实现控制释药,构建多刺激响应型的介孔硅药物控释系统。
另外,利用二胺环氧丙基硅烷衍生物在不同的PH条件下的反应,将其修饰在介孔硅表面,也可以构建离子响应型的介孔硅控释系统。聚(4-乙烯吡啶)、聚乙二醇二丙烯酸等皆可作为有机分子介孔硅纳米阀。有机分子分子作为纳米阀的介孔硅纳米控释系统的优点是,聚合物包裹层有优良的包封率,能有效防止客体分子提前释放。但有机分子合成过程复杂,产率低,易产生副反应,同时,有机分子作为纳米阀,本身对生物体无药理作用,同样易产生生物毒副作用。
- 基于分子空间结构形成的纳米阀的介孔硅纳米控释系统
还可以利用有些大分子本身巨大的空间结构,来构建介孔硅纳米阀,例如聚酰胺-胺型树枝状高分子、葡萄糖酸功能化的天然大分子胰岛素、乳糖酸衍生物等。这样的高分子材料,由于本身的空间的结构,可直接用于介孔硅纳米颗粒的纳米阀,通过简单的化学反应,使其与介孔硅表面产生纽带,封堵孔道,然后利用各种材料的化学性质,构建刺激响应型的介孔硅控释系统。
另外,蛋白质、多肽、酶、核酸、亲和素等也可以作为大分子封堵介孔硅孔道,形成纳米阀。其优点是生物大生物大分子大多是人体细胞成分,生物相容性好,对机体几乎无毒副作用。但由于其合成困难,结构复杂,键位连接不紧密等因素,可能导致封堵性不好,刺激响应型难以发掘等问题。
- 基于超分子作用力形成的纳米阀的介孔硅纳米控释系统
基于超分子作用力形成的纳米阀原理是,以二羟基萘衍生物作为分子轴承,将一种联吡啶大环分子通过超分子作用力组装在分子轴承上,对介孔硅孔道进行封堵,构建还原剂响应型的介孔硅控释系统。还可以以环糊精作为主体分子,构建刺激响应型的介孔硅药物控释系统。本方法较为灵活,随着研究的进展,纳米阀的种类会更加多样化。
第二章 实验方案
2.1实验目的
中空介孔硅的现行制备方法有很多种,本文采用溶胶凝胶法制备中空介孔硅,并通过制备过程,研究中空介孔硅纳米颗粒药物载体的特征,掌握中空介孔药物控释系统的原理和设计思路,体会其在现代医药学领域尤其是抗癌药物研究中的应用。熟练掌握中空介孔硅纳米颗粒的简单制备方法,研究其载药原理,并进行载药量研究。通过扫描电镜等手段表征中空介孔硅纳米粒子的形貌。
2.2试剂和仪器
表2.2.1 试剂
试剂 | 化学式 | 纯度 | 厂家 |
氨水 | NH3·H2O | 分析纯 | 国药化学试剂有限公司 |
十六烷基三甲基溴化铵 | C19H42BrN | 分析纯 | 国药化学试剂有限公司 |
正硅酸四乙酯 | C8H20O4Si | 分析纯 | 国药化学试剂有限公司 |
碳酸钠 | Na2CO3 | 分析纯 | 武汉欣万维有限公司 |
甲醇 | CH3OH | 分析纯 | 国药化学试剂有限公司 |
盐酸 | HCl | 分析纯 | 国药化学试剂有限公司 |
乙醇 | C2H6O | 分析纯 | 国药化学试剂有限公司 |
表2.2.2 仪器
仪器 | 型号 | 厂家 |
超声清洗机 | BQS-40 | 昆山超声仪器有限公司 |
分析天平 | FA2104N | 上海精密科学仪器有限公司 |
马尔文纳米粒度和ZETA仪 | Nano S90 | 美国PPS粒度仪公司 |
离心机 | TG16-WS | 湘仪仪器有限公司 |
紫外分光光度计 | 760CRT | 上海精密科学仪器有限公司 |
水浴锅 | HH501S | 常州诺基仪器有限公司 |
2.3实验方案
通过完成资料检索、收集,查阅、整理文献,确定最简单实用的实验方案和进度安排。本实验方案共分为四步,利用十六烷基三甲基溴化铵(CTAB)、正硅酸四乙酯(TEOS)等试剂制备中空介孔硅纳米颗粒(HMSN),并进行载药研究。通过扫描电镜等手段表征中空介孔硅纳米粒子的形貌,之后研究中空介孔硅纳米粒子载药量大小的研究。本实验反应时间较长,需要有足够的耐心,细节的把握很重要。
首先,制备实心SiO₂,利用正硅酸四乙酯(TEOS)、EtOH、NH₃▪H₂O等试剂通过电动搅拌反应生成实心SiO₂,之后进行离心等操作,水和乙醇交替洗涤三次,真空干燥,得到实心纳米硅颗粒。然后,利用十六烷基三甲基溴化铵(CTAB),在乙醇和水的混合溶液中加入氨水,反应完全后用针管滴加正硅酸四乙酯(TEOS),搅拌,离心,水和乙醇交替洗涤三次,干燥,称重,得到SiO₂@CTAB-SiO₂。随后进行SiO₂@CTAB-SiO₂的刻蚀,取上一步全部量,超声分散于水中,取碳酸钠溶液对目标物质进行刻蚀,离心,水和乙醇交替洗涤三次,真空干燥,称重,其中加入碳酸钠溶液的量要根据SiO₂@CTAB-SiO₂的质量而定。最后,制备HMSN,将上一步中制得的刻蚀的SiO₂@CTAB-SiO₂均匀分散到甲醇/盐酸的混合液中,剧烈搅拌12h,之后将上述溶液置于油浴锅中80℃回流48h,回流后8000r/min离心10min,水和乙醇交替洗涤三次,真空干燥,即得最终的中空介孔硅(HMSNs)。实验结果的表征利用马尔文纳米粒度和ZETA仪检测。本实验过程相对简单,制备的产品纯度较高,结果较为理想,但用时较长,具体实施如下。
- 制备实心SiO₂
在500ml三口烧瓶中依次加入:214mlEtOH、30mlH₂O、5mlNH₃▪H₂O,置于30℃恒温水浴下,电动搅拌开启。




